
AGUA
Líquido, sólido y gaseoso
Solvente universal, por lo que es casi imposible tener agua pura. Una clasificación de los grupos
químicos es según su interacción con el agua
Insaboro, incoloro, solo si es pura.
El agua es un dipolo (formación de enlaces, constante dieléctrica)
Se forman enlaces de hidrogeno o puentes de hidrogeno entre ellas: cada molécula de agua
puede interaccionar hasta con otras 4 por enlaces de H (tensión superficial, punto de ebullición
y densidad)
Forma enlaces de H con la mayoría de las moléculas presentes en biología (solvente universal)
Tiene pH neutro (7,0) ya que [𝐻
+
] = [𝑂𝐻
−
]
El agua es un dipolo
Presenta distribución asimétrica de los electrones.
Alrededor del oxígeno se encuentra una densidad de cargas negativas y los núcleos de
hidrogeno presentan una densidad de carga positiva. La carga neta de la molécula es 0 ya que
posee el mismo número de electrones que de protones
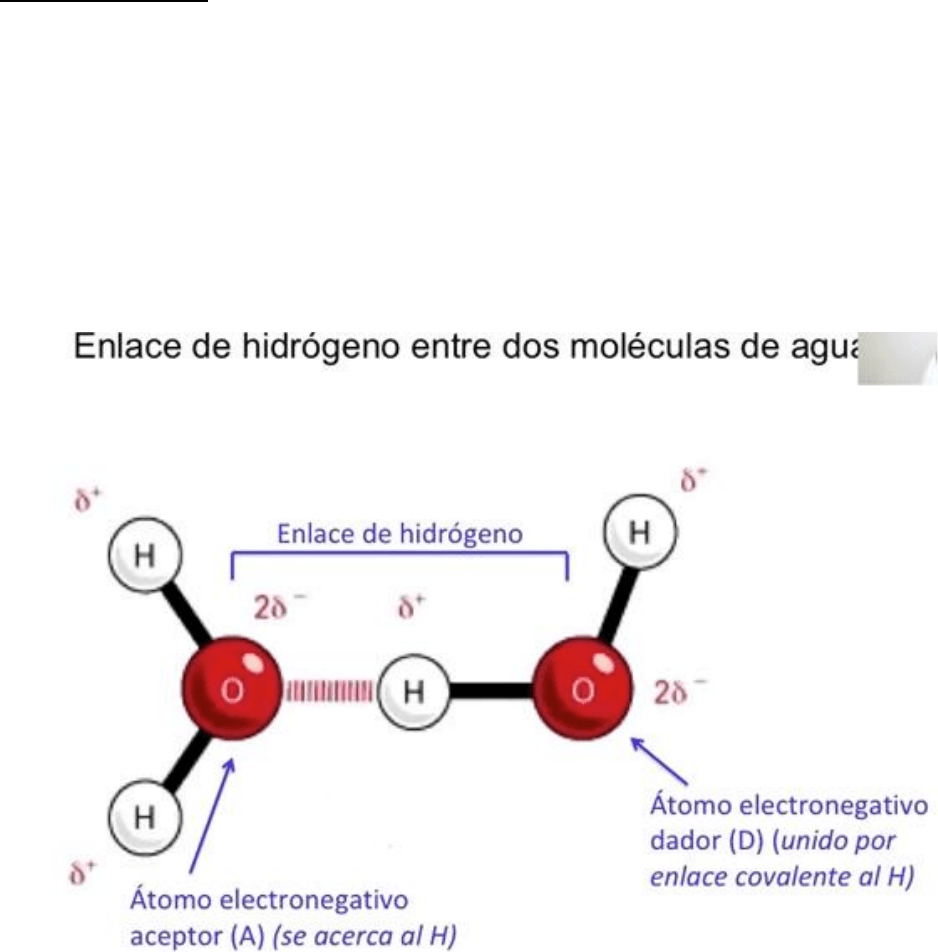
Enlace de hidrogeno
El enlace de hidrogeno es la fuerza atractiva (débil) entre un átomo electronegativo aceptor (A)
y un átomo de (H) unido covalentemente a otro átomo electronegativo dador (D)
A…….H ----D
Átomo dador unido covalentemente al hidrogeno “presta” su átomo de hidrogeno para formar
el puente, el otro átomo que se acerca al hidrogeno es el aceptor
El enlace de hidrógeno es la fuerza atractiva entre un átomo electro negativo aceptor y el
átomo de hidrógeno que está unido en forma covalente a otro átomo electro negativo
En el enlace de hidrogeno entre dos moléculas de agua el átomo electronegativo es el oxígeno.
El átomo aceptor se acerca al hidrogeno de otra molécula de agua
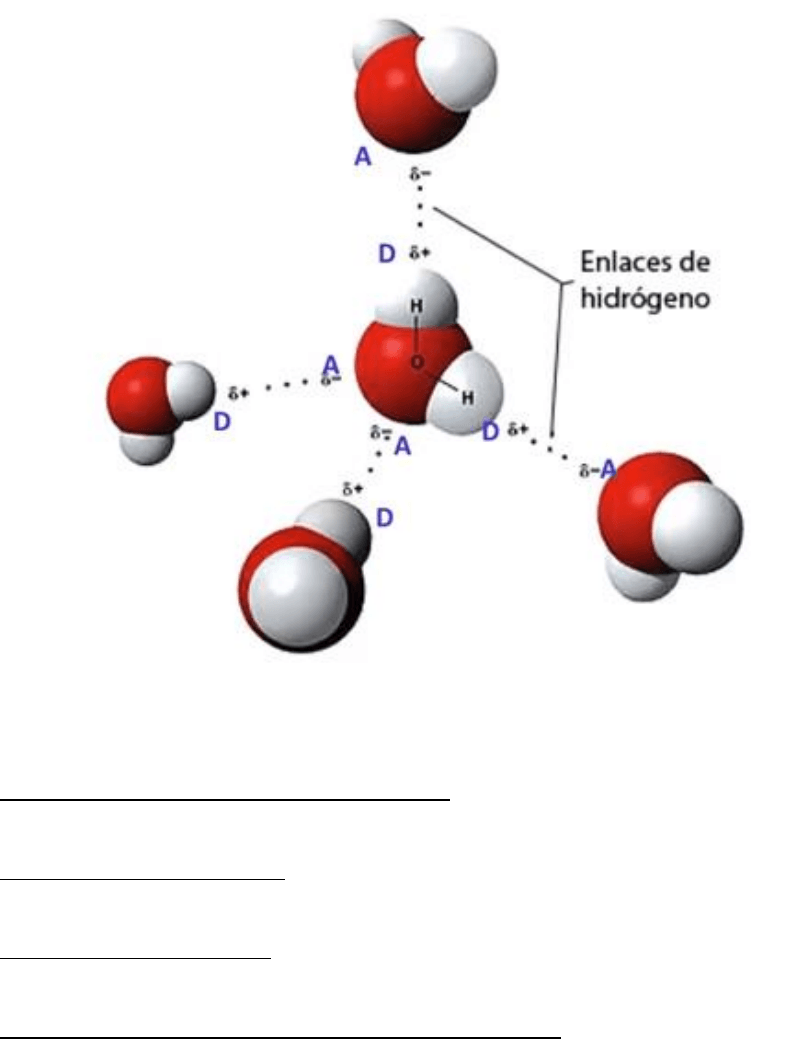
Una molécula de agua puede interaccionar hasta con otras 4 moléculas, en dos de ellas siendo
dador y en las otras dos siendo aceptor
Tensión superficial – elevada cohesión interna: cantidad de energía necesaria para aumentar su
superficie por unidad de área
Elevada constante dieléctrica: hace que los iones no interacciones entre ellos, porque la fuerza
de la interacción es inversamente proporcional a la constante dieléctrica del solvente
Punto de ebullición elevado: temperatura necesaria para romper los enlaces de hidrogeno
entre moléculas
Mayor densidad en estado líquido que en estado gaseoso
Tipos de enlaces químicos
Enlace químico: es la fuerza que une a los átomos para formar compuestos químicos
Los enlaces químicos no son todos iguales, dependen de las características electrónicas de los
átomos involucrados, así como sus valores de electronegatividad, entre otros factores
El enlace covalente ocurre entre átomos que se unen y comparten algunos pares de
electrones de su capa de valencia este es el tipo de enlace de predominante en las
moléculas orgánicas y los ejemplos más conocidos de enlaces covalentes se observan en
las interacciones de los elementos no metálicos entre sí
El enlace iónico consiste en la atracción electrostática entre iones o cargas eléctricas de
signos opuestos los iones podrían formarse a partir de átomos con la transferencia de uno
o más electrones de una toma a otro las sustancias iónicas casi siempre son el resultado de
la interacción entre metales no metales
El enlace metálico se da únicamente entre átomos metálicos como por ejemplo el cobre
hierro y aluminio entre otros por lo general constituyen estructuras sólidas sumamente
compactas es un enlace que une los núcleos atómicos entre sí rodeados de sus electrones
Electronegatividad: es la capacidad de un átomo en una molécula de atraer electrones
hacia sí. Cuanto mayor sea la electronegatividad de un átomo mayor será su capacidad
para atraer electrones
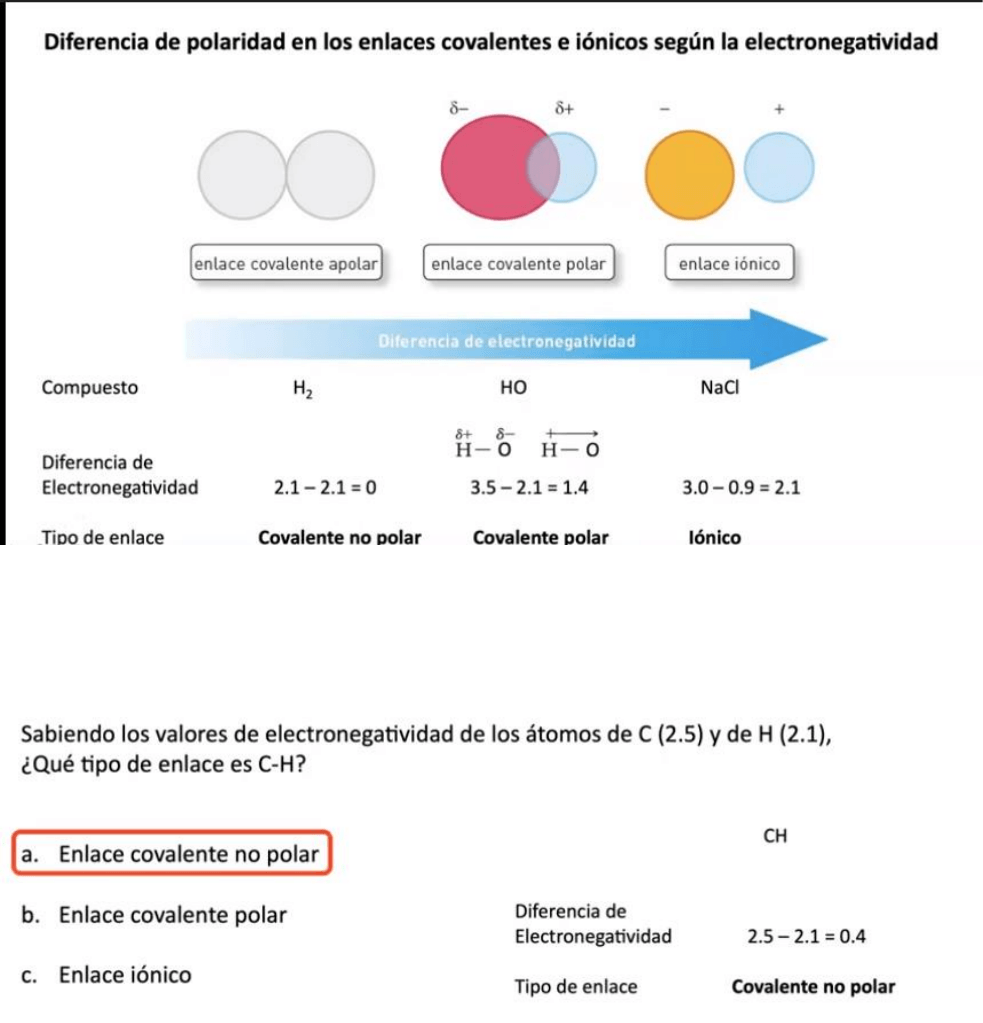
Polaridad de los enlaces y electronegatividad
Enlace covalente no polar: los electrones se comparten equitativamente entre dos átomos
(de 0 a 0,4)
Enlace covalente polar: uno de los átomos ejerce una mayor atracción sobre los electrones
de enlace que el otro (de 0,5 a 1,6)
Enlace ionico: cuando hay una gran diferencia en la capasidad relativa para atraer electrones entre los
dos atomos (mayor a 1,7)

agua, enlaces quimicos y medidas de concentracion.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.