AGUA
Se encuentra en los tejidos y líquidos orgánicos mayormente en estado libre, puede ser disolvente
de sustancias y pasar de un lado a otro, de la sangre a los tejidos, dentro y fuera de las células.
Representa el 60% del peso corporal: intracelular (45%), intersticio (10%) y plasma (5%)
Agua total
Liq intracelular
Liq extracelular
Liq intersticial
Plasma
Hombre
60%
45%
15%
10%
5%
Mujer
55%
40%
15%
10%
5%
Lactante
77%
48%
29%
24%
5%
Estructura del agua
Formada por dos átomos de hidrógenos y un átomo de oxigeno. Cada átomo de hidrogeno esta
unido por un enlace covalente a un átomo de oxigeno. El ángulo del enlace H-O-H es 104.5°.
La disposición de los electrones hace una asimetría eléctrica.
Aunque la molécula de agua no tenga una carga neta, se la considera un dipolo eléctrico (posee
zonas parcialmente positivas y parcialmente negativas). La polaridad de las moléculas de agua
permite que ellas puedan atraerse electrostáticamente entre sí. La unión electrostática de este
tipo se llama puente de hidrogeno: uniones electrostáticas débiles, de vida media corta, se
forman y se rompen constantemente, son cooperativas. El agua posee una elevada cohesión.
Cada molécula de agua es capaz de unirse por puentes hidrogeno con cuatro moléculas de agua.
PROPIEDADES DEL AGUA
Tensión superficial
Cuando la superficie del agua está en contacto con el aire se comporta como si su superficie fuera
una membrana elástica. Las fuerzas de atracción de las moléculas de agua se dirigen hacia todas
las circundantes, pero como en la superficie ya no hay mas moléculas de agua, las moléculas de
agua de esta zona no están sujetas a fuerzas de atracción semejantes proveniente de todas
direcciones, por lo cual tienden a aglutinarse más en esta parte que en otras zonas del liquido.
Capilaridad
Las moléculas de agua, al ponerse en contacto con una superficie como el endotelio de los vasos o
el vidrio de un tubo capilar, se unen a una superficie y atraen hacia ellas a otras moléculas, lo cual
genera un ascenso del líquido.
Punto crioscopico
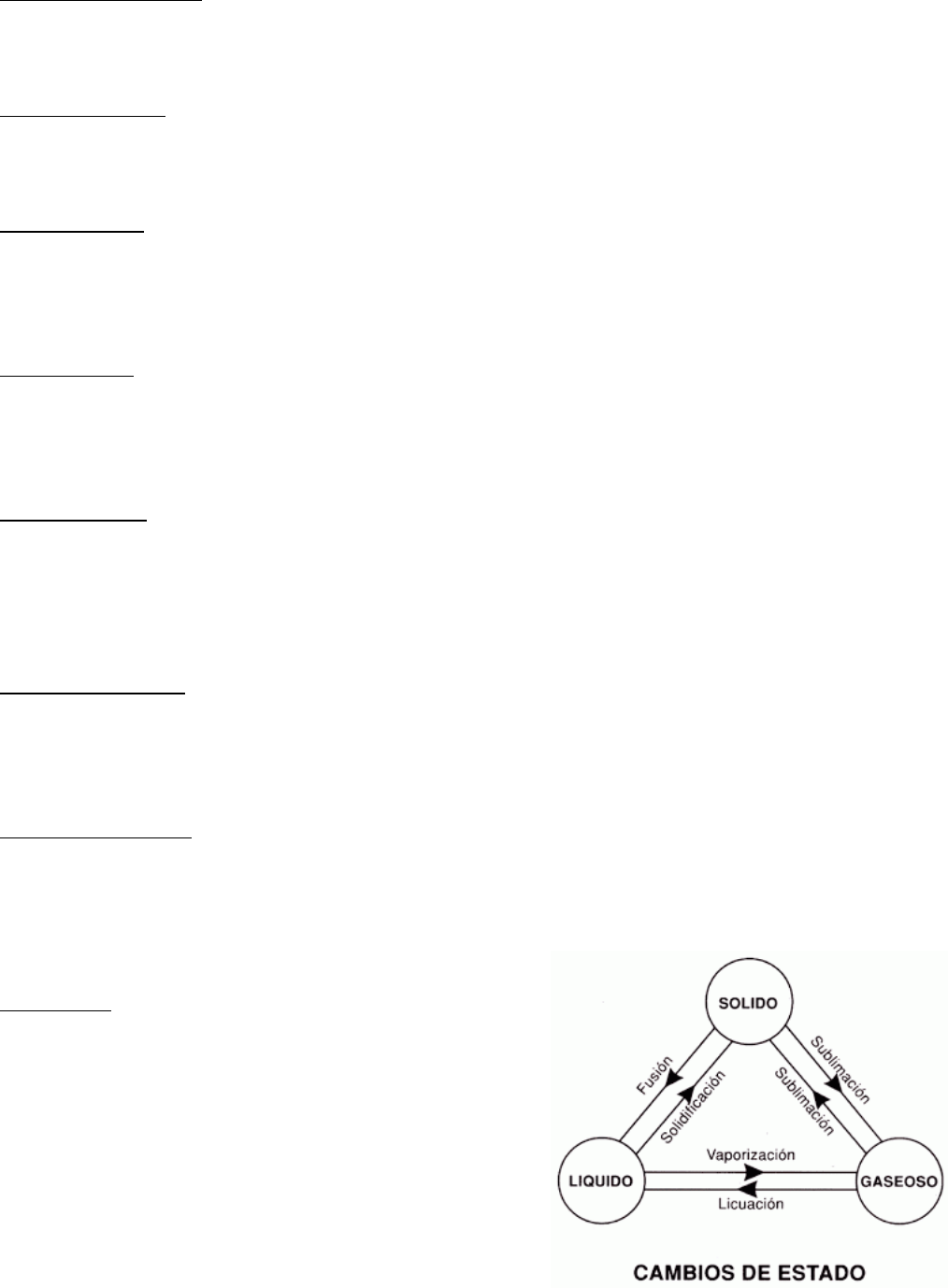
Cuando un liquido se enfría, disminuye la energía cinética de sus moléculas, desaparece el
movimiento y adquiere aspecto de un sólido, esto se llama cristalización, y la conversión de solido
a liquido se denomina fusión. El agua se congela a 0°C (punto de fusión = punto de congelación).
Propiedades coligativas
Dependen del número de partículas de solutos presente en una cantidad específica de disolvente y
varían en proporción directa a la concentración.
Punto de ebullición
El agua líquida se transforma a vapor a 100°C a una presión barométrica de 760 mmHg. Si se
agregan solutos al agua, el punto de fusión disminuye y el de ebullición aumenta.
Presión de vapor
Es la tendencia de las moléculas de agua a escapar hacia el espacio que las rodea lo cual ejerce
presión sobre la atmosfera. Un líquido volátil es aquel que se evapora con facilidad a temperatura
ambiente. Cuando lo hace con lentitud se denomina no volátil.
Calor especifico
Cantidad de calor necesaria para aumentar la temperatura de 1 g de agua de 14.5 a 15.5°C. Al
calor especifico del agua se le asigna un valor de 1 cal/ g °C. Se utiliza para romper los puentes de
hidrogeno intramoleculares. Es básica para estabilizar la temperatura del organismo.
Presión osmótica
Una solución tiene agua y solutos. Las moléculas de soluto ejercen presión sobre las paredes del
recipiente que las contiene. La presión osmótica es la presión que ejerce un mol de una sustancia
no disociable en 1 litro de solución. NaCl tiene 2 osmoles, CaCl2 tiene 3 osmoles.
La presión osmótica potencial de las proteínas se denomina presión oncotica, es de 18 mmHg.
Agua como nucleofilo
En las reacciones metabólicas, los nucleofilos (ricos en electrones) atacan a los átomos deficientes
en electrones (electrófilos), ninguno de estos poseen necesariamente una carga formal positiva o
negativa. El agua es un nucleofilo excelente, que rompe enlaces amida, glucosidico o ester.
HIELO: Congelamiento
En los líquidos, la densidad (peso) aumenta a medida que la temperatura cae, porque las
moléculas individuales se mueven más lentamente, y los espacios entre ellas disminuyen. El agua
en estado sólido ocupa más volumen que en estado liquido. El punto de fusión y de congelación es
0° C, y el calor de fusión es 79.9 cal/ g.
Vaporización
Se produce a 100°C y requiere 540 cal/ g. Para que la molécula
de agua se separe de las moléculas vecinas, deben romperse
los puentes de hidrogeno, lo que requiere de energía térmica.

La interacción con agua influencia la estructura de las biomoleculas
El enlace covalente es el más fuerte y sostiene las moléculas juntas.
Las biomoleculas se doblan para colocar grupos polares y cargas en sus superficies. La mayoría de
las biomoleculas son antipáticas. Los aminoácidos cargados o polares están generalmente en
contacto con el agua, los fosfolipidos cargados de fosfatidilserina y fosfatidiletanolamina también.
Interacciones hidrofobicas: tendencia de compuestos no polares de asociarse entre sí en un
ambiente acuoso, causada por la necesidad de reducir al mínimo interacciones energéticas
desfavorables entre los grupos no polares y el agua, no por la atracción mutua.
Micelas: se forman en medio acuoso. Las colas hidrofobicas se orientan hacia el interior, y las
polares en contacto con el agua. Las disoluciones micelares son disoluciones coloidales. Las
disoluciones micelares reciben el nombre de emulsiones.
Monocapa lipidica: se forma en la interfase aire-agua, las colas hidrofobicas se orientan hacia el
aire y las cabezas polares hacia el agua.
Bicapas lipidicas: están en las membranas biológicas. La parte hidrofilica de los fosfolipidos de la
bicapa delimita ambos lados a la zona hidrofobica, y evita su contacto con el medio acuoso.
Fuerzas Van der Waals: atracciones entre los dipolos transitorios generados por el movimiento
rápido de electrones en todos los átomos neutrales. Son más débiles que el puente de hidrogeno.
Interacciones electrostáticas: interacciones entre grupos cargados con signos opuestos, ayudan a
formar la estructura biomolecular. Cuando las interacciones electrostáticas estén dentro o entre
biomoleculas se llaman puentes salinos.
Agua como solvente: debido al carácter polar de las moléculas de agua.
Sustancias iónicas: sustancias como el ClNa, son en general solubles en agua, suelen formar
atracciones electrostáticas. Cuando se ponen en contacto con el agua, los dipolos de la molécula
originan fuerzas de atracción electrostáticas que vencen las fuerzas de atracción entre los iones Na
y Cl, y así los aniones se mueven libremente.
Sustancias polares no iónicas: también establecen puentes de hidrogeno, ya que presentan
grupos polares como OH, C=O, NH3+. Es el caso de los glúcidos (alcoholes, aldehídos, cetonas) y de
las bases nitrogenadas.
AUTOIONIZACION DEL AGUA
El agua puede actuar tanto como un acido como una base. H20 --- H + OH; 2 H2O --- H3O+ + OH-
Los pares conjugados acido base son: - acido1 y base1 (H2O y OH)
- acido2 y base2 (H3O y H2O)
A 25°C, la constante de equilibrio (Keq) es muy pequeño: el agua está muy poco disociada.
Keq: [H][OH]= 1.86x 10 -16 M 1 L agua = 1 kg agua
[H2O] Concentración molar H2O: 55.5 mol/L: 55.5 M
Kw: [H] x [OH] = 1x 10 -14 a 25°C
[H]= 1x 10 -7 M Solución Acida [H] > [OH]
[OH]= 1x 10 -7 M Solución Básica [H] < [OH]
SOLUCIONES: mezcla homogénea de dos o más componentes que se encuentran en una sola fase.
Solvente o disolvente: se encuentra en mayor cantidad.
Soluto: se encuentra en menos cantidad.
Mezcla heterogénea: presenta dos o más fases, no guarda la misma composición y propiedades
físico químicas en toda su extensión.
Tipos de soluciones
Saturada: solución en equilibrio con un soluto no disuelto.
No saturada o insaturada: es la que contiene menos soluto que el necesario para la saturación.
Sobresaturada o supersaturada: la cantidad de soluto disuelto se encuentra en mayor proporción
que la esperada para la solución saturada, a una determinada temperatura.
SOLUBILIDAD: concentración de soluto que tiene un valor fijo o constante.
La disolución depende de:
-Naturaleza del soluto o solvente: miscibles (líquidos que se mezclan) o inmiscibles (no se mezclan)
-Temperatura: ↑ temperatura ↑ solubilidad del solido
-Presión (en los gases): ↑ presión ↑ solubilidad de los gases (no en líquidos ni sólidos)
UNIDADES DE CONCENTRACION
% masa/ masa
% masa/ volumen
% volumen/ volumen
g st/ 100 g sc
(soluto+solvente:solución)
g st/ 100 ml sc
(soluto+solvente NO: solución)
ml st/ 100 ml sc
Molaridad (M)
Molalidad (m)
Normalidad (N)
Osmolaridad (OsM)
Mol/ lt sc (1000 ml)
1 mol: masa atómica
1 mol: 6.02x 10 23
mol st/ kg sv (1000 g)
No depende de la
temperatura
eq-g st/ lt sc (1000 ml)
Eq/g: PM/n (n° H o OH
o cargas liberadas)
n° eq: n° moles x n
n° eq: N x V (en Lt)
N: M x n
OsM st/ lt sc (1000 ml)
OsM: Molaridad x I (n°
partículas)
OSMOSIS: transferencia de agua a través de una membrana que permite el paso de agua pero NO
el de solutos (membrana selectivamente permeable). En ausencia de otras fuerzas, se dirige de
una menor concentración de soluto (medio hipotónico) a una mayor (medio hipertónico). Cuando
dos o más soluciones tienen el mismo número de partículas disueltas por unidad de volumen y por
lo tanto el mismo potencial eléctrico, son isotónicas: no hay movimiento neto de agua a menos
que se ejerza una presión sobre uno de sus lados.
Membranas biologicas.docx
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.