Actividad eléctrica del corazón:
La actividad eléctrica comienza a nivel de las células que generan de manera espontánea potenciales de acción, llamadas células
marcapaso, en el nódulo sinusal que constituyen el marcapasos primario del corazón. Su frecuencia de descarga es de alrededor de
75 pulsos por minuto. Situado a nivel de la unión de la vena cava superior y la aurícula derecha, está formado por un grupo de
miocitos ramificados que se conectan con las células del miocardio auricular.
Las células del nódulo sinusal están sometidas a una acción de estiramiento que puede modular su frecuencia de descarga (función
de tipo mecanorreceptor). Este estiramiento sería inducido por la presencia de la arteria del nódulo sinusal
(desproporcionadamente grande en relación con el tamaño del nodulo) y por la distensión de las paredes de la aurícula durante el
arribo de sangre proveniente de las venas cavas.
El nódulo auriculoventricular localizado en el piso de la aurícula derecha, contiene células similares a las de nódulo sinusal, pero su
frecuencia intrínseca de descarga es menor. La irrigación del nódulo proviene en el 90% de los casos de la arteria coronaria derecha
y en el 10% restante de la izquierda. La lenta conducción del impulso a través del nódulo engendra un retardo entre la activación
auricular y ventricular, lo que permite una contracción secuencial de esas cámaras. Las fibras inferiores del nódulo
auriculoventricular convergen y forman el haz de his que desciende por el tabique interventricular, donde se divide en dos ramas:
derecha e izquierda. Esta última se divide en dos fascículos: anterior y posterior. Las ramas del haz de his terminan en las fibras de
purkinje, células de gran diámetro cuyas propiedades eléctricas les confieren la mayor velocidad de conducción. Estas células
forman una red subendocardica, a partir de la cual transmiten el influjo eléctrico al músculo ventricular.
Tres haces conectan los nódulos sinusal y auriculoventricular, cuyas fibras presentan características similares a las de las fibras de
purkinje. Estos haces, llamados internodal anterior, medio y posterior, nacen en la periferia del nódulo sinusal y descienden por la
pared auricular hasta alcanzar el nódulo auriculoventricular. Un cuarto haz constituye una banda superficial que parte de la base de
la vena cava superior y pasa de la aurícula derecha a la izquierda.
El corazón cumple su función merced a la activación y contracción secuencial de las aurículas y los ventrículos, que resulta de la
interacción de cuatro propiedades fundamentales: la excitabilidad, el automatismo, la conducción y la contractilidad. Estas
propiedades dependen de mecanismos existentes en la membrana celular, que crean y mantienen amplio gradientes iónicos entre
los medios intracelular y extracelular.
Potencial de acción cardíaco:
El potencial de acción cardíaco se conduce de una célula a otra a través de uniones en hendidura, esta es una sinapsis eléctrica que
permite que la corriente eléctrica fluya entre dos células vecinas.
El fenómeno de exitación dura alrededor de 0,5 mseg en la fibra nerviosa, 5-10 ms en la fibra muscular esquelética y 250 ms en la
fibra cardíaca ventricular. La considerable duración del potencial de acción cardíaco se debe principalmente a la corriente de calcio
que mantiene un flujo entrante de cargas positivas una vez que la corriente rápida de sodio ha sido inactivada.
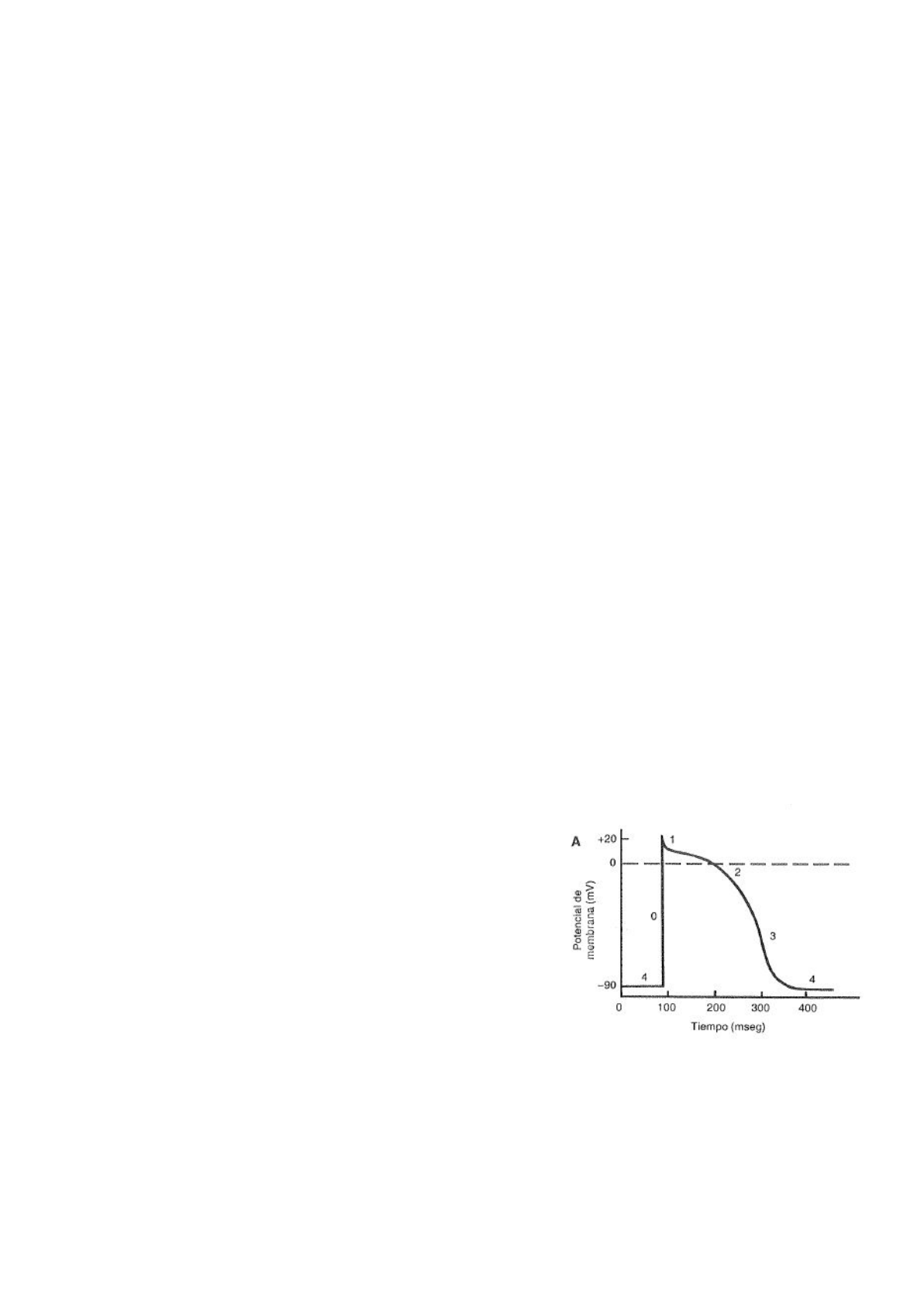
La figura de la derecha representa esquemáticamente un potencial de acción ventricular (el más utilizado para el estudio del
corazón), el cual se divide en cinco fases. la número 4 corresponde al potencial de membrana en ausencia de actividad eléctrica
(potencial de reposo). La fase 0 (despolarización rápida) desplaza el Vm a
valores positivos entre 15 y 25 mV, y es seguida por una breve repolarizacion
rápida temperada (fase 1) que retorna el potencial de membrana a valores
cercanos a cero. Esta se continúa con la fase 2 o meseta, qué es responsable
aproximadamente del 70% de la duración total y es característica del
potencial de acción cardíaco. La fase 3 de repolarizacion rápida tardía
retorna el potencial de membrana al valor de reposo. Ciertas características
de estas fases determinan las propiedades del miocardio. La velocidad de
despolarización de la fase 0 desempeña un papel preponderante en la
conducción. La duración de la meseta controla la entrada de calcio, factor
clave en el acoplamiento excito-contráctil, y es responsable de la
imposibilidad del miocardio de contraerse titanicamente porque durante
este periodo la célula es refractaria.
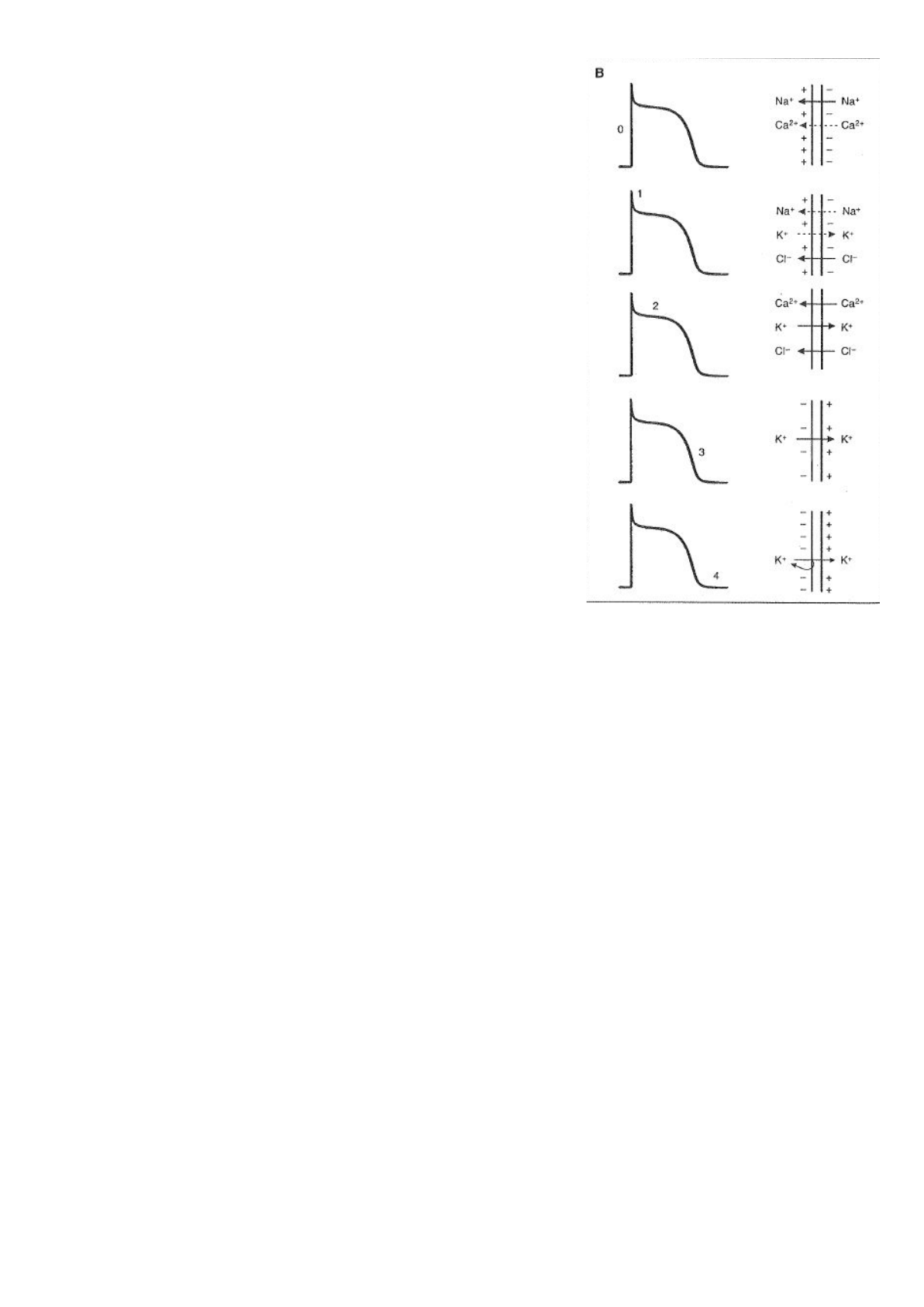
● Fase 4 (PMR): Corriente de potasio con rectificación hacia adentro (Ik1): El PMR
de las células cardíacas es determinado fundamentalmente por la distribución
asimétrica del ion K y por la permeabilidad al potasio. El potencial de membrana
en reposo de las células ventriculares y auriculares determinado casi
exclusivamente por la corriente de K a través de los canales conocidos como
“rectificadores hacia adentro”(Ik1). La característica más notable de Ik1 es que
deja pasar más corriente hacia dentro de la célula que hacia afuera. Sin embargo,
la corriente de K hacia afuera es la que atraviesa este canal en forma fisiológica,
ya que el potencial de membrana raramente se hiperpolariza por debajo del
potencial de equilibrio para el K (Ek).
El PMR en el miocardio varía según el tipo celular: es de 60 mV en las celulas
nodales (SA y AV), de -80 mV en la auriculares y ventriculares y de -90 mV en los
otros tejidos de conducción (His y purkinje).
● Fase 0: corriente de sodio (INa): La fase 0 constituye la despolarización rápida del
potencial de acción. en las células ventriculares así como en las células auriculares
y de la red de his-purkinje, esta rápida despolarización depende de la apertura de
los canales rápidos de Na (se abren a -70 mV) similares a los presentes en
músculo esquelético y nervio. Esta corriente de Na (INa) es designada como
rápida porque exhibe cinética de activacion e inactivacion muy rápida en
comparación con otras corrientes. Debido a que los canales rápidos de Na son
operados por voltaje, luego de una despolarización la compuerta de activación se
abre y INa llega a su pico aproximadamente a 1 mseg. Luego de la activación pico
de INa la corriente comienza a disminuir debido al cierre de los canales mediante
el proceso de inactivacion. Una vez que el canal se encuentra en estado inactivo
no puede volver a abrir a menos que se reactive. La reactivación sólo es posible a
potenciales negativos y luego de un lapso determinado. es decir, lo mismo que la
activación y la inactivación, el proceso de reactivación depende de voltaje y del
tiempo.
El potencial de membrana nunca llega a ENa por diversas razones: 1) a medida que el potencial de membrana se acerca ENa, la
fuerza impulsora que promueve el ingreso de Na disco disminuye; 2) los canales de Na se inactivan inmediatamente luego de su
apertura; 3) las corrientes repolarizadora se empiezan a activar Durante la etapa final de la fase 0. por lo tanto, durante la fase 0, el
potencial de mebrana más positivo que se alcanza es de aproximadamente +35 mV, lo que determina un cambio de potencial de
110 a 120 mV en sólo unos 2 mseg.
A PMR muy polarizados (-90 mV), un estimulo supraumbral generará una fase 0 rápida y de gran amplitud, mientras que a PMR
parcialmente despolarizados (-70 mV), un estímulo similar producirá una fase 0 lenta y de menor amplitud. Esto se debe a que la
despolarización subumbral del PMR previo al estímulo a inactivado algunos canales de Na al cerrar sus compuertas de inactivacion.
Este fenómeno es evidente luego de la despolarización del PMR producido por la acumulación de K en el medio extracelular qué
ocurre durante la isquemia miocárdica. si el umbral se alcanza rápidamente, la fase 0 es rápida y de Gran amplitud. En cambio, si el
umbral se alcanza lentamente, hay más tiempo para que la dependencia de voltaje de la inactivación se haga más importante, y la
fase 0 es más lenta y de menor amplitud.
● Fase 1: corriente transitoria hacia afuera (Ito): La fase 1 del potencial de acción cardíaco consiste en una rápida repolarización
transitoria del potencial de membrana que sigue inmediatamente a la fase 0. La fase 1 varía de una especie a otra y además en
diferentes regiones del corazón de una misma especie. Esta repolarizacion temprana se debe primariamente al egreso de K (e
ingreso de Cl).
La corriente responsable de la fase 1 se denomina “transitoria hacia afuera” y se la expresa como Ito. Ito se produce por la apertura
de los canales dependientes de voltaje y del tiempo. Además, estos canales también presentan inactivación luego de pasar por el
estado abierto. Estas características hacen que Ito sea transitoria. el umbral para su activación es de aproximadamente -30 mV. La
reactivación de Ito auricular es más rápida que la ventricular y por eso el potencial de acción ventricular a menudo carece de fase 1
a frecuencias normales.
Ito está compuesta por dos corrientes separadas: Ito1 e Ito2. Ito1 es una corriente de K qué es independiente de la concentración
interna de Ca++ para su activación y es sensible al bloqueador 4- aminopiridina. Ito2, depende del Ca++ intracelular para su
activación y el ion permanente es Cl (ICl-(Ca)). ICl(Ca) es más importante durante la primera porción de la meseta del potencial de
acción (fase 2), una vez que el Ca++ citosolico ha aumentado. Ito1 es la más importante de las dos para generar la fase 1.
● Fase 2: corriente de calcio (ICa): Corresponde a la meseta del potencial de acción. Es un período durante el cual el valor del
potencial de membrana se mantiene relativamente constante durante varios milisegundos. La presencia de esta prominente
meseta es responsable de la larga duración del potencial de acción en las células cardíacas, la cuál es la mayor diferencia entre los
potenciales de acción de las células cardíacas y las esqueléticas o nerviosa. La meseta es causada por un balance entre corrientes
cationicas hacia el interior de la célula (despolarizantes) y corrientes catiónicas hacia el exterior de esta (polarizantes). La principal

corriente despolarizante es una corriente de Ca++ (ICa). Las corrientes repolarizante son la corriente de Cl (ICl(Ca)), y por
corrientes de K a través de los dos canales diferentes: la ya mencionada Ito1, la de potasio tardía. Está, es la corriente responsable
de repolarizar el potencial de membrana durante la fase 3. La corriente de Ca++ de la fase 2 se produce a través de canales
operados por voltaje y que presentan inactivación. La cinetica de inactivacion de estos canales es lenta se los llama canales de
Ca++ tipo L o de larga duración (ICa-L). Existen también en las células cardíacas canales de Ca++ con cinéticas de activacion e
inactivacion más rápida que los canales L. Son los llamados canales Ca+ de tipo T o de apertura transitoria (ICa-T).
ICa-L es el nexo primario en el acoplamiento excito contráctil cardíaco. El ingreso de iones de Ca++ a través de los canales L durante
la meseta del potencial de acción es lo que liga los acontecimientos eléctricos del potencial de acción con Los mecánicos, ya que
estimula la liberación de Ca++ de los depósitos intracelulares (liberacion de Ca inducida por Ca), la reposición de intracelulares y, en
menor medida, la activación directa de las proteínas contráctiles.
● Fase 3: corriente tardia de potasio (Ik):La fase 3 corresponde a la repolarizacion final del potencial de acción y se debe a la
corriente generada por la lenta apertura de los canales de K tardios (Ik). La fase 3 es causada primariamente por el desbalance de
las corrientes que estaban relativamente equilibradas durante la fase 2. Debido a la inactivación de los canales de Ca, ICa-L
disminuye mientras que Ik aumenta. Ik es generada por canales de K operados por voltaje, pero que carecen de inactivacion. Son
canales de activacion muy lenta que se activan gradualmente durante la despolarización sostenida de la fase 2 y que se
encuentran plenamente abiertos durante la fase 3.
Durante la fase final de la fase 3, Ik1 contribuye a repolarizar el potencial de membrana y a regresar al PMR. Se han descrito dos
componentes de Ik. Uno que se activa relativamente rápido (Ikr) y otro que se activa muy lentamente (Iks).
Corrientes adicionales que contribuyen al PA cardiaco:
● Corriente de K activada por acetilcolina (Ik(ACh)): La acetilcolina activa los receptores muscarínicos M2 y, via proteína G, activa a
una corriente saliente de K+ mediada por GIRK (canales de K+ rectificadores de entrada activados por subunidades βγ de
proteína G). Esta corriente es notoria en las células de los nodos SA y AV, en las que disminuye el ritmo de marcapasos mediante
hiperpolarización celular. También desacelera la propagación del potencial de acción a través del nodo AV.
● Corriente de Cl estimulada por AMPc (ICl(AMPc)): Cuando los niveles intracelulares de AMPc aumentan (por estimulación
simpática por ejemplo), se hace más evidente una corriente saliente de Cl que acorta el PA.
● Corriente de la bomba Na-K (Ipump): Ipump (hiperpolarizante) se encarga de mantener el PMR durante la fase 4 junto con Ik1.
● Corriente del intercambiador Na/Ca++ (INa/Ca): contribuye al potencial de membrana tanto en reposo como durante del potencial
de accion. Ingresa 3 Na y saca un Ca++ por lo que introduce una carga positiva (corriente despolarizante). Aunque tambien puede
trabajar de modo inverso produciendo una corriente polarizante.
● Corriente de K sensible a ATP (Ik(ATP)): son activados ante una disminucion de la [ATP]i. En condiciones normales no contribue al
PA, por lo general, se activan durante isquemias cardiacas.
Periodos refractarios y supernormales:
La reactivación demorada de los canales rápidos de Na dependientes de voltaje determina la refractariedad del corazón. El tiempo
durante el cual el potencial de membrana permanece a niveles más positivo que -60 mV, prácticamente entre las fase 0 y el tercio
inferior de la fase 3, corresponde al período refractario absoluto. a valores de Vm entre -60 y -80 mV encontramos el período
refractario relativo.
Luego del período refractario relativo se encuentra una corta fase de súper normalidad en la que se puede provocar una respuesta
con un estímulo menor que el normal, porque el Vm se halla más cerca del umbral y los canales de sodio están casi totalmente
recuperados. Para frecuencias cardíacas normales, el período refractario absoluto dura unos 200-250 mseg y los periodos
refractarios relativo y de súper normalidad entre 30-50 mseg cada uno. en el músculo auricular estas cifras se reducen a la mitad.
Diferencias regionales en los potenciales de acción cardíacos:
● Nódulo sinoauricular: el nódulo sinusal contiene células especializadas que generan potenciales de acción. Estás, no presentan un
potencial de membrana estable entre los potenciales de acción. La fase 4 muestra una lenta despolarización espontánea que se
denomina potencial de marcapaso. Dado que estas células no presentan un verdadero potencial de reposo, se denomina potencial
diastolico maximo (PDM) al potencial más negativo que alcanza la célula entre los potenciales de acción. Este potencial es menos
negativo que los potenciales de reposo del resto de las células cardíacas debido a una permeabilidad disminuida al K a potenciales
negativos causada por la carencia de Ik1 en las células del nódulo sinusal. El PDM de estas últimas varía entre -55 mV en las
verdaderas células del nódulo y -70 mV en las células de transición que se ubican en el límite entre el nódulo y las aurículas. El
potencial de marcapaso lleva el PDM al umbral para generar un potencial de acción.
Una vez que se alcance el umbral se produce la despolarización de fase 0 que tiene lugar por la apertura de los canales de calcio de
tipo L y no por los canales rápidos de Na, que se encuentran inactivados al PDM y durante el potencial de marcapaso. Cómo los
canales de calcio tipo L tienen una cinética más lenta qué los canales de Na, la fase 0 de las células del nodulo es más lenta que la de
las células ventriculares. No hay fase 1 y la fase 2 es breve. La fase 3 es determinada por la apertura de los canales de K tardíos que
retornan el potencial de membrana al PDM para así iniciar un nuevo ciclo.
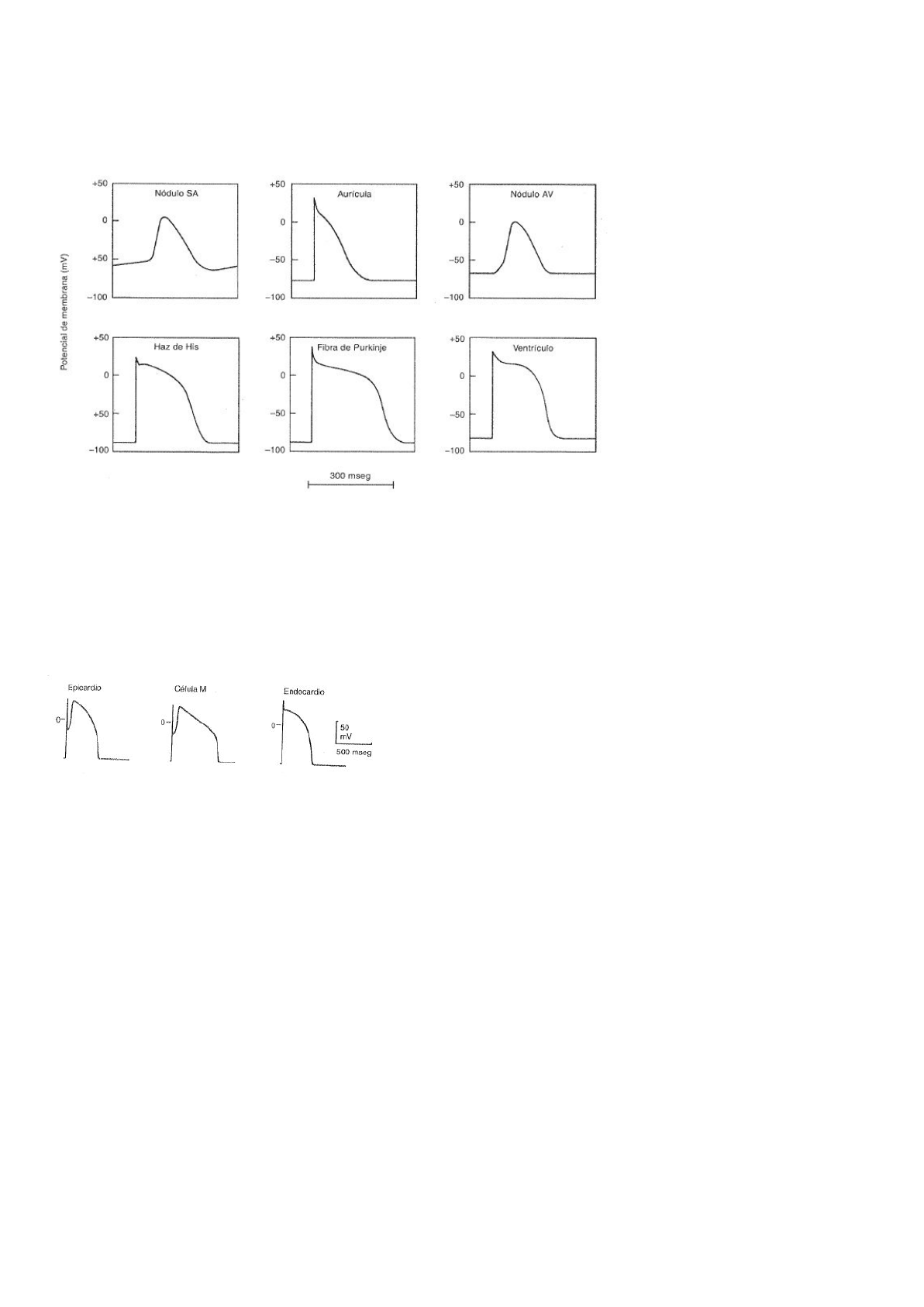
● Aurícula: el potencial de reposo es de alrededor de -85 mV y la fase 0 es rápida, generada por INa. Generalmente carece de
meseta. posee una prominente fase uno que se debe a una predominante Ito presente en estas células.
● Nódulo auriculoventricular: presentan despolarizacion espontáneas durante la fase 4 y la despolarización de fase 0 es producida
por los canales de calcio de tipo L. La despolarización espontánea de fase 4 es más lenta que la del nódulo sinusal.
● Fibras de purkinje: similares al típico potencial de acción ventricular. Las células del haz de his poseen potenciales de acción muy
similares a los de las células de purkinje. Poseen una fase 1 prominente y una larga meseta. Además presentan automatismo.
● Ventrículo:
Las células del epicardio poseen una prominente fase 1 en relación con las células del endocardio esto se debe a la mayor densidad
de canales generadores de Ito en el epicardio.
Las células M (miocardio) poseen una fase 1 prominente (al igual que las células del epicardio y por las mismas razones). Presentan
una prolongada duración del potencial de acción, esto hace que sean las últimas células miocárdicas en repolarizarse en forma total
y muy posiblemente generen esta manera la onda U del ECG. La prolongada duración del potencial de acción de las células M que se
debe a una disminuida densidad de canales de K generadores de Iks.
Las células del endocardio casi no tiene Ito (fase 1).
AUTOMATISMO:
El corazón normal Tiene tres tejidos con actividad de marcapasos intrínseca: El nódulo sinusal, el nodulo auriculoventricular y las
fibras de purkinje. La capacidad de despolarizarse espontáneamente se conoce como automatismo cardíaco. La frecuencia de
descarga derivada de la despolarización espontánea depende de tres factores: el potencial de reposo, la velocidad de
despolarización de la fase 4 y el potencial umbral. Mientras menor sea la diferencia entre el umbral y el PDM y mayor la velocidad
de despolarización, mayor será la frecuencia de descarga de una célula. Se considera que las células del nódulo sinusal tienen el
potencial de reposo menos negativo del corazón y la velocidad de despolarización espontánea más rápida, es fácil entender que
estas células sean las primeras despolarizarse, y asuman la función de marcapasos primario del corazón. Una vez que el nódulo
sinusal dispara potencial de acción, la onda de despolarización se propaga a otras regiones del corazón. Las células automáticas de
estas otras zonas del corazón no tienen en condiciones normales la oportunidad de disparar constantemente potenciales de acción
antes que la onda de despolarización proveniente del nódulo sinusal las alcance y las lleve hasta el umbral de exitación.
● Automatismo de las fibras de purkinje: en condiciones fisiológicas las fibras de purkinje pueden tener un potencial de marcapaso
extremadamente lento en la fase 4. Las fibras de purkinje poseen todas las corrientes presentes en las células ventriculares más
una corriente adicional denominada If (corriente funny, rara). If es la corriente responsable de la mayor parte de la corriente
despolarizante que genera el potencial de marcapaso de las células de purkinje. Se trata de una corriente cationica a través de los
canales no selectivos que dejan pasar tanto Na (ingreso) como K (egreso). Cuando este canal se abre a potenciales negativos
predomina el ingreso de Na por sobre el egreso de K y la célula se despolariza lenta y espontáneamente hasta que abre los
canales Na dependientes de voltaje que disparan el potencial de acción.
● Automatismo en las células del nódulo sinusal: diversos factores contribuyen al potencial de marcapaso de las células del nódulo
sinusal. La corriente despolarizante If también está presente en las células del nódulo sinusal y contribuyen al potencial de
marcapasos en ellas. Además una corriente de Na denominada INa-B también contribuye a la despolarización. Para que esto
suceda, INa-B debe predominar sobre la corriente repolarizadora de K, Ik, qué es la responsable de la fase 3. Ik no presenta

inactivacion, pero su conductancia se reduce a medida que el potencial de membrana se repolariza. Ik decae lentamente a medida
que el potencial de membrana se aproxima al potencial diastolico maximo, lo que hace que INa-B comience a predominar sobre Ik
y se inicie el potencial de marcapaso que despolariza espontáneamente a la célula. Por último, la corriente de calcio a través de los
canales T (ICa-T) contribuye a despolariza la membrana durante la fase final del potencial de marcapasos. En resumen, el potencial
de marcapaso de las células del nódulo sinusal es determinado por el aumento de ingreso de Na a través de los canales que
generan If e INa-B, el aumento de ingreso de calcio a través de los canales de tipo T y la disminución de egreso de K a traves de los
canales responsables de Ik.
● Automatismo en las células del nódulo AV: Al igual que el nodo SA, la ritmicidad intrínseca del nodo AV depende de la interacción
de tres corrientes de membrana tiempo y voltaje-dependientes: Ik, ICa e If. Como el ritmo de marcapasos intrínseco del nodo AV
es más lento (aproximadamente 40 latidos/min) que el del nodo SA, no determina la frecuencia del corazón; su actividad de
marcapasos se considera secundaria.
If:
La corriente marcapasos (If) se observa en las células de los nodos SA y AV y en las fibras de Purkinje. El canal que subyace a esta
corriente es un canal catiónico inespecífico llamado HCN (activado por hiperpolarización, AMPc-dependiente). Como los canales
HCN conducen tanto K+ como Na+, el potencial de inversión de la If se sitúa alrededor de los −20 mV, entre los potenciales de
Nernst para el K+ (aproximadamente −90 mV) y para el Na+ (aproximadamente +50 mV). Los canales HCN tienen la propiedad
inusual (de ahí el subíndice f para corriente «funny» o extraña) de que no conducen a valores de Vm positivos sino que se activan
por la hiperpolarización al final de la fase 3 y se inactivan cuando la celula se despolariza. La activación es lenta (100 ms) y la
corriente no se inactiva. De este modo, la If produce una corriente despolarizante de entrada mientras se activa lentamente al final
de la fase 3. La If no es la única corriente que contribuye a la actividad de marcapasos; en las células de los nodos SA y AV, la ICa y la
Ik también contribuyen de un modo significativo a la despolarización de la fase 4.
If es inhibida por ivabridina y se utiliza cuando hay un aumento de la actividad simpatica en el corazon (taquicardia).
Existen dos teorias de como se genera el automatismo:
● El marcapaso de Difrancesco: Propuesta por Difrancesco, el decia que If es la corriente despolarizante responsable de
generar el potencial de marcapasos de las células especializadas.
● El reloj de Lakatta: propuesto por Lakatta, el decia que una corriente llamada “corriente derivada del intercambiador Na/Ca
(Incx)” era exclusiva para producir el automatismo. Lakatta descubre que hay una liberacion minima de calcio que aparece
antes del PA, y propone que el reticulo sarcoplasmatico es quien libera ese calcio al citosol de manera ciclica y sincronizada
(no se sabe el motivo). Este calcio activa a Incx, que encuentra el calcio, lo saca e introduce Na, que es quien genera la
corriente despolarizante responsable de generar el potencial de marcapasos de las células especializadas.
Difrancesco y Lakatta estuvieron peleados por mucho tiempo debido a quien tenia la razon. Finalmente, se amigan y acuerdan que:
If es importante para iniciar el potencial diastólico de marcapasos (DD), pero no parece ser la única corriente responsable, ya que su
bloqueo no suprime totalmente el automatismo. Por lo tanto, If es importante al inicio, luego aparece Incx, y finalmente Ica-T
termina de contribuir a la despolarizacion.
Propagacion del impulso:
Paso 1: Una vez que el nodulo SA dispara el potencial de accion, en el interior de cada aurícula el potencial de acción se propaga
entre los miocitos cardíacos a través de una vía directa de una célula a otra siguiendo un eje general de derecha a izquierda y hacia
abajo. El PA viaja, tambien, a traves de 4 vias internodales: anterior, media, posterior y el Haz de Bachmann, hasta el nodo AV. Una
vez que el potencial de acción alcanza el nodo AV discurre hasta el entramado de fibras de His-Purkinje y sale de nuevo al músculo
ventricular.
Paso 2: el tabique se despolariza de izquierda a derecha.
Paso 3: se despolariza la región anteroseptal.
Paso 4: el miocardio siempre se despolariza desde el endocardio (células que revisten a los ventrículos) hacia el epicardio (células en
la superficie externa del corazón). El ápex del ventrículo izquierdo se despolariza cuando las fibras de Purkinje están aún en proceso
de conducir el potencial de acción hasta la base del ventrículo izquierdo.
Paso 5: la despolarización se propaga desde el ápex hasta la base a través de las fibras de Purkinje. Esta propagación hasta la base
comienza incluso aunque la señal en el vértice esté propagándose aún desde el endocardio al epicardio. La última región en
despolarizarse es la región posterobasal del ventrículo izquierdo.
Paso 6: los ventrículos están completamente despolarizados.
El retardo de conducción no es proporcional a la distancia recorrida, lo cual indica que la velocidad de propagación no es uniforme.
En contraste con el miocardio ordinario y las vías de conducción rápida, los potenciales de acción de las celulas nodales presentan
menor amplitud y una fase cero más lenta porque la corriente de calcio constituye el elemento predominante de la excitación. El
mayor retardo de conducción se observa entre el nódulo auriculoventricular y el haz de his. Esto se debe al hecho de que un
potencial lento genera corrientes locales débiles y, por lo tanto, es menos apto para la conducción. Además, las uniones
intercelulares comunicantes o en hendidura son menos numerosas en el nódulo auriculoventricular. El miocardio se comporta como

una célula única gigante (sincitio funcional) debido a la presencia de los discos intercalares que contienen conexones que permiten
el paso de iones y moléculas de bajo peso molecular (ATP, glucosa,etc) y constituyen vías de baja resistencia eléctrica. Estos canales
conducen la corriente del circuito local, de manera que el flujo qué parte del nódulo sinusal se propaga a toda la masa del tejido.
La permeabilidad de estos canales es controlada por el pH y el calcio intracelular. La acidosis y la sobrecarga cálcica existentes en la
isquemia prolongada provocan la ruptura de estas conexiones, lo que aísla al tejido normal del tejido infartado en vías de necrosis.
El intercambiador Na/Ca contribuye a modular la fuerza de contracción. El movimiento neto de calcio producido por este
mecanismo puede contribuir a la entrada de calcio durante la sístole y a su salida durante la diástole. Los intercambiadores Na-H y
Cl-HCO3 y el cotransportador Na-HCO3 contribuyen a mantener constante el pH del citoplasma.
El corazon se despolariza desde endocardio a epicardio, y se repolariza al revez. La heterogeneidad transmural de las corrientes de K
entre epicardio y endocardio generan esta diferencia en la conduccion.
Modulacion de la actividad marcapasos, velocidad de conduccion y contractilidad:
Tres mecanismos pueden ralentizar el ritmo de descarga del nodo SA (es decir, un efecto cronotrópico negativo). En primer lugar,
puede disminuir la pendiente de la despolarización durante la fase 4, alargando de este modo el tiempo necesario para que el Vm
alcance el umbral. De este modo la diástole es más larga y disminuye la frecuencia cardíaca. En segundo lugar, el potencial diastólico
máximo puede volverse más negativo. En este caso el Vm empieza la fase 4 a un potencial más negativo y de este modo tarda más
en alcanzar el umbral, suponiendo que la pendiente de la despolarización de la fase 4 no haya variado. En tercer lugar, el umbral
para el potencial de acción puede volverse más positivo. Asumiendo que no cambia el potencial diastólico máximo ni la pendiente
de la despolarización de la fase 4, el Vm requerirá más tiempo para alcanzar un umbral positivo. Obviamente, la combinación de
estos tres mecanismos tendría un efecto potenciador. Por el contrario, las células del nodo SA pueden usar cada uno de estos tres
mecanismos en el sentido opuesto para incrementar el ritmo de descarga (efecto cronotrópico positivo).
-Acetilcolina: El nervio vago, que es parasimpático, libera acetilcolina (ACh) a los nodos SA y AV y ralentiza la actividad marcapasos
intrínseca por los tres mecanismos comentados en el párrafo anterior. En primer lugar, la ACh disminuye la If en el nodo SA,
reduciendo la pendiente de despolarización de la fase 4. En segundo lugar, la ACh abre los canales GIRK aumentando la
conductancia relativa del K+ y haciendo que el potencial diastólico máximo de las células del nodo SA sea más negativo. En tercer
lugar, la ACh reduce la ICa en el nodo SA, disminuyendo de este modo la pendiente de despolarización de la fase 4 y desplazando
también el umbral hasta valores más positivos. Estos tres efectos cooperan para alargar el tiempo para que el nodo SA se
despolarice hasta su umbral; el efecto neto es una disminución de la frecuencia cardíaca. El efecto fisiológico de la ACh sobre el
nodo AV es ralentizar la velocidad de conducción. El mecanismo se basa en la inhibición de la ICa que también vuelve el umbral más
positivo para las células del nodo AV. La velocidad de conducción disminuye porque a la célula le resulta más difícil despolarizar a las
células vecinas.
-Las catecolaminas (adrenalina y noradrenalina), que actúan a través de receptores β1-adrenérgicos, producen un aumento de la
frecuencia cardíaca por dos mecanismos. En primer lugar, aumentan la If en las células nodales incrementando de este modo la
pendiente de despolarización de la fase 4. En segundo lugar, las catecolaminas aumentan la ICa en todas las células miocárdicas. El
incremento de la ICa en las células del nodo SA y AV aumenta la pendiente de despolarización de la fase 4 y también hace que el
umbral se vuelva más negativo.
Las catecolaminas no parecen modificar el potencial diastólico máximo. Sin embargo, sí acortan el potencial de acción como
resultado de las acciones que ejercen sobre varias corrientes concretas. Las catecolaminas aumentan la fuerza de la contracción
(efecto inotrópico positivo) en el músculo auricular y ventricular por cuatro motivos. En primer lugar, el aumento de la ICa (es decir,
flujo de entrada de Ca2+) conduce a un aumento local mayor de la [Ca2+]i y también a una mayor liberación de Ca2+ inducida por
Ca2+ desde el RS. En segundo lugar, las catecolaminas aumentan la sensibilidad del canal de liberación de Ca2+ del RS al Ca2+
citoplásmico. En tercer lugar, las catecolaminas también potencian el bombeo de calcio hacia el RS mediante la estimulación de la
bomba de calcio SERCA, incrementando de este modo los depósitos de Ca2+ para una liberación posterior. En cuarto lugar, el
aumento de la ICa presenta más Ca2+ al SERCA, de modo que los depósitos de Ca2+ del RS aumentan con el paso del tiempo. Los
cuatro mecanismos determinan una mayor disponibilidad de Ca2+ para la troponina C, permitiendo una contracción más fuerte.
EL ELECTROCARDIOGRAMA (ECG)
El electrocardiograma es el registro de las variaciones de potencial creadas en el cuerpo por la actividad eléctrica del corazón. la
onda de despolarización debida a la activación secuencial de las cámaras cardíacas genera una diferencia de potencial entre las
zonas activadas y en reposo, lo que induce variaciones en el campo eléctrico que aparecen como ondas en el electrocardiograma. la
morfología y polaridad de estas ondas depende de la secuencia del proceso de activación y de la localización de los electrodos que
las registran.
Los puntos seleccionados para el registro del ECG reciben el nombre de derivaciones. Para obtener un ECG de 12 derivaciones se
colocan dos electrodos en las extremidades superiores, dos en las extremidades inferiores y seis en localizaciones estándar sobre el
tórax. En diferentes combinaciones, los electrodos de los miembros generan las seis derivaciones de los miembros (tres estándar y
tres aumentadas) y los electrodos situados en el pecho generan las seis derivaciones precordiales. En una derivación un electrodo
será el lado positivo de un voltímetro y uno o más electrodos el lado negativo. Por tanto, una derivación registra la fluctuación en la
diferencia de voltaje entre electrodos positivos y negativos. Variando los electrodos que se consideran positivos y negativos se
registrará un ECG de 12 derivaciones. Cada derivación mira al corazón desde un ángulo y un plano únicos; es decir, desde lo que en
esencia es su punto de vista particular.
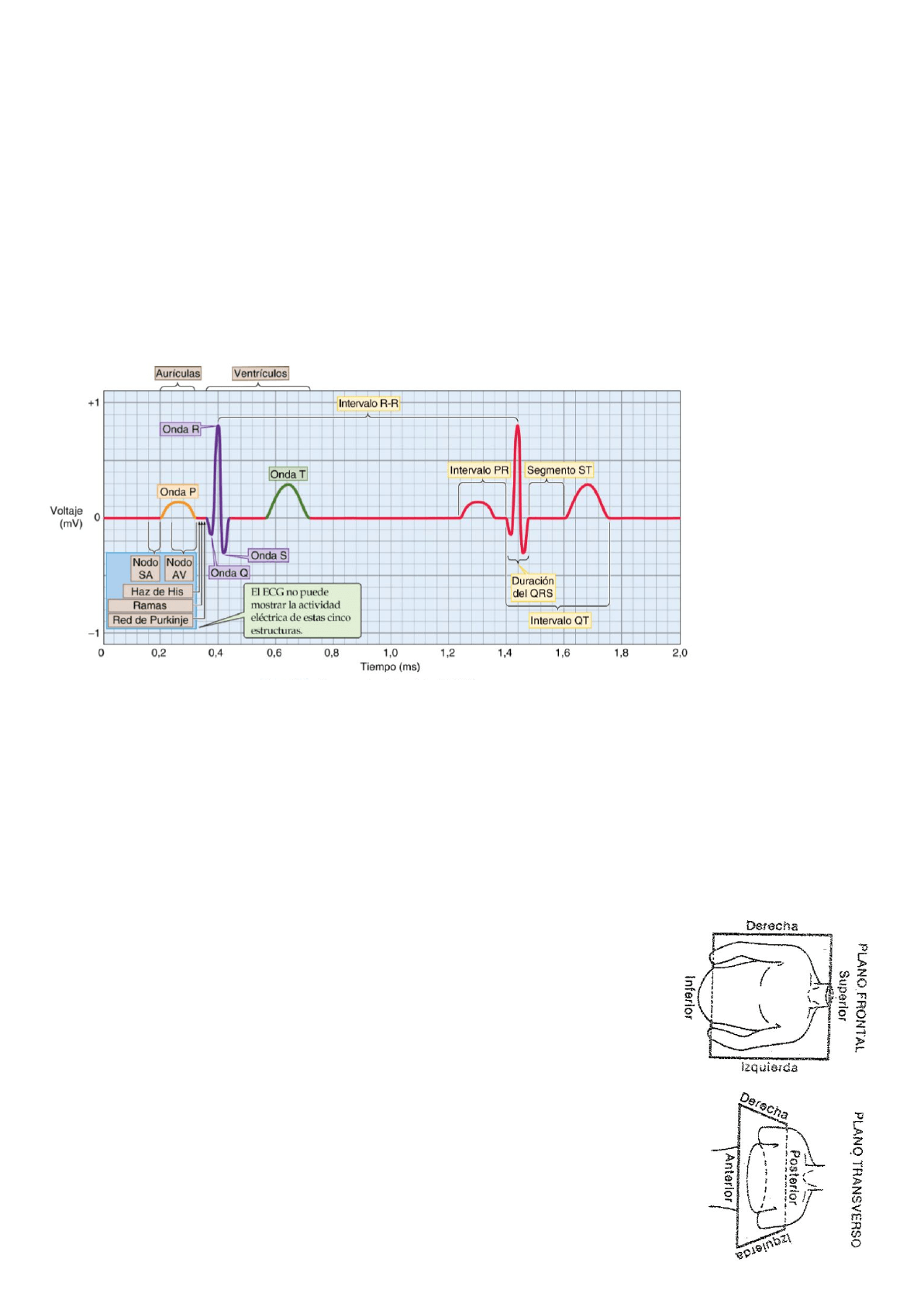
Las fluctuaciones en el voltaje extracelular registrado por cada derivación varían desde fracciones de un milivoltio hasta varios
milivoltios. Estas fluctuaciones se llaman ondas y se las denomina con letras del alfabeto. La onda P refleja la despolarización del
músculo auricular derecho e izquierdo. El complejo QRS representa la despolarización del músculo ventricular. La onda T representa
la repolarización de ambos ventrículos. Finalmente, una onda U, rara vez visible, puede reflejar la repolarización del músculo papilar.
La forma y la magnitud de estas ondas son diferentes en cada derivación, ya que cada una ve la actividad eléctrica del corazón desde
una posición concreta en el espacio.
Como el movimiento de la carga (es decir, la onda de actividad eléctrica que se propaga por el corazón) tiene una dirección y una
magnitud tridimensionales, la señal medida en un ECG es un vector.
Para registrar el vector eléctrico dependiente del tiempo del corazón, el médico o el técnico de ECG construyen un sistema de
derivaciones en dos planos perpendiculares entre sí. El plano frontal se define por las seis derivaciones de los miembros. El plano
transversal perpendicular se define por las seis derivaciones precordiales. Cada derivación es un eje en uno de los dos planos sobre
el cual proyecta el corazón su actividad eléctrica. El registro del ECG desde una sola derivación muestra cómo contempla dicha
derivación los cambios de voltaje del corazón dependientes del tiempo.
-Las derivaciones de los miembros: El ECG de 12 derivaciones se obtiene colocando al paciente relajado en decúbito supino y
conectando cuatro electrodos a las extremidades. Desde el punto de vista eléctrico, el torso y las extremidades se contemplan como
un triángulo equilátero (triángulo de Einthoven) con un vértice en la ingle y los otros dos en las articulaciones de los hombros. Como
el cuerpo es un «conductor de volumen» eléctrico, una conexión eléctrica a un brazo equivale eléctricamente a una conexión en la
articulación del hombro y una conexión en cualquiera de las piernas equivale a una conexión en la ingle. Por convención, la pierna
izquierda representa a la ingle. El cuarto electrodo, conectado a la pierna derecha, se usa como toma de tierra. Las tres derivaciones
de los miembros iniciales representan la diferencia entre dos de los electrodos de las extremidades:
• DI (conexión positiva al brazo izquierdo, conexión negativa al brazo derecho). Esta derivación define un eje en el plano frontal a 0
grados.
• DII (positiva en la pierna izquierda y negativa en brazo derecho). Esta derivación define un eje en el plano frontal a 60 grados.
• DIII (positiva en la pierna izquierda, negativa en el brazo izquierdo). Esta derivación define un eje
en el plano frontal a 120 grados.
Una reconstrucción electrónica de la conexión de las tres extremidades define un punto de
referencia eléctrico en el medio del corazón que constituye la conexión negativa para las
derivaciones de los miembros «unipolares» aumentadas y para las derivaciones del tórax.
Las tres derivaciones de los miembros unipolares comparan un electrodo de una extremidad con
el promedio de las otras dos:
• aVR (conexión positiva en el brazo derecho [right], conexión negativa definida electrónicamente
en el medio del corazón):
el eje definido por esta derivación en el plano frontal es de −150 grados. La a representa
aumentado y la V representa unipolar.
• aVL (conexión positiva en brazo izquierdo [left], conexión negativa en el medio del corazón): el
eje definido por esta derivación en el plano frontal es de −30 grados.
• aVF (conexión positiva en la pierna izquierda [foot], conexión negativa en el medio del corazón):
el eje definido por esta extremidad en el plano frontal es de +90 grados.
Así pues, los extremos positivo y negativo de estas seis derivaciones definen ejes cada 30 grados
en el plano frontal.
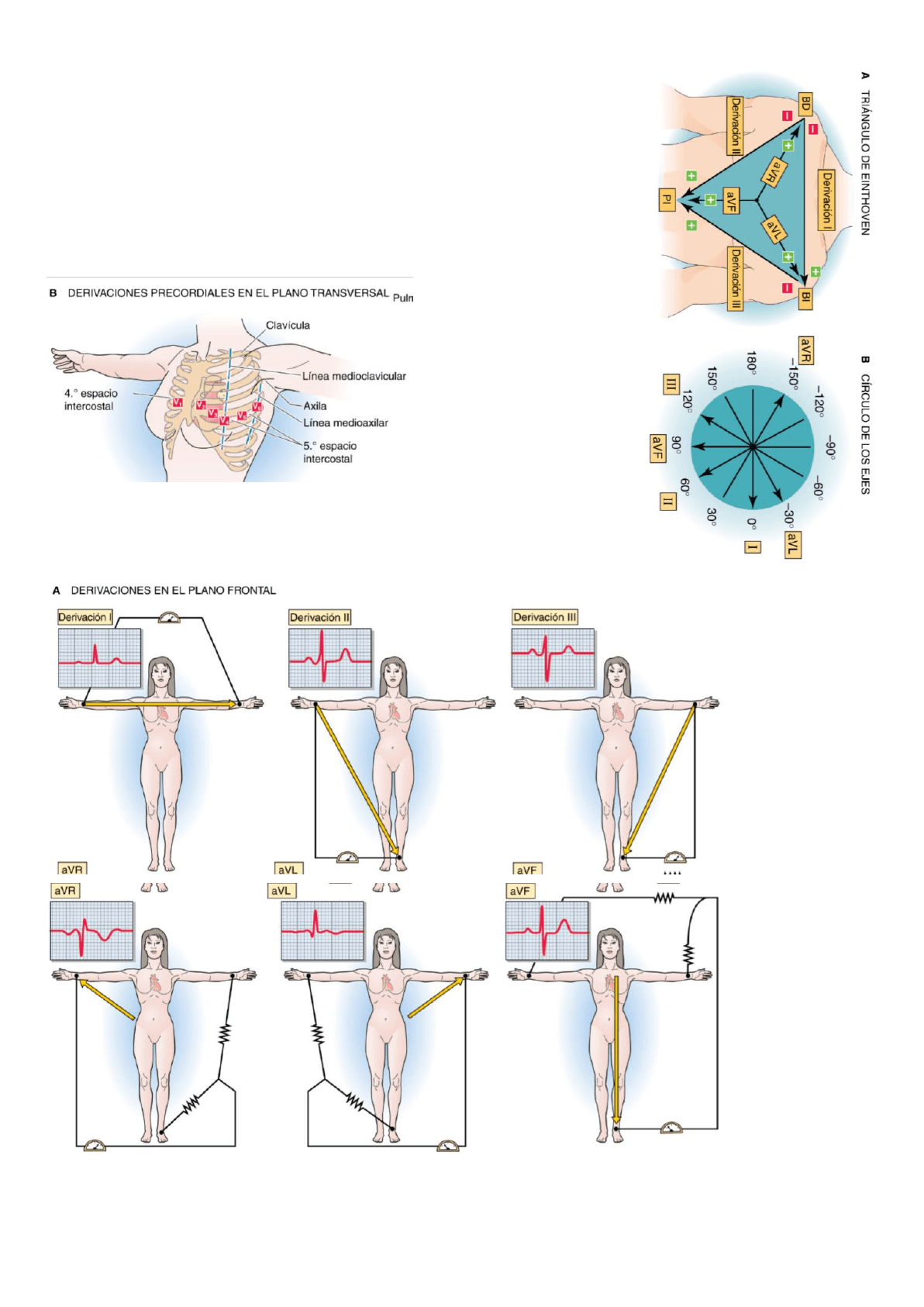
-Las derivaciones precordiales: Las derivaciones precordiales están en el plano transversal,
perpendicular al plano de las derivaciones frontales. La conexión positiva es una de seis
localizaciones diferentes sobre la pared torácica y la conexión negativa está definida
electrónicamente en el medio del corazón por el promedio de las tres derivaciones de los
miembros. Las derivaciones resultantes se denominan V1 a V6, donde V significa unipolar:
• V1: cuarto espacio intercostal a la derecha del esternón.
• V2: cuarto espacio intercostal a la izquierda del esternón.
• V4: quinto espacio intercostal en la línea medioclavicular.
• V3: a mitad de camino entre V2 y V4.
• V6: quinto espacio intercostal en la línea medioaxilar.
• V5: a mitad de camino entre V4 y V6.
Vectores electricos:
En cada derivacion del ECG, la morfologia y la polaridad de sus ondas estan relacionadas con los cambios de la orientacion de los
frentes de excitacion con el corazon. Para analizarlas e imaginar la progresion de todo el proceso de despolarizacion, se representa
un vector que tiene magnitud y direccion, y que se grafica como una flecha con su punta positiva.
La excitación se origina en el nódulo sinusal, y desde allí se propaga hacia abajo y hacia la aurícula izquierda. El frente de onda que
activa las aurículas está representado por un vector con el polo (+) por izquierdo orientado hacia el lado izquierdo del tórax y algo
hacia abajo. El campo generado por este dipolo hara (+) el brazo izquierdo con respecto al derecho y así producir a una onda P
positiva en DI, lo mismo que el DII; pero en DIII, qué es casi perpendicular al eje del dipolo equivalente, la onda P será pequeña,
difasica, o puede estar ausente.
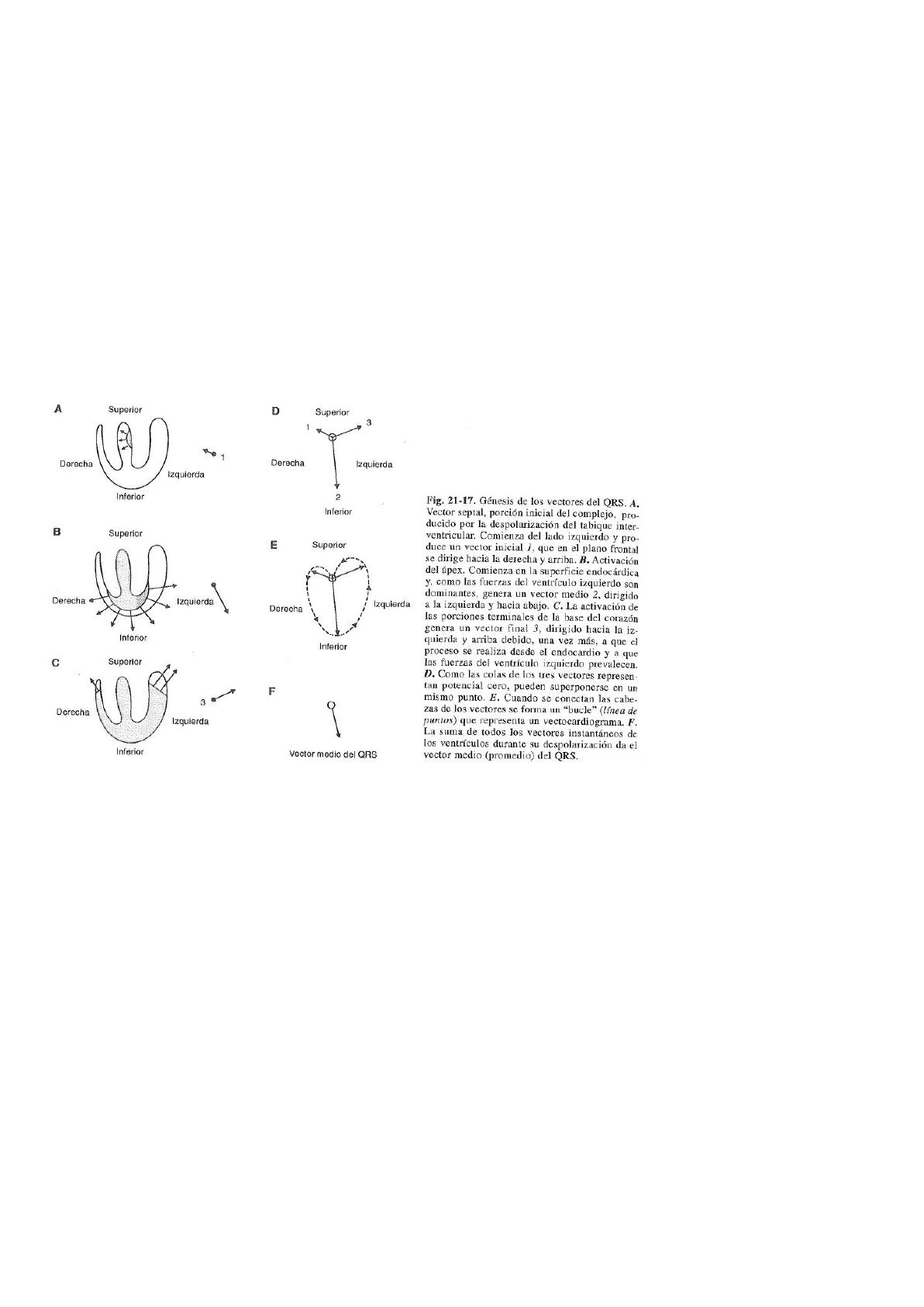
Las primeras fibras ventriculares que son activadas eléctricamente se encuentran en el lado izquierdo de la porción media del
tabique interventricular. A causa de ello, el primer frente de la onda de activación ventricular se dirige a través del músculo septal
de izquierda a derecha. Luego sobreviene una ordenada pero compleja progresión desde las regiones subendocardicas hacia la
subepicárdicas (vector 2) y desde el apex hacia la base (vector 3). Por lo tanto, se podría representar la activación ventricular con 3
vectores: 1, inicial o septal; 2, medio o ventricular; y 3, final o basal. El vector de mayor magnitud es el dos y representa la dirección
general del proceso de activación que estaría orientada hacia la izquierda y abajo, aproximadamente paralela a DII; por ese motivo
el complejo QRS es predominantemente positivo en DII, tambien positivo pero de menor magnitud en DI, y pequeño, positivo o
negativo en DIII.
Eje electrico:
En presencia de un registro electrocardiografico, además de calcular la frecuencia cardíaca, controlar la secuencia, morfología y
duración de sus ondas y observar la presencia o no de alteraciones ritmo, se debe determinar el eje eléctrico. El eje electrico medio
del corazón, en el plano frontal, es el valor del angulo que forma el vector medio del QRS con la linea horizontal (DI).
La utilidad práctica de determinarlo radica en que en individuos normales sus valores reflejan la posición anatómica del corazón, en
concordancia con los hábitos constitucionales del individuo: tipo horizontal en los brevilineos y vertical en los longilineos, con
varias posiciones intermedias. Por otra parte, el eje eléctrico sufre desviaciones en condiciones patológicas.
Uno de los procedimientos para hacer el eje eléctrico medio del corazón, en el plano frontal, consiste en la representación, dentro
de una circunferencia, del triangulo de Einthoven qué contiene las derivaciones bipolares DI, DII y DIII. Se determina el vector para
DI (suma algebraica de las ondas del QRS en esa derivación) y se traslada este valor al lado apropiado del triángulo, respetando la
polaridad convencional. Se repite este procedimiento con cualquiera de las otras dos derivaciones. Se proyectan líneas
perpendiculares desde esas colas de estos componentes hacia el interior del triángulo. Su intersección determinará la posición de la
cabeza y la cola del vector medio del QRS. El ángulo por entre este vector y la horizontal es el valor del eje eléctrico medio del
corazón, que normalmente en el adulto se halla entre 0 y +90°. Cuando el vector encontrado se dirige hacia valores negativos, entre
-10° y -60°, el eje eléctrico está desviado hacia la izquierda, y a la inversa, valores entre +110° y +160° indican una desviacion hacia
la derecha.

ARRITMIAS:
Cualquier cambio en el ritmo cardíaco que se aleje del ritmo sinusal
normal se define como una arritmia. Aunque algunas arritmias son
patológicas, e incluso potencialmente mortales, otras son normales y
convenientemente adaptativas, como la taquicardia sinusal y la arritmia
sinusal.
La taquicardia sinusal es una frecuencia cardíaca más rápida de la
normal impulsada por el nodo sinusal. Esta arritmia se observa en
personas atemorizadas o sobresaltadas, o durante un ejercicio normal.
La arritmia sinusal es la denominación de un fenómeno normal: un
cambio sutil en la frecuencia cardíaca que ocurre con cada ciclo
respiratorio. La inspiración acelera la frecuencia cardíaca mientras que
la espiración la desacelera. Las respiraciones profundas exageran estos
cambios cíclicos. La magnitud del efecto puede variar notablemente de
un individuo a otro. La frecuencia cardíaca sigue bajo el control del
ritmo marcapasos del nodo SA.
Aunque la lista de arritmias patológicas es bastante larga, hay dos
problemas básicos que son responsables de la práctica totalidad de las
arritmias: una alteración de la conducción y una alteración de la
automaticidad.
Cuando se lesiona un tejido (p. ej., por estiramiento o anoxia), el
desequilibrio de las corrientes iónicas puede conducir a una
despolarización. A su vez, esta despolarización inactiva parcialmente a
la INa y a la ICa desacelerando la propagación de la corriente (es decir,
ralentizando la conducción). Como resultado el tejido puede volverse
menos excitable (bloqueo de conducción parcial) o completamente
inexcitable (bloqueo de conducción completo).
Otro tipo de trastorno de la conducción es la presencia de una vía de
conducción aberrante que refleja una anomalía anatómica. Un ejemplo sería la existencia de una vía de conducción accesoria que
transmite rápidamente un potencial de acción desde las aurículas a los ventrículos sorteando el nodo AV, que normalmente impone
un cierto retraso a la conducción.
Algunos ejemplos de arritmias:
● Extrasistoles o latidos ectopicos: son producidos por excitacion del automatismo o reentrada
● fibrilacion ventricular: es la arritmia mas grave. se produce por una activacion asincronica de las fibras ventriculares, lo cual
convierte la actividad electrica en caotica, pudiendo producir la muerte.
● bradicardias: arritmia caracterizada por disminucion de la frecuencia cardiaca. Generalmente causada por estimulacion
vagal.
● Síndrome de QT largo Los pacientes con síndrome de QT largo (SQTL) tienen un potencial de acción ventricular prolongado
y son propensos a desarrollar arritmias ventriculares. En concreto, son susceptibles de desarrollar una forma de taquicardia
ventricular conocida como torsade de pointes, en la cual los complejos QRS cambian constantemente sus ejes y su amplitud
alrededor de una línea de base. El SQTL puede ser congénito o adquirido. La forma congénita puede implicar mutaciones de
los canales de Na+ cardíacoso de K+. La forma adquirida del SQTL, mucho más frecuente, puede deberse a diversos
trastornos electrolíticos (especialmente hipopotasemia e hipocalcemia) o por medicación prescrita o de libre disposición (p.
ej., varios antiarrítmicos, antidepresivos tricíclicos y algunos antihistamínicos no sedantes cuando se toman juntamente con
ciertos antibióticos, y en especial con la eritromicina).

fisio gastro intestinal.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.