
Enzimas
Las enzimas son catalizadores biológicos
En los seres vivos ocurren reacciones químicas, síntesis o rupturas de enlace, transporte
de sustancias, etc., con notable velocidad y eficiencia.
Los catalizadores aceleran una reacción química sin formar parte de los productos finales
ni desgastarse en el proceso.
En las condiciones presentes en los sistemas biológicos (temperatura alrededor de 37º en
homeotermos, pH más o menos neutro, presión constante) la mayoría de las reacciones
bioquímicas ocurrirían muy lentamente o NO se producirían.
En los medios biológicos existen catalizadores llamadas ENZIMAS, quienes disminuyen la
Energía de activación (Ea) sobre sustratos.
Las ENZIMAS muestran gran especificidad
aún entre isómeros ópticos; poseen un sitio
activo, lugar donde se une al sustrato.
Las ENZIMAS:
1- Luego de la reacción, se recuperan sin alteraciones. No forman parte de los productos
finales.
2- Permiten que se produzcan reacciones que en condiciones normales transcurrirían a
velocidades muy bajas.
3- Aceleran las reacciones químicas en forma reversible.
1
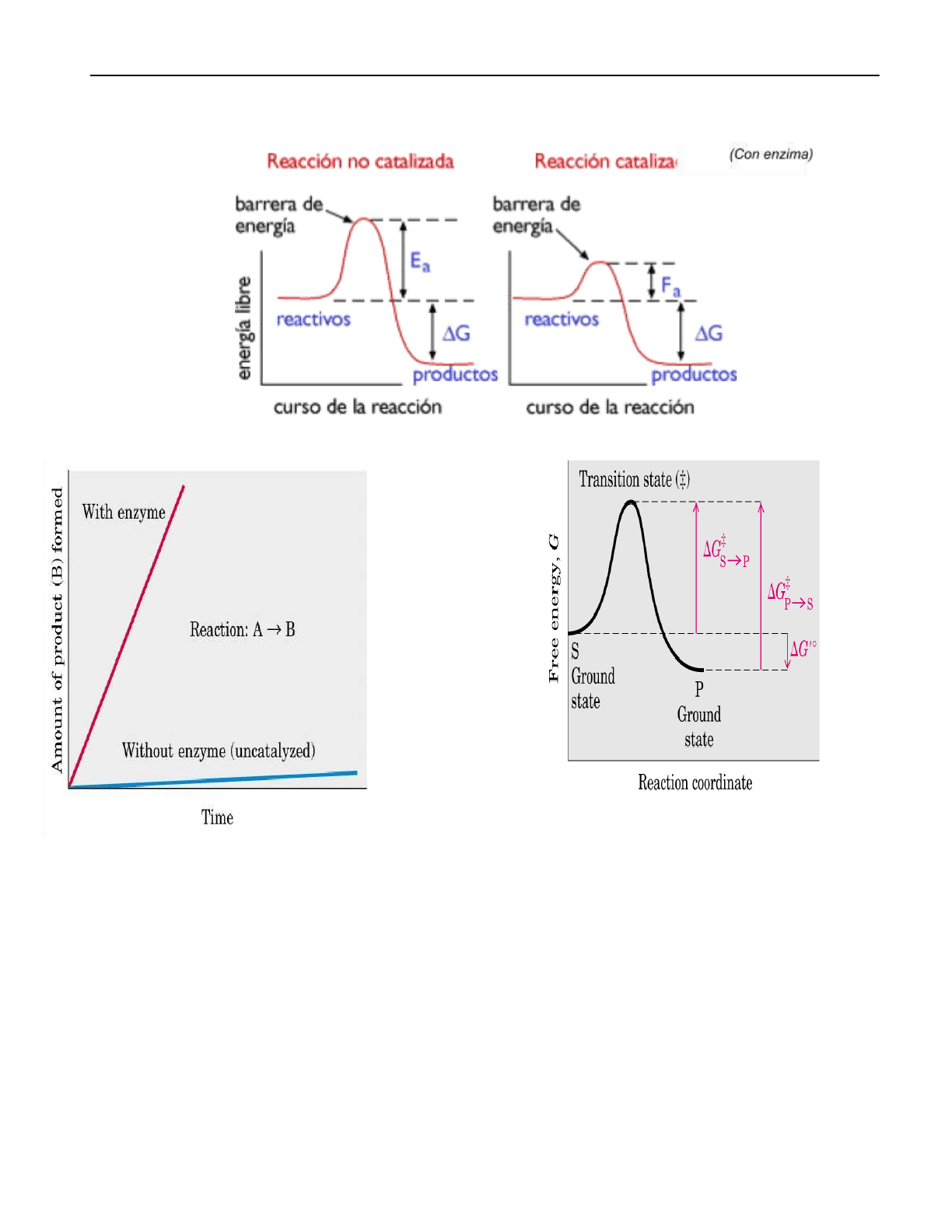
Gráficamente:
El Delta G en esta reacción primero es positivo, y luego negativo.
Es una reacción coordinada en la cual el producto de la primera reacción es sustrato de la segunda
(reacciones acopladas). Y disminuye la energía de activación.
Las enzimas pueden nombrarse de diferentes formas…
A)Agregando el sufijo “asa” al sustrato sobre el que actúan: ureasa, amilasa, tirosinasa, etc.
B)Con nombres particulares: pepsina, tripsina, etc.
C)Llevan el nombre según la reacción que catalizan: deshidrogenasa, descarboxilasas, etc.
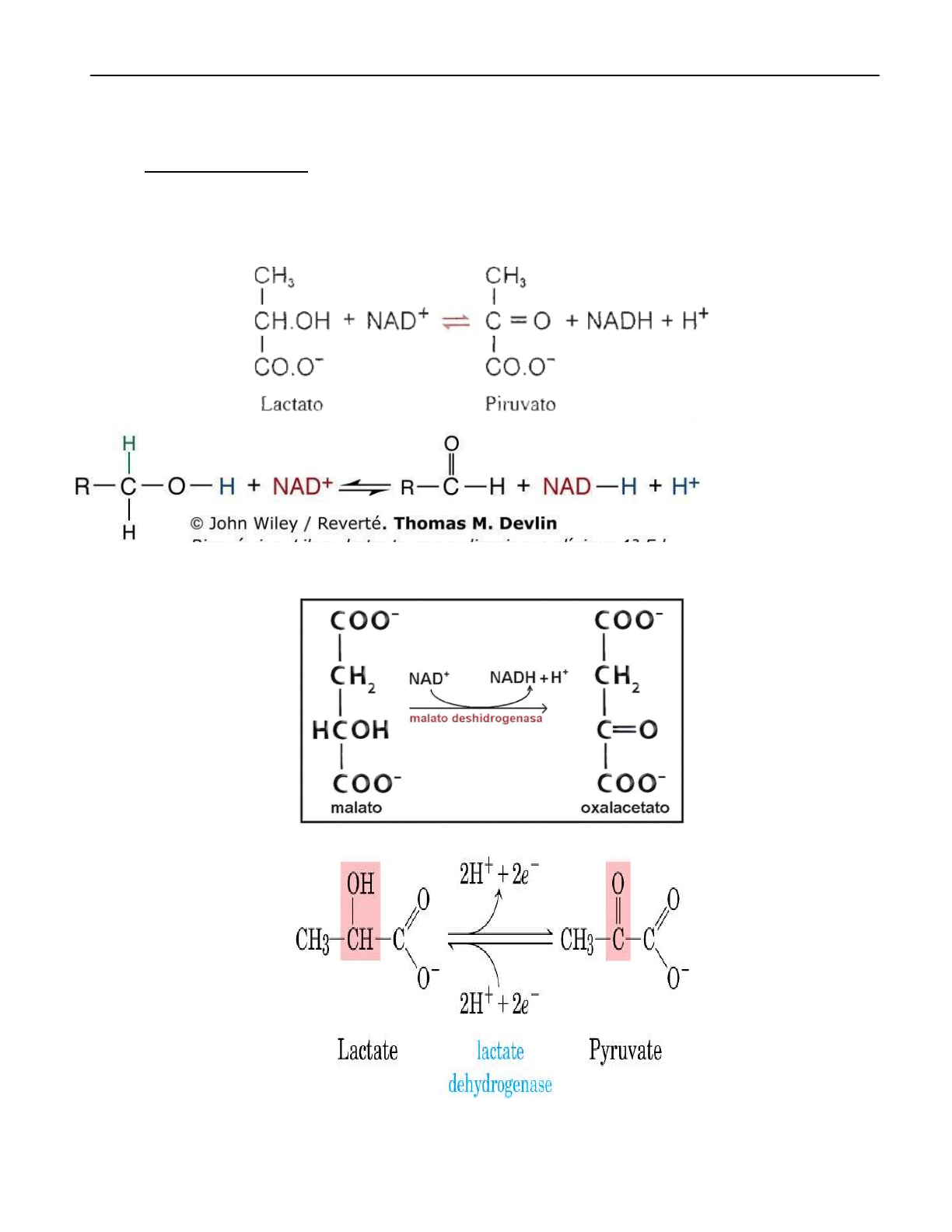
Teniendo en cuenta la reacción que catalizan y de acuerdo a la IUB:
1- Oxidoreductasas: Catalizan reacciones de óxido-reducción.
Ejemplo: la Lactato deshidrogenasa o L-Lactato-NAD Oxido-reductasa, cataliza la
oxidación del Lactato a Piruvato y la reacción inversa, utilizando como coenzima NAD.
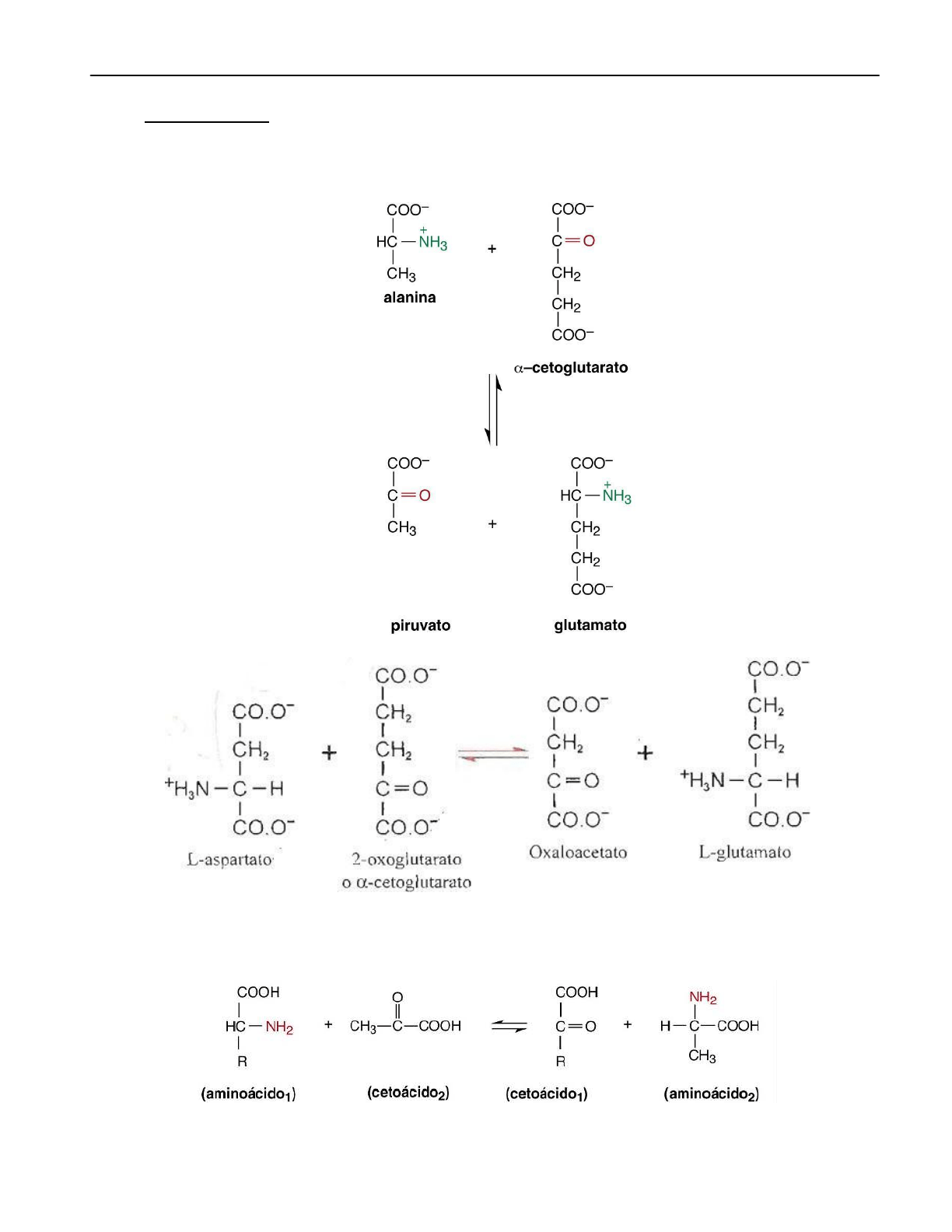
2- Transferasas: Catalizan las transferencia de un grupo de átomos (amina,
carboxilo, metilo, etc.)
Ejemplo: las Aminotransferasas o Transaminasas que transfieren grupos aminos, las
Aciltransferasas que utilizan grupos acilos.
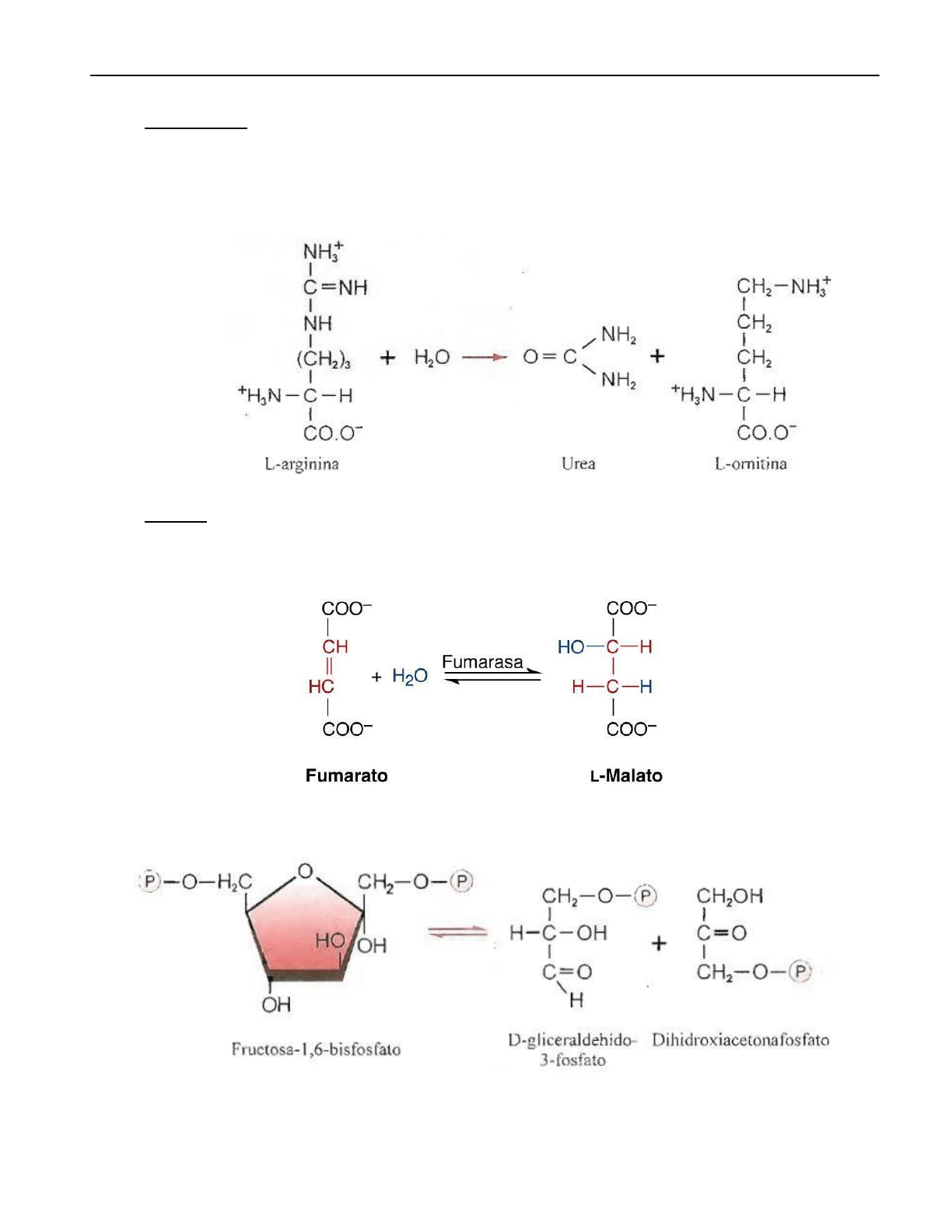
3- Hidrolasas: Catalizan la ruptura de enlaces C-O, C-N, C-S, O-P por adición de
agua.
Ejemplo: Aceticolinesterasa y la Ribonucleasa hidrolizan la unión éster entre y colina de
la Acetilcolina y las uniones entre nucleótidos en el ARN respectivamente. Otra es la
Arginasa que cataliza la hidrólisis de la Arginina para formar urea.
4- Liasas: Catalizan la ruptura de uniones C-C, C-S y C-N (excluyendo uniones
peptídicas) por un proceso diferente a la hidrólisis.
Ejemplo: la Aldolasa que escinde a la Fructosa 1,6 difosfato en dos triosas fosfatos.
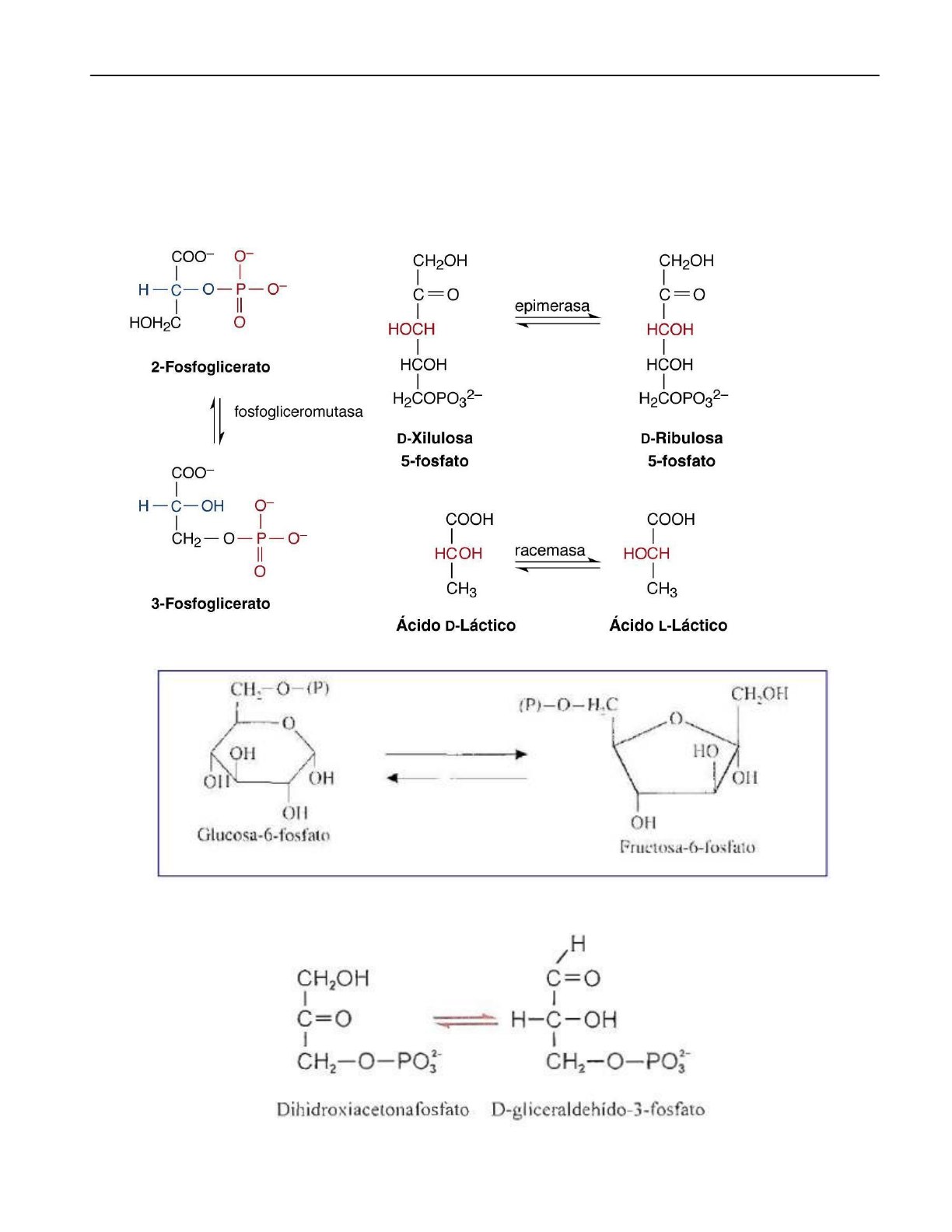
5-Isomerasas: interconvierten isómeros de cualquier tipo: ópticos, geométricos y de posición.
Cuando la reacción es entre isómeros de posición son MUTASAS, si se trata de otros
isómeros, ISOMERASAS.
Ejemplo:
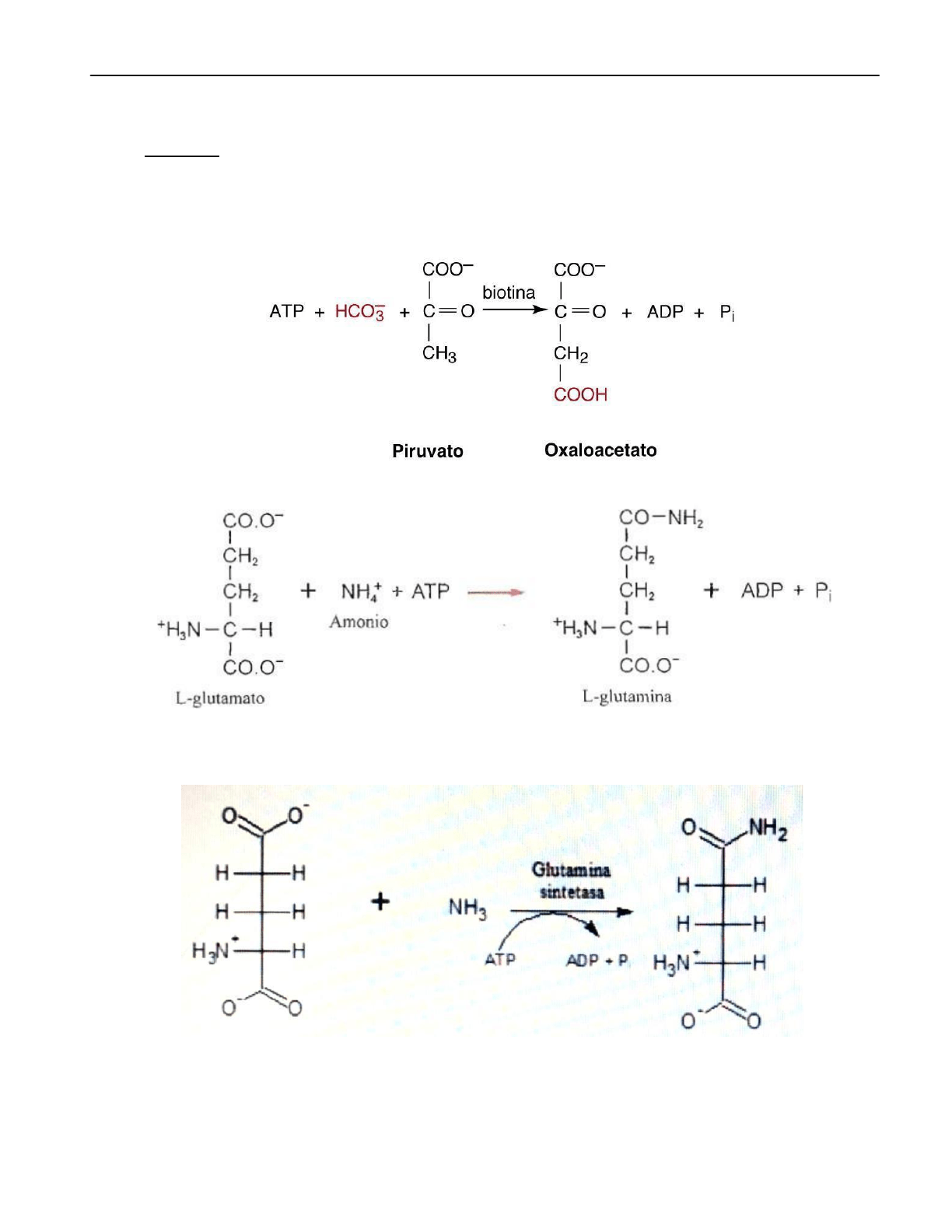
6- Ligasas, sintetasas o cintazas: catalizan la unión de moléculas acoplada con la
hidrólisis de un enlace de alta energía. . En gral, siempre que tenga ATP será ligasa,
quien provee la energía necesaria para la síntesis.
Ejemplo: la glutamina sintetasa actúa en la reacción entre el ácido glutámico y amoníaco
para formar glutamina
Naturaleza química de las enzimas…
Las enzimas son de naturaleza proteica, algunas son proteínas simples como las

hidrolasas, otras son asociaciones de subunidades o cadenas polipeptídicas; son
oligoméricas.
Hay enzimas que sólo pueden realizar su función catalítica asociándose con otras
moléculas no proteicas, las COENZIMAS, que pueden estar unidas a las enzimas por
enlace covalente u otro tipo de enlace, quien representa el “GRUPO PROSTÉTICO”.
Las oxido-reductasas (1), transferasas (2), isomerasas (5) y ligasas (6) requieren la
participación de coenzimas.
Las coenzimas intervienen en la reacción experimentando cambios que compensan las
transformaciones del sustrato.
Ejemplo: las oxido-reductasas actúan aceptando o cediendo protones o electrones del
sustrato. Algunas poseen estructura de tipo nucleotídica y por otra parte están relacionadas
con las vitaminas, sobre todo con las del complejo B.
El sistema completo se llama holoenzima y está constituido por la parte proteica
apoenzima y la coenzima.
APOENZIMA
COENZIMA
Naturaleza proteica
Naturaleza no proteica
Termolábil
Termoestable
Macromolécula
Experimenta cambios luego de la
reacción
No dializable
Dializable
Marcada especificidad por el
sustrato
No poseen afinidad por el sustrato
HOLOENZIMA = APOENZIMA + COENZIMA
(Enzima total) (Proteína) (Parte no proteica)
La parte proteica o apoenzima es la parte que le da especificidad a la holoenzima.
La apoenzima unida a la coenzima le da actividad a la holoenzima.
Una coenzima puede unirse a diferentes apoenzimas y actuar frente a diferentes sustratos.
Metaloenzimas…

Son enzimas en las que la presencia de iones metálicos en la molécula es indispensable
para su acción catalítica, de esta manera mantiene las estructuras terciaria y
cuaternaria. Si pierde el componente metálico pierde su actividad.
Ejemplos. Contienen…
• Fe: Catalasas, peroxidasas, hemoproteínas.
• Cu: tirosinasa, citocromo oxidasa.
• Zn: anhidrasa carbónica
• Mo: Xantino oxidasa.
• Mg: enzimas que usan ATP.
• Mn: Acetil-CoA carboxilasa y desoxiribonucleasa.
• CI
-
: amilasa.
Iones metálicos como el Ca
2+
, el Na
+
y el K + son necesarios para la actividad de
algunas enzimas.
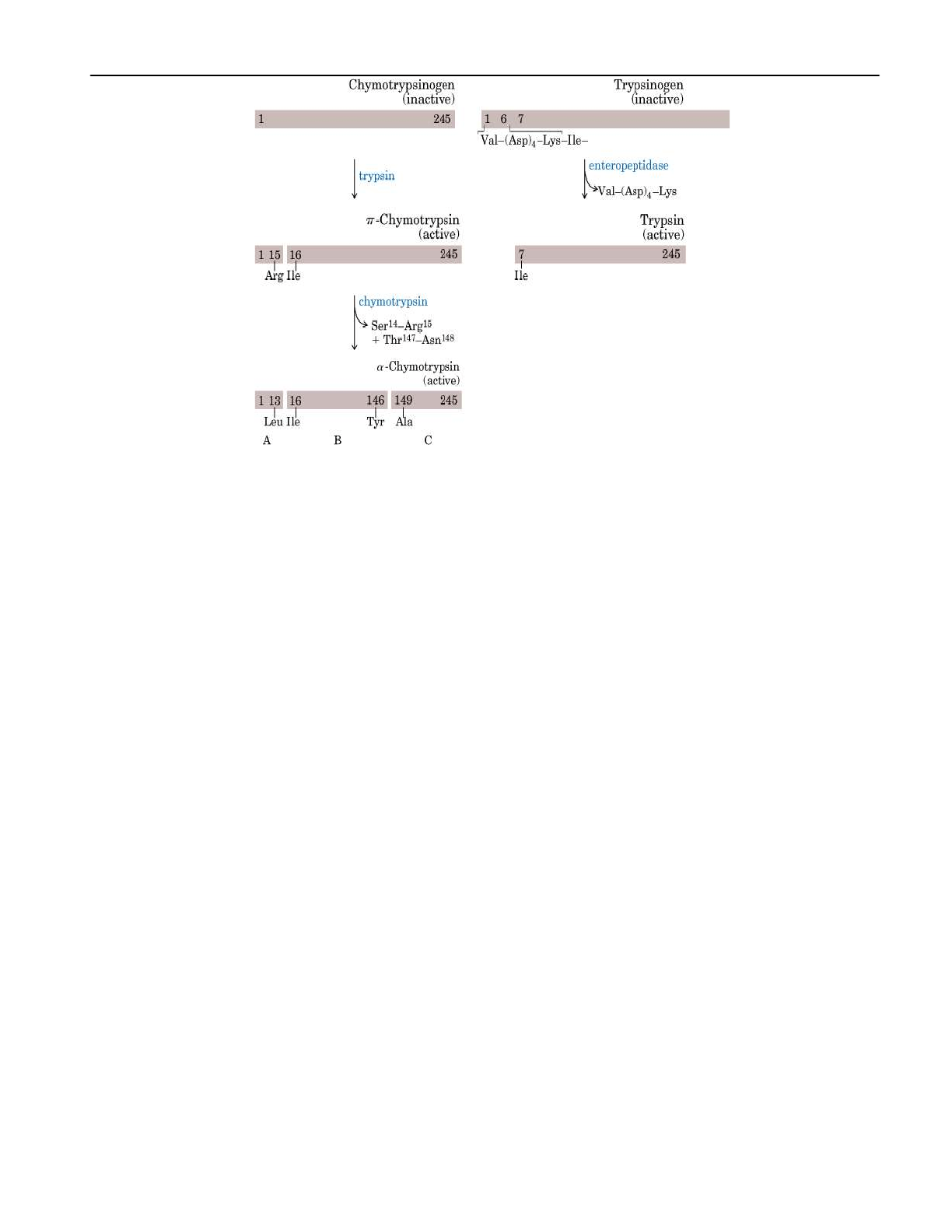
Zimógenos, proenzima o preenzimas …
Son precursores inactivos de una enzima.
Son proteínas simples que se convierten en enzimas activas por hidrólisis. Otra enzima
produce la ruptura del sitio catalítico de la cadena polipeptídica del zimógeno, lo cual permite
que la molécula reacomode su sitio activo y adquiera actividad catalítica. O también por
aumento del HCl (disminuye pH).
Se sintetizan como zimógenos porque si se sintetizara en su forma activa destruiría la célula.
Ej.:
ZIMÓGENO
ENZIMA
Pepsinógeno
Pepsina
Tripsinógeno
Tripsina
Sistemas o Complejos multienzimáticos…
Conjunto de enzimas diferentes y ordenadas, que poseen acciones complementarias.
El producto de la reacción catalizada por la primera enzima es sustrato de la segunda, y
así sucesivamente.
Ejemplo: Cadena respiratoria.
Isoenzimas o isozimas o formas moleculares múltiples…
Son proteínas diferentes con igual actividad enzimática.
Ejemplo la LDH que presenta cinco isozimas que se las enumera del 1 al 5, según la
movilidad electroforética, siendo diferente la distribución relativa de las mismas según el
tejido.
En diafragma se encuentran las cinco, en corazón predomina 1 y 2. En hígado y músculo
voluntario es frecuente encontrar la 5.
Ejemplo
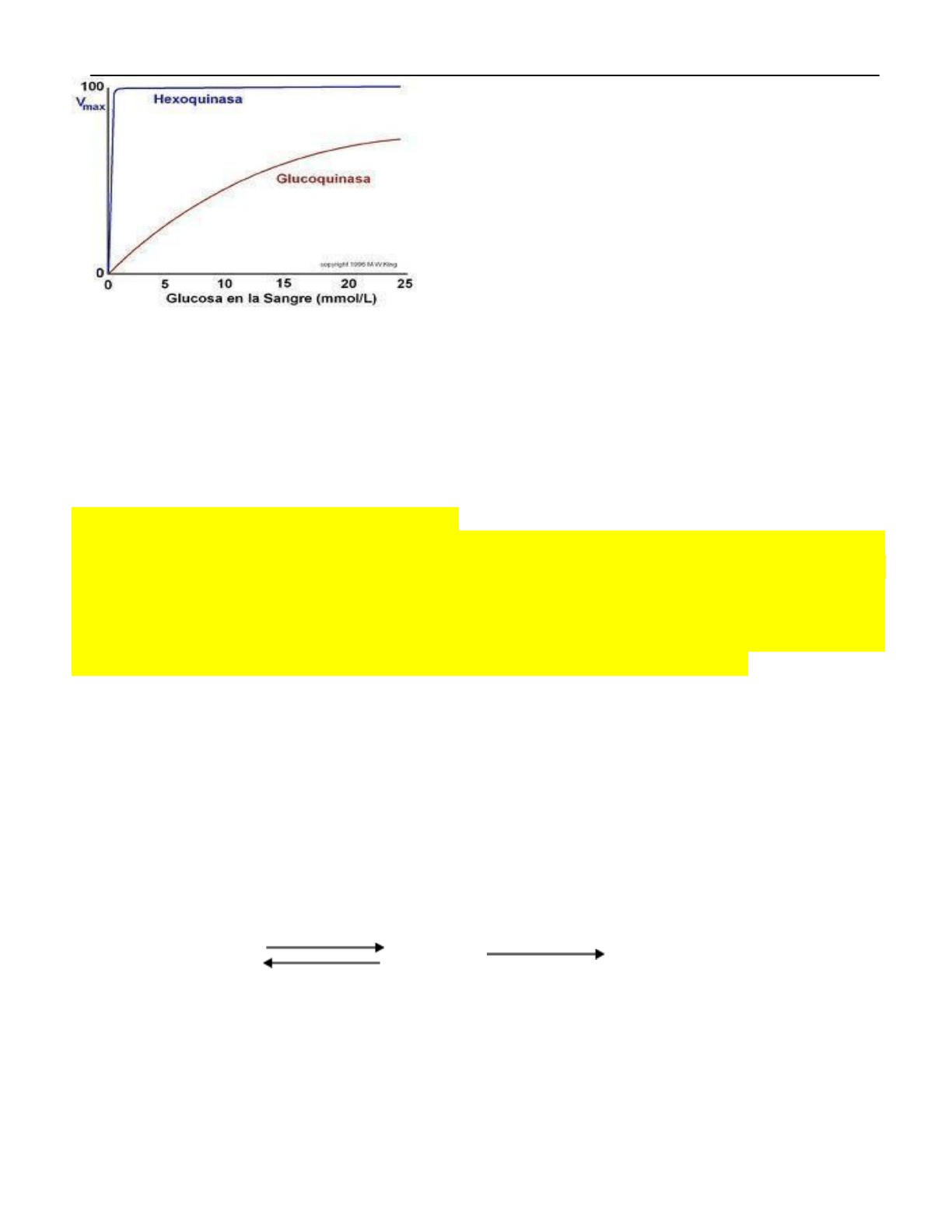
HEXOQUINASA: Tiene baja la Km.
Fosforila la glucosa, si ya hay mucha
glucosa fosforilada, es inhibida por G6P.
GLUCOQUINASA: en hígado y páncreas.
No se inhibe
Distribución intracelular de las enzimas:
Hay enzimas que son sintetizadas en ciertas células y luego “exportadas” hacia el lugar en
el cual han de cumplir su misión. Las enzimas de los jugos digestivos y las que participan
en la coagulación de la sangre son extracelulares. La enorme mayoría de las enzimas son
intracelulares, las que no están distribuidas al azar, así por ejemplo las enzimas que
participan en la glucólisis se encuentran en el citoplasma, las que intervienen en el ciclo
de Krebs lo hacen en las mitocondrias, las hidrolasas en los lisosomas, etc.
Catálisis enzimática
Es el proceso mediante el cual se acelera la velocidad de la reacción
disminuyendo la Ea. Durante la reacción, la enzima se une al o a los sustratos,
transitoriamente (enlaces no covalentes), y luego se disocia en enzima y
producto.
Al finalizar la reacción, la enzima aparece sin cambios y puede unirse a otra
molécula de sustrato. Muy pequeñas cantidades de enzima pueden acelerar
enormemente la velocidad de la reacción.
E + S (E-S) E + P
(Enzima) (Sustrato) (Complejo Enzima - Sustrato) (Enzima) (Producto)
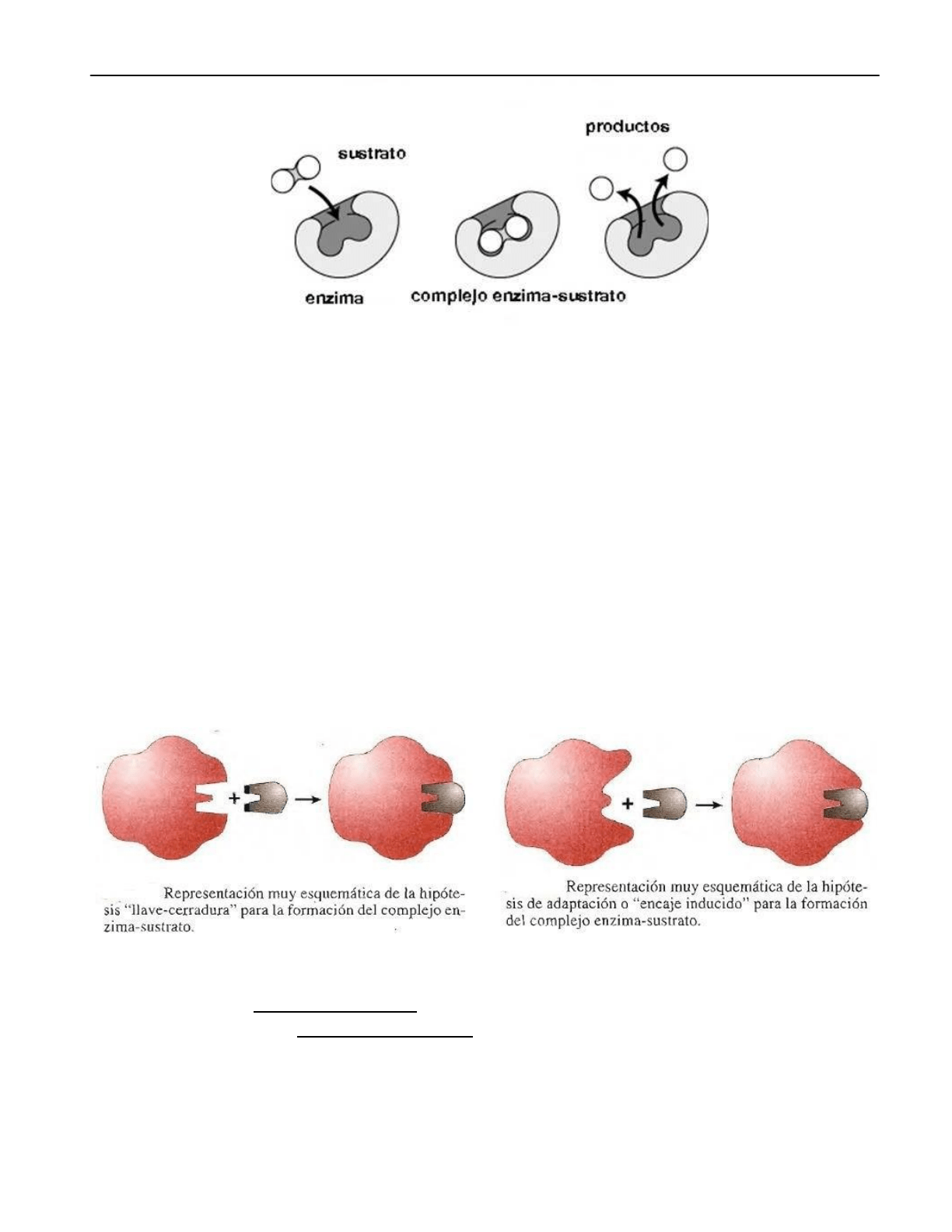
Sitio activo
Es el lugar de la enzima donde se fija el sustrato y se cumple la acción catalítica.
Es una agrupación de aminoácidos ordenados, distribuidos espacialmente de manera
precisa.
La “coenzima” participa en asegurar la conformación óptima, se une a la enzima,
generalmente próximo al sitio activo y a veces forma parte del lugar del sustrato.
Fischler a fines del siglo XIX propuso el MODELO LLAVE-CERRADURA: la estructura del
sustrato y la del sitio activo son complementarias, de la misma forma que una llave encaja
en una cerradura.
Actualmente se acepta la hipótesis de Koshland (MODELO AJUSTE INDUCIDO): la
enzima tiene una estructura flexible. Cuando el sustrato se une a la enzima induce
cambios conformacionales en ésta, que reacomoda sus aa para formar el complejo E-S.
¿Cómo determinamos la actividad enzimática?
La actividad de las enzimas puede determinarse midiendo:
A- la cantidad de producto formado, en un tiempo determinado.
B- la concentración de sustrato consumido, en un tiempo determinado.
UNIDAD INTERNACIONAL (UI): UI es la cantidad de enzima que cataliza la transformación
de 1
µmol (micromol) de sustrato por minuto bajo condiciones definidas de pH, T, etc.
Condiciones que se logran fuera de un organismo.
¿Cuáles son los factores que modifican la actividad enzimática?
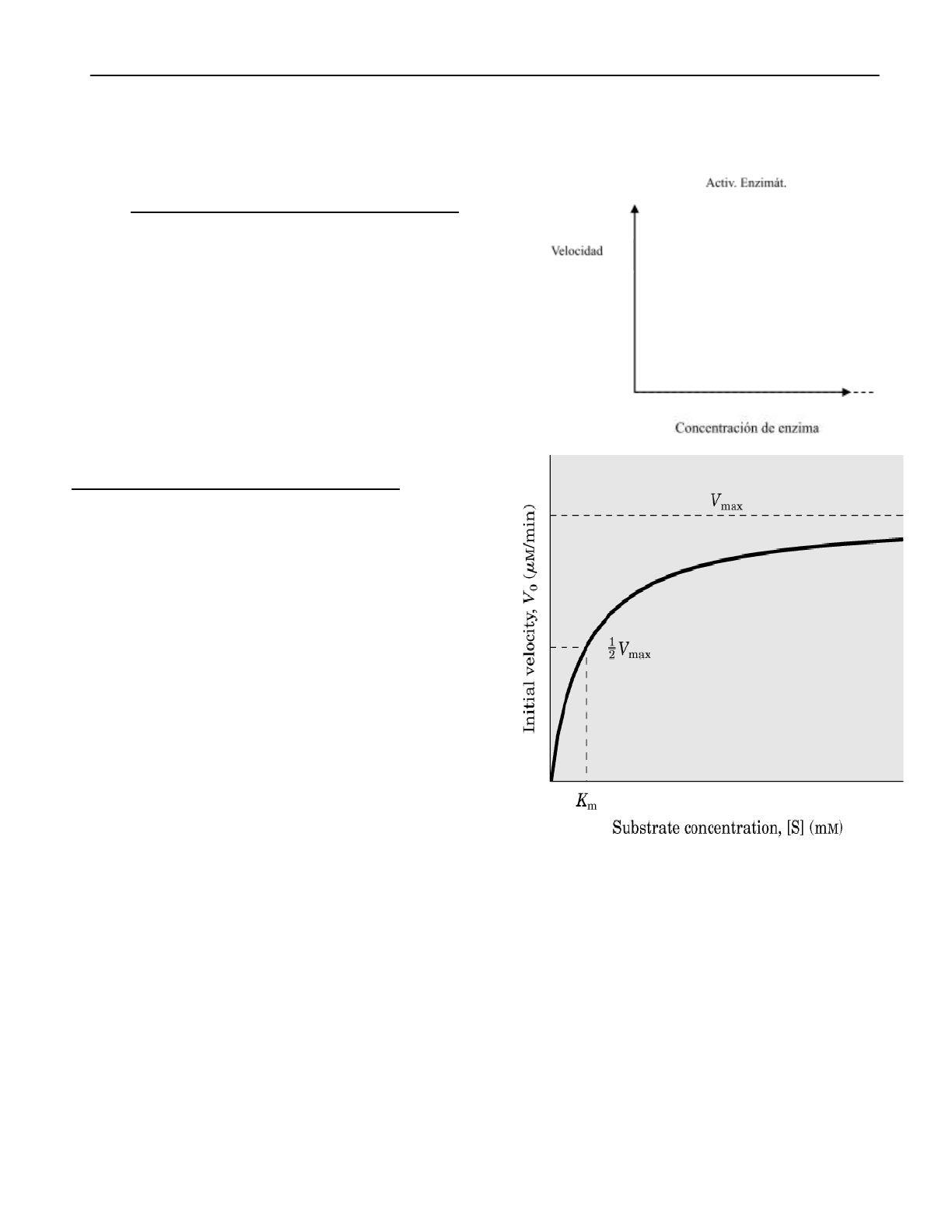
CONCENTRACIÓN DE LA ENZIMA
La velocidad de una reacción catalizada por
una enzima es directamente proporcional a la
concentración de la enzima.
La velocidad de la reacción se indica en el eje
de las ordenadas vs. la concentración de la
enzima.
CONCENTRACIÓN DE SUSTRATO
Si solo varía la (S) se obtendrá una hipérbola.
La concentración de sustrato varía;
al comienzo el aumento de la velocidad es
proporcional al aumento de
[S] por incremento
de la formación del complejo E-S.
A alta
[S] toda la enzima está saturada de
sustrato, y por más que aumente la [S] no
se formarán más complejo E-S, se alcanza
la “velocidad máxima” (Vmáx) de la
reacción.
“constante de Michaelis”: Km: [S] con la cual la velocidad de la reacción alcanza la mitad
de la velocidad máxima. NO es la mitad de la velocidad máxima.
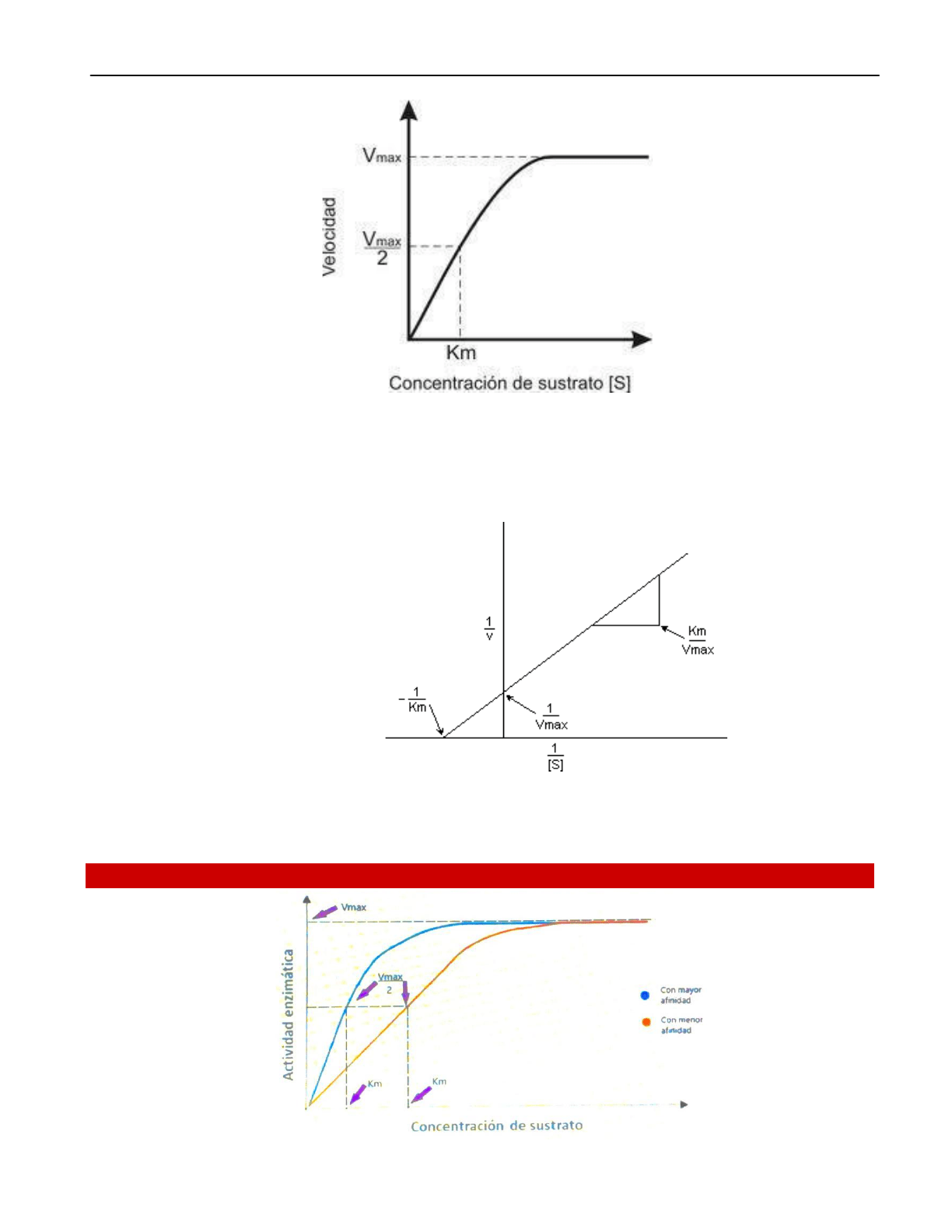
Este Km guarda una relación inversa con la afinidad de la enzima y el sustrato.
A mayor afinidad menor Km, a pH y T constante.
El Km nos da una idea de la afinidad y tiene un valor fijo para cada enzima.
Actividad de dos enzimas:
a) Una con gran afinidad por el sustrato
b) Otra con baja afinidad por el sustrato
Marque Vmáx y Km, señale las diferencias y explique las conclusiones obtenidas.
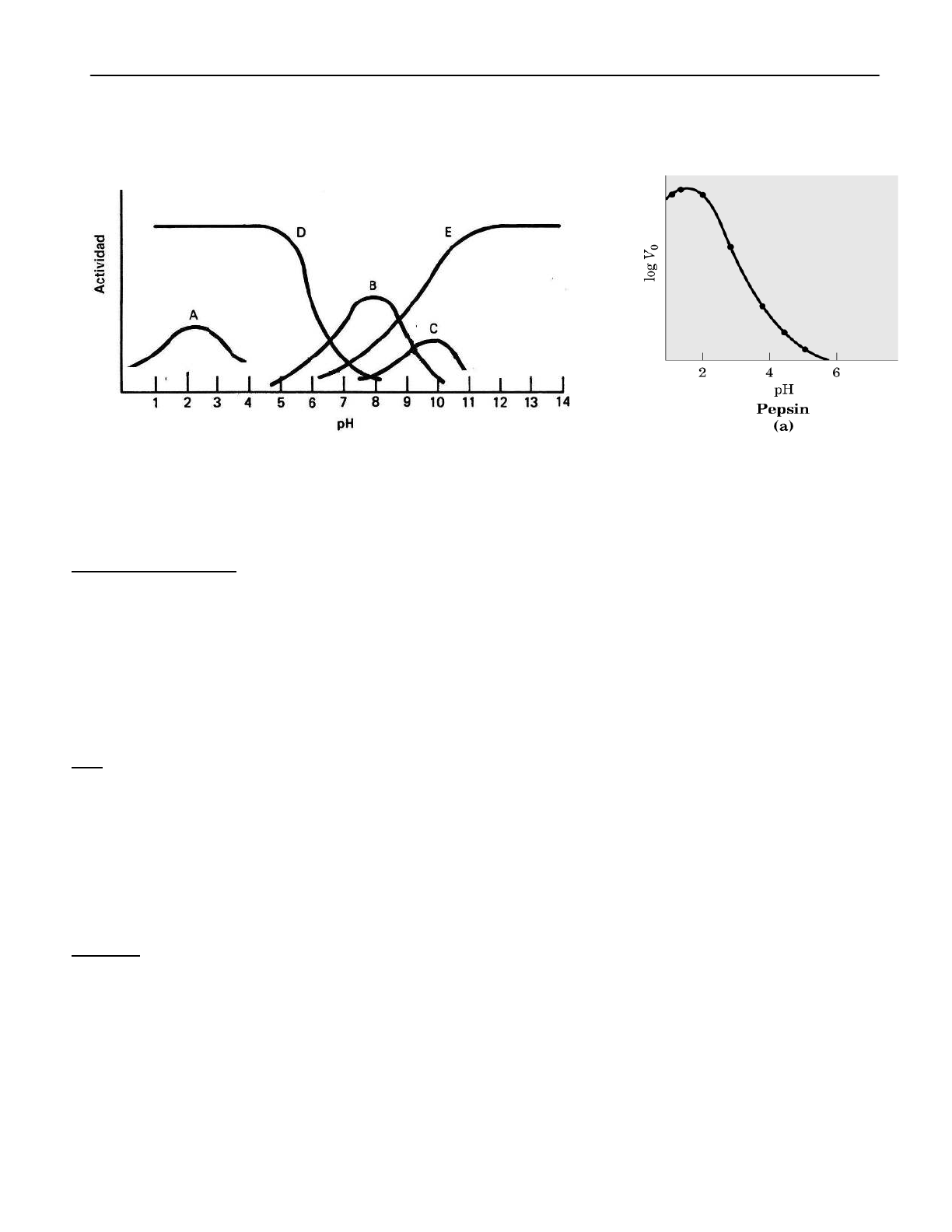
15)- Identifique cuál curva corresponde a la PEPSINA y cuál a la FOSFATASA
ALCALINA. JSR.
A = Pepsina
C = Fosfatasa alcalina
TEMPERATURA:
Las enzimas son proteínas, luego de los 37ºC comienzan a inactivarse por
desnaturalización hasta llegar a los 60º-70ºC en que son inactivadas completamente.
La actividad enzimática aumenta al incrementar la temperatura pero se llega a un valor
máximo que corresponde a la “Temperatura óptima”, por encima de esa temperatura la
actividad cae rápidamente.
pH
Para la mayoría de las enzimas el pH óptimo es de 6-8, sin embargo algunas enzimas
como la pepsina tiene un pH óptimo de 1-2, la tripsina de 8-8,5, la fosfatasa ácida de 5,
fosfatasa alcalina 9,5, etc.
El pH óptimo es aquel en el cual ciertos grupos esenciales poseen carga apropiada para
asegurar la formación del complejo E-S.
IONES:
Hay algunos iones que actúan como activadores o modificadores positivos o como
inhibidores o modificadores negativos.
Hay enzimas que requieren iones en el medio para actuar, como por ejemplo las enzimas
que transfieren restos fosfatos, necesitan Mg
++
, la amilasa, Cl
-
; y otras que requieren Na
+
,
K
+
, Ca
++
, Mn
++
.
Los metales que actúan como inhibidores lo hacen uniéndose al sitio activo de la enzima y
Este documento contiene más páginas...
Descargar Completo
6 Enzimas.docx.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.