
Daiana Soto
METABOLISMO DE BASES NITROGENADAS
DIGESTION Y ABSORCIÓN DE ACIDOS NUCLEICOS
Absorción:
Ribonucleasas y desoxirribonucleasas.
Nucleasas.
Nucleosidasas.
Fosfatasas.
Transporte:
Nucleósidos.
Bases nitrogenadas.
Pentosas.
La absorción de un ácido nucleico ocurre gracias a las enzimas que provienen del jugo
pancreático como las ribonucleasas y desoxirribonucleasas y por enzimas del borde en cepillo
como las nucleasas, nucleosidasas, fosfatasas.
Las ribonucleasas y las desoxirribonucleasas son las que actúan a nivel del ARN y ADN
respectivamente, cumplen la función de romper las uniones fosfodiéster haciendo que los ácidos
nucleicos se conviertan en nucleótidos. Las nucleasas tienen una acción similar a estas, ya que
también actúan sobre cualquier tipo de unión fosfodiéster generando nucleótidos. Las fosfatasas
son enzimas inespecíficas, lo que hacen es retirara grupos fosfatos, por lo que cuando el
nucleótido pierde un grupo fosfato este se convierte en un nucleósido. Las nucleosidasas lo que
hacen es romper la unión glucosídica que mantienen unida a la azúcar con la base nitrogenada de
esos nucleósidos.
A nivel de transporte, la mayor parte de los nucleósidos originados las nucleasas ya sea del jugo
pancreático o del borde en cepillo, van a ser absorbidos como tal sino también si actúa una
nucleosidasas se van a absorber bases nitrogenadas y pentosas. Las pentosas como son un azúcar
de 5 carbonos pasan por difusión pasiva al tracto gastrointestinal hacia la sangre.
También puede ocurrir que los nucleósidos y las bases nitrogenadas absorbidas por la
nucleosidasas puedan ser atacadas por las bacterias de la flora intestinal y también hay
posibilidad de que en el mismo intestino las bases nitrogenadas se conviertan en ácido úrico y
sean eliminado del organismo.
METABOLISMO DE PURINAS Y PIRIMIDINAS
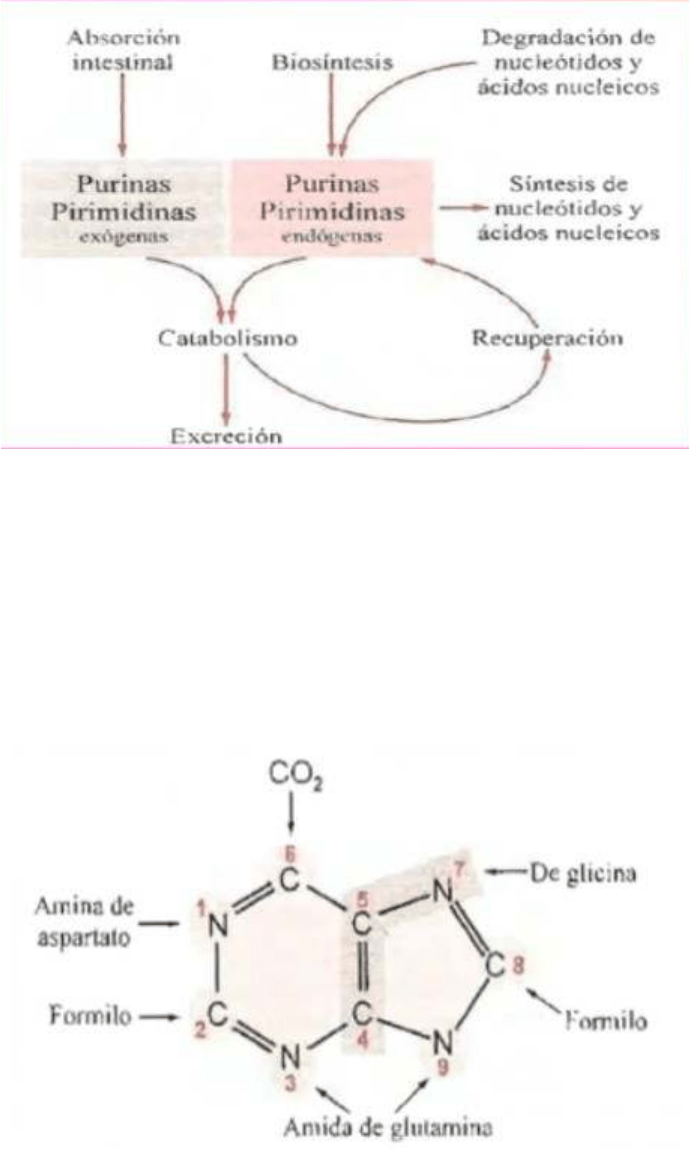
Existe un pool de purinas y pirimidinas que son de origen exógeno y endógeno, las exógenas
provienen de la absorción intestinal mientras que las endógenas provienen de la biosíntesis o de
la degradación de ácidos nucleicos y nucleótidos.
Daiana Soto
Al pool de purinas y pirimidinas se lo puede:
Catabolizar para su posterior excreción.
Se lo puede reutilizar para la síntesis de nuevos nucleótidos y ácidos nucleicos
Y se los puede utilizar en la vía de recuperación o reciclaje.
BIOSINTESIS DE LAS PURINAS
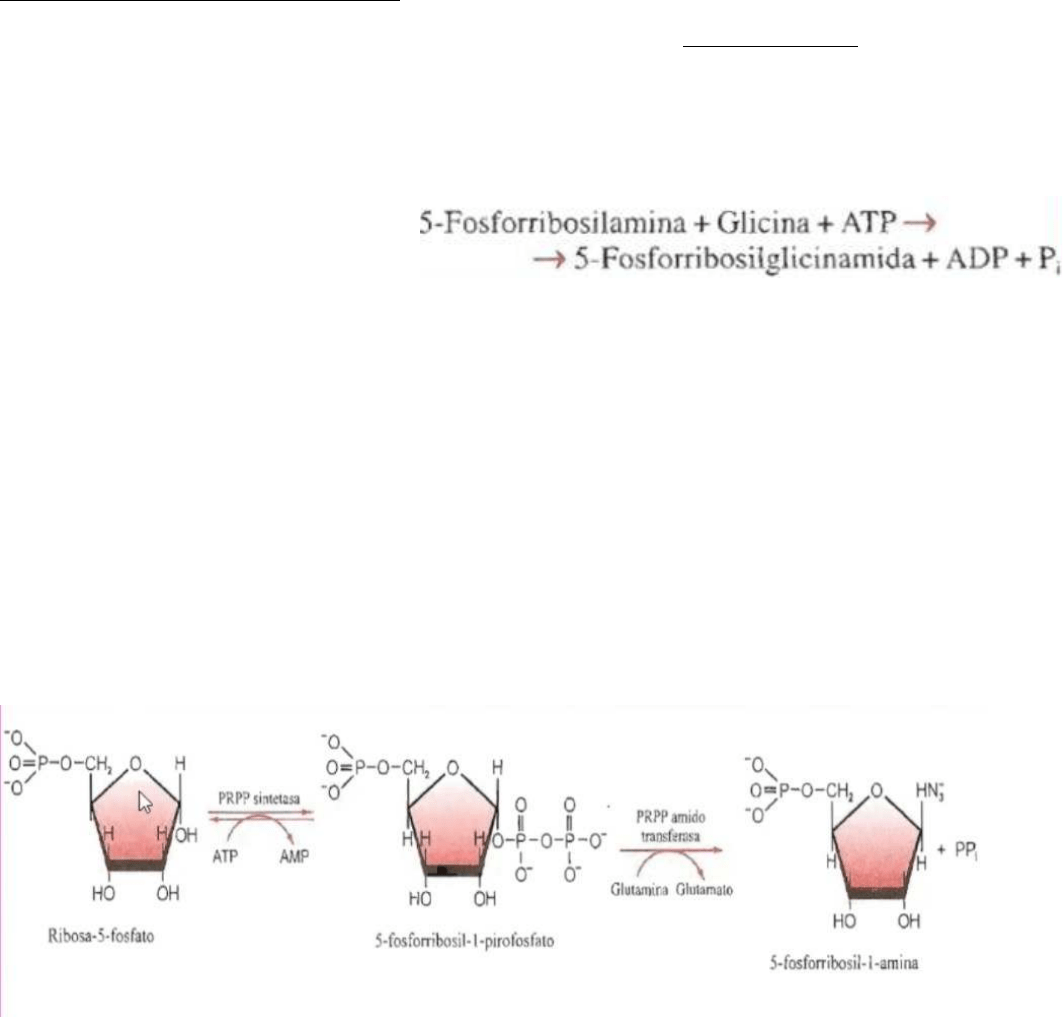
El anillo de las purinas está formado por 2 anillos, uno grande y otro chico. Cada uno de los H y
C presentes en el anillo provienen de una determinada molécula que actúa como donante de esos
C y H, por lo tanto, son las moléculas precursoras a partir de las cuales se sintetizan las purinas.
Por ejemplo, el N numero 1 lo dona el aminoácido aspartato gracias a su grupo amino; el C 2 y 8
aportado por el formilo; el C 3y 9 lo aporta el aa glutamina; el C 6 lo provee el CO2 y el C7 es
aportado por la glicina.
Daiana Soto
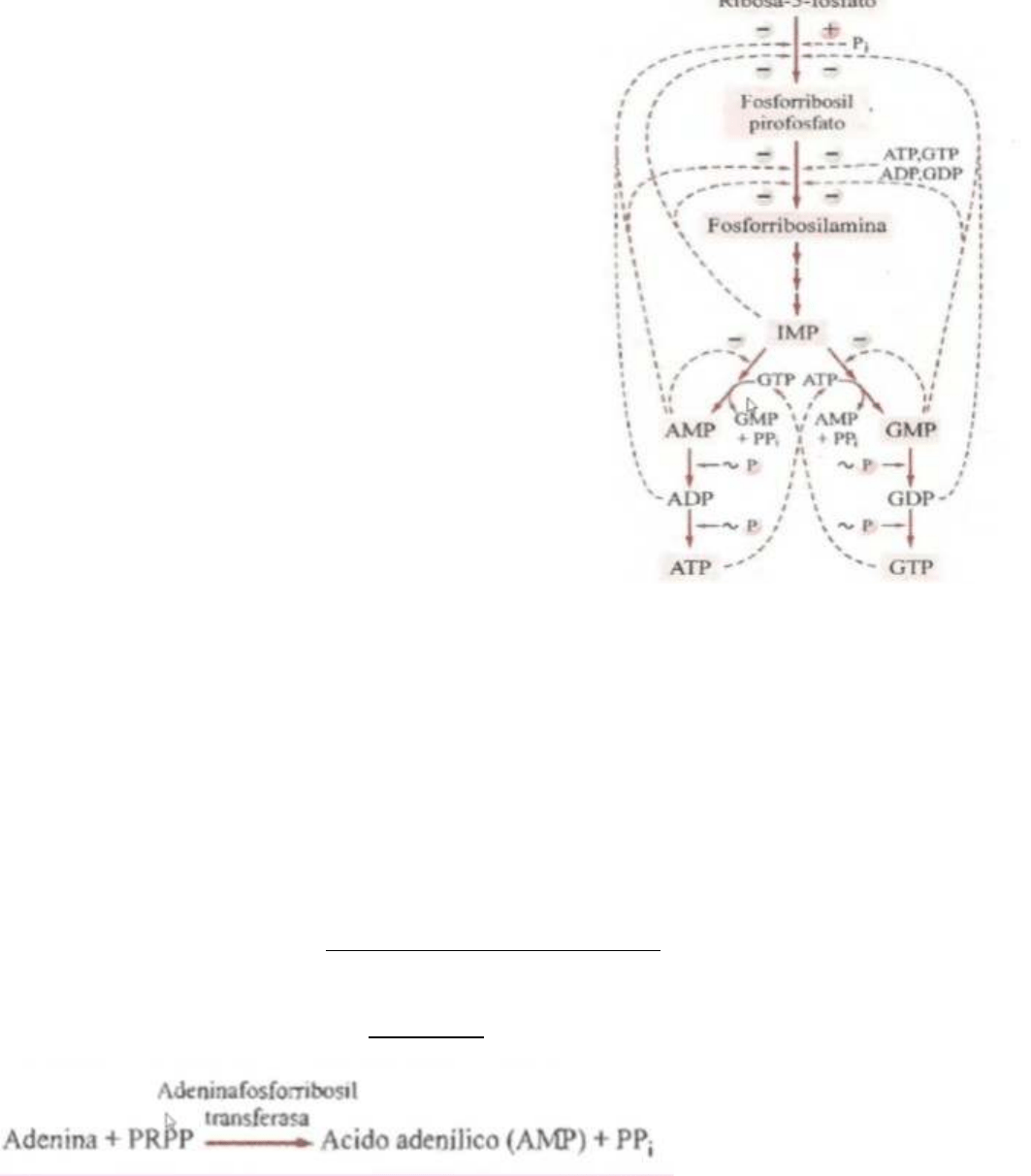
La síntesis de las purinas comienza con transformación de la ribosa-5-fosfato en 5-fosforribosil-
1-pirofosfato y luego a 5-fosforribosil-1-amina.
La ribosa-5-fosfato se obtenía de la vía de las pentosas que es la vía paralela al glucolisis. En esta
vía se producía el NADP + H y ribosa-5-fosfato.
La ribosa-5-fosfato en presencia de ATP que se hidroliza a AMP adquiere 2 grupos fosfatos
transformándose en el 5-fosforribosil-pirofosfato. Es una reacción reversible en donde actúa la
enzima fosforribosil pirofosfato sintetasa.
Una vez formado el 5-fosforribosil-pirofosfato sobre el actúa una amido transferasa que se
encarga de usar a la glutamina para que esta transfiera su grupo amino transformándose en
glutamato. Para eso los 2 fosfatos unidos al carbono 1 se van como pirofosfato inorgánico y a ese
carbono se le une el grupo amina. Como se forma PPi la reacción es irreversible.
Una vez formada la 5-fosforribosil-amina sobre ella va a actuar la glicina (aa donante) por acción
de la enzima fosforribocilglicinamida
sintetasa y además se tiene ATP que se
hidroliza a AMP y Pi, formando así la 5-
fosforribosilglicinamida.
La glicina incorporada en esta reacción aporta los carbonos 4 y 5 y el nitrógeno 7 de la purina.
Los restantes átomos se agregan en etapas sucesivas hasta formar un nucleótido, ya que la ribosa-
5-fosfato permanece unida al N 9 durante todo el proceso. Se obtiene ácido inosínico o inosina
monofosfato (IMP), cuya base nitrogenada es hipoxantina. El carbono 6 de la hipoxantina de
IMP es aminado por transferencia del grupo a-amina de aspartato para formar AMP; la hidrólisis
de un enlace fosfato de GTP provee la energía necesaria.
En otra vía alternativa, la hipoxantina de IMP es oxidada a xantina y posteriormente aminada en
carbono 2 por transferencia del grupo amida de glutamina; se obtiene ácido guanílico o
guanosina monofosfato (GMP). La hidrólisis de ATP a AMP y PPi suministra la energía para la
transferencia del grupo -NH2
Daiana Soto
REGULACIÓN DE LA BIOSINTESIS DE PURINAS
Los pasos principales de regulación están en las primeras dos
etapas, es decir cuando la ribosa-5-fosfato se convierte en
fosforribosil pirofosfato y cuando este se convierte en
fosforribosilamina.
La PRPP sintetasa es activada por fosfato e inhibida por
nucleótidos de purina y pirimidina, lo cual constituye un
ejemplo de control por retroalimentación.
En la primera etapa es inhibida por los nucleótidos obtenidos
actúa como una retroalimentación negativa, pero es activada
por el fosfato inorgánico; lo mismo ocurre con el siguiente
paso en donde la enzima que participa es inhibida por los
productos finales que son los nucleótidos, pero también
existe un control negativo por parte del GMP y el AMP
sobre la enzima que transforma IMP en AMP y el IMP en
GMP.
VIA DE RECUPERACIÓN DE LAS PURINAS
En este mecanismo lo que sucede es la reutilizacion de aquellas bases nitrogenadas ya formadas,
o sea, bases nitrogenadas obtenidas por la degradacion de algun nucleotido o porque son bases
nitrogenadas que se incorporaron con la dieta.
Suponiendo que ya se tiene a la adenina como base nitrogenada preformada la cual va a
interactuar con la fosforribosilpirofosfato formando ácido adenilico (AMP) y PPi. Los dos
grupos fosfatos que están unidos al C1 del fosforribosilpirofosfato se van ocupando ese lugar la
adenina. Participa la enzima adeninafosforribosil transferasa. Otra forma es que el
fosforribosilpirofosfato interaccione con las purinas hipoxantina y guanina convirtiéndose en
ácido inosinico (IMP) el cual luego puede convertirse en AMP y GMP, y el ácido guanilico
(GMP) y PPi. Estas dos reacciones son irreversibles debido que se genera PPI.

Daiana Soto
El fosforribosilpirofosfato, que es la molécula que se produce al principio de la síntesis de las
purinas a partir de la ribosa-5-P, es una molécula clave para la síntesis de las purinas ya que se
utiliza tanto en la biosíntesis novo de las purinas y en la vía de recuperación de estas. También
puede ser utilizado en la síntesis de las pirimidinas.
CATABOLISMO DE LAS PURINAS
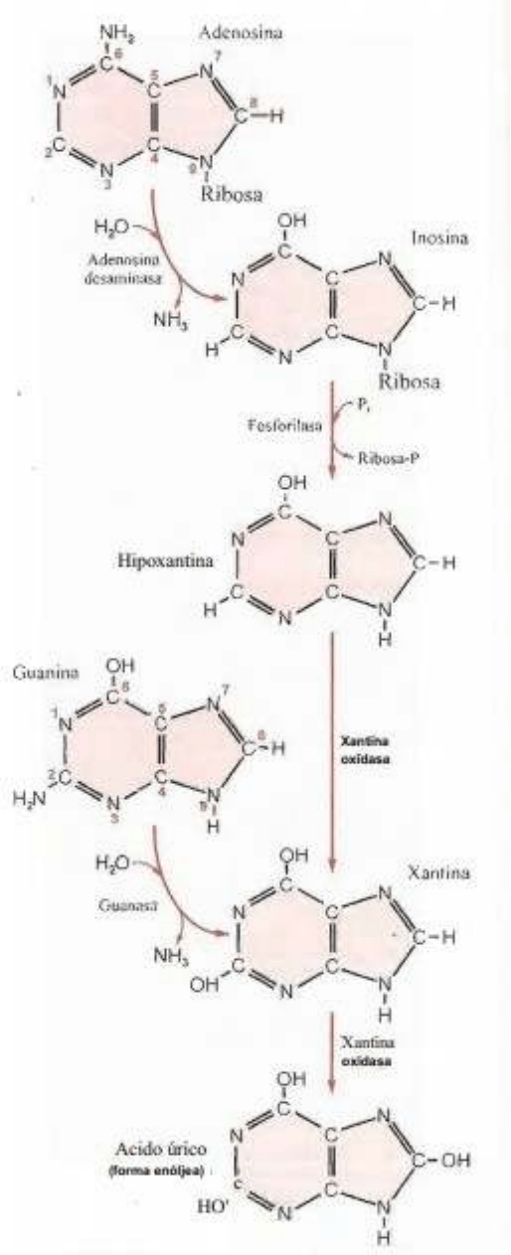
La adenosina va a sufrir la acción de una adenosina desaminasa, la cual hace que el grupo amino
del anillo más grande sea remplazado por un grupo OH con participación de H2O. El grupo
amino se va como NH3 donde se junta el NH2 y el H del agua. Con el amoniaco genera se puedo
eliminar como tal en sales de amonio por orina o puede ser utilizado para la síntesis de la urea.
La adenosina se convierte en la inosina, la cual va a perder la ribosa por acción de una
fosforilasa obteniendo la base nitrogenada hipoxantina, la misma es atacada por xantina oxidasa
que la convierte en xantina, mediante la transformación del H del anillo mas grande en un OH.
Si sobre la xantina vuelve a accionar la xantina oxidasa se genera en cambio del H del anillo más
chico por un OH, haciendo que se produzca el ácido úrico que es una molécula que existe en
forma de urato (disociada) o ácido úrico (no disociada).
También la guanina inicia su catabolismo por desaminación hidrolítica catalizada por guanasa;
se produce xantina. Es decir, las vías catabólicas de adenina y guanina convergen en la
formación de un intermediario común, la xantina.
Generalmente nuestro organismo genera ml por día de ácido úrico de los cuales el 80% es
eliminado por orina mientras que el 20% es eliminado como CO2 y NH3 o urea.
En el OH del ácido úrico tiene un Pka de 5,75 por lo cual a ph fisiológico de la sangre 7,4 la
mayor parte se encuentra en su forma desprotonado llamada urato, sin embargo, si el ph fuera
igual que el pka existiría 50% de su forma desprotonado y 50% en su forma no desprotonado, en
cambio si el ph fuera más acido existiría en su forma de ácido úrico.
Existe una patología en la cual hay aumento de ácido úrico en sangre denominado hiperuricemia,
7mg) y en orina (uricosuria). La enfermedad se denomina gota y generalmente es genética
denominándose gota primaria o también se puede producir a consecuencia de una enfermedad de
base como una diabetes denominándose gota secundaria. Normalmente esa hiperuricemia se
manifiesta sobre todo porque los pacientes sienten un dolor intenso en todas sus articulaciones,
debido a que el exceso de ácido úrico se acumula en las articulaciones haciendo que estas se
inflamen. Si el origen es genético o a consecuencia de una enfermedad básicamente hay una gran
a acumulación de ácido úrico y eso puede ser debido a fallas en alguna enzimas en particular, ya
que si hay más cantidad de ácido úrico es porque hay más cantidad de síntesis de purinas, por lo
que puede ser una falla en las síntesis de alguna proteína destinada a la síntesis de purinas que
Daiana Soto
termina haciendo que se genere más ácido úrico; o
también puede está dado en la enzima xantina
oxidasa que lleva a la producción de ácido úrico.
Es por esto que una de las medicaciones más
utilizada para la gota es alopurinol el cual tiene una
similar estructura al ácido úrico y actúa como
inhibidor de la xantina oxidasa.
Daiana Soto
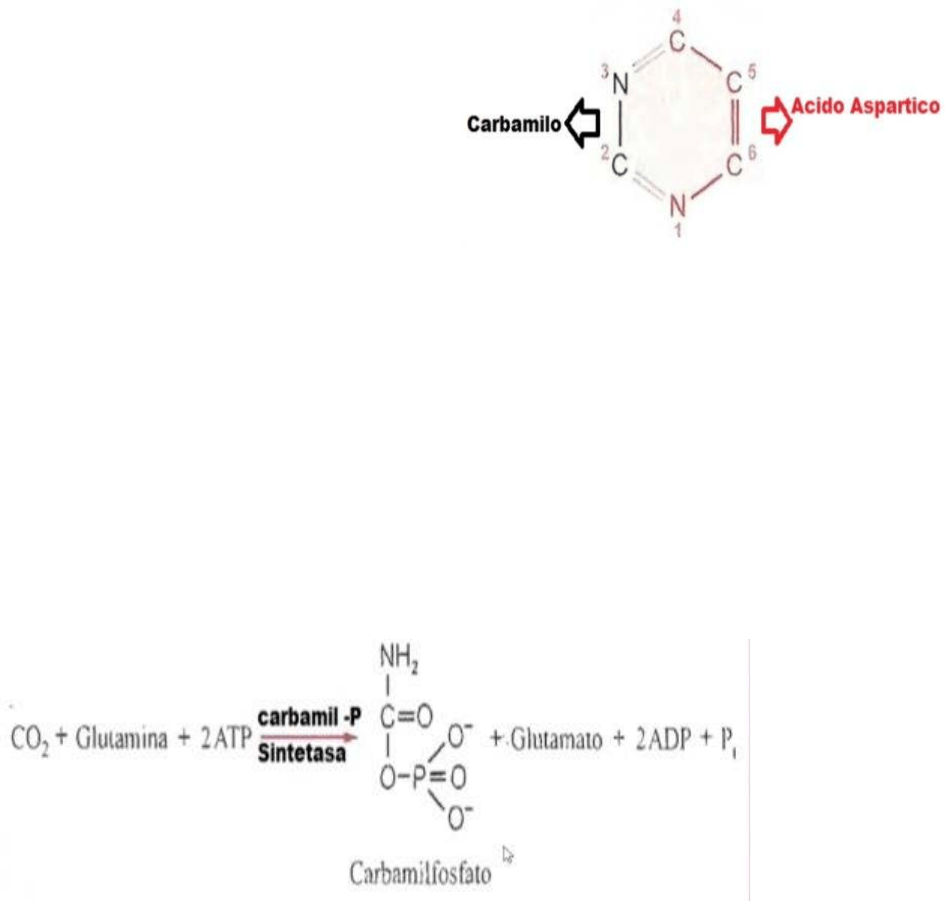
BIOSINTESIS DE PIRIMIDINAS
Las pirimidinas tienen un solo anillo y son
dos moléculas las que aportan la mayoría de
los carbonos y nitrógenos del anillo. El
nitrógeno 1 el C6, 5 y 4 son aportados el
aminoácido acido aspártico mientras que el
nitrógeno 2 y el C3 son aportados por
carbamilo.
En la síntesis de pirimidinas comienza con la producción de carbamil fosfato, por lo que CO2
reacciona con la glutamina (donante grupo amino) y 2ATP, formando carbamil fosfato,
glutamato (glutamina sin el grupo fosfato) y de la hidrolisis de los 2 ATP se obtiene 2 ADP y 1
Pi (el otro grupo fosfato fue donado para formar el carbamil fosfato). La enzima que participa es
la carbamil-fosfato-sintetasa. Esta enzima es citosólica, la otra es mitocondrial, la cual genera
carbamil fosfato en la primera etapa de la síntesis de la urea. Son isozimas.
Una vez formado el carbamil fosfato, va a interaccionar con el ácido aspártico formando el ácido
carbamil aspártico que luego se convierte en el ácido dihidroxoorótico y después en el acido
orotico. Ese acido interacciona con el fosforribosil pirofosfato generando un primer nucleótido
denominado uridin monofosfato que luego se descarboxila formando el primer nucleótido
pirimidico llamado uridina monofosfato.
La biosíntesis de las pirimidinas ocurre en paralelo con las de las purinas, debido a que en la
síntesis de las purinas se forma fosforribosil pirofosfato que sirve para la síntesis de purinas
como pirimidinas. Es por esto que en la célula hay la misma proporción de purinas y pirimidinas.
Una vez que se forma la uridina monofosfato o UMP la misa puede sufrir una descarboxilación
convirtiéndose en UDP, luego se puede volver a fosforilar formando UTP el cual puede adquirir
un grupo amino de la glutamina transformándose en citidina trifosfato, o puede sufrir una
reducción convirtiéndose en desoxiUDP (se reduce el azúcar), luego se desfosforila
convirtiéndose en dUMP y luego adquiere un grupo metil convirtiéndose en timina monofosfato.
Daiana Soto
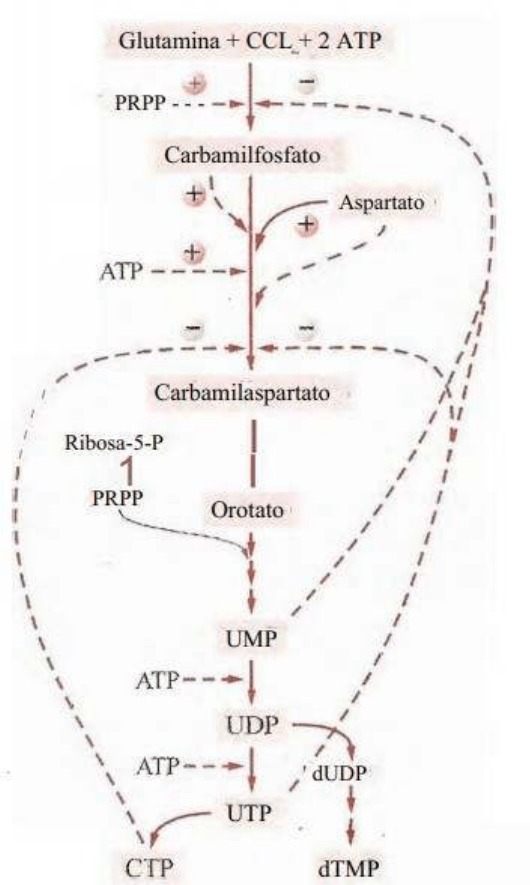
REGULACION DE LA SINTESIS DE LA
PIRIMIDINAS
Los nucleótidos obtenidos por esta vía pueden actuar
de manera negativa durante la etapa de formación de
carbamil fosfato actuando sobre la enzima, y además
sobre enzima que permite la unión de carbamil con el
aspartato formando carbamil aspartato.
Pero, además, las dos reacciones pueden ser
activadas, como el fosforribosil pirofosfato que
puede activar la enzima fosforribosil pirofosfato
sintetasa; el carbamil fosfato junto con el aspartato
puede estimular la actividad de la enzima siguiente
para que las dos moléculas se junten; el ATP puede
activar la segunda reacción.
CATABOLISMO DE LA PIRIMIDINAS
Las bases pirimídicas son degradadas hasta productos solubles, fácilmente eliminados o
utilizados por las células. La citosina, por desanimación, es convertida en uracilo; este recibe dos
hidrógenos donados por NADPH para formar dihidrouracilo. Posteriormente, por hidrólisis y
ruptura del anillo pirímídico, se producen p-alanina, CCL y NH, como productos finales.
La timina es hidrogenada a dibidrotimina en reacción ligada a NADPH. Luego el ciclo se abre y
se producen P-aminoisobutirato. CO2 y NH3, Eventualmente, el P-aminoisobutirato se convierte
en succinil-CoA, intermediario del ciclo del ácido cítrico.
Daiana Soto
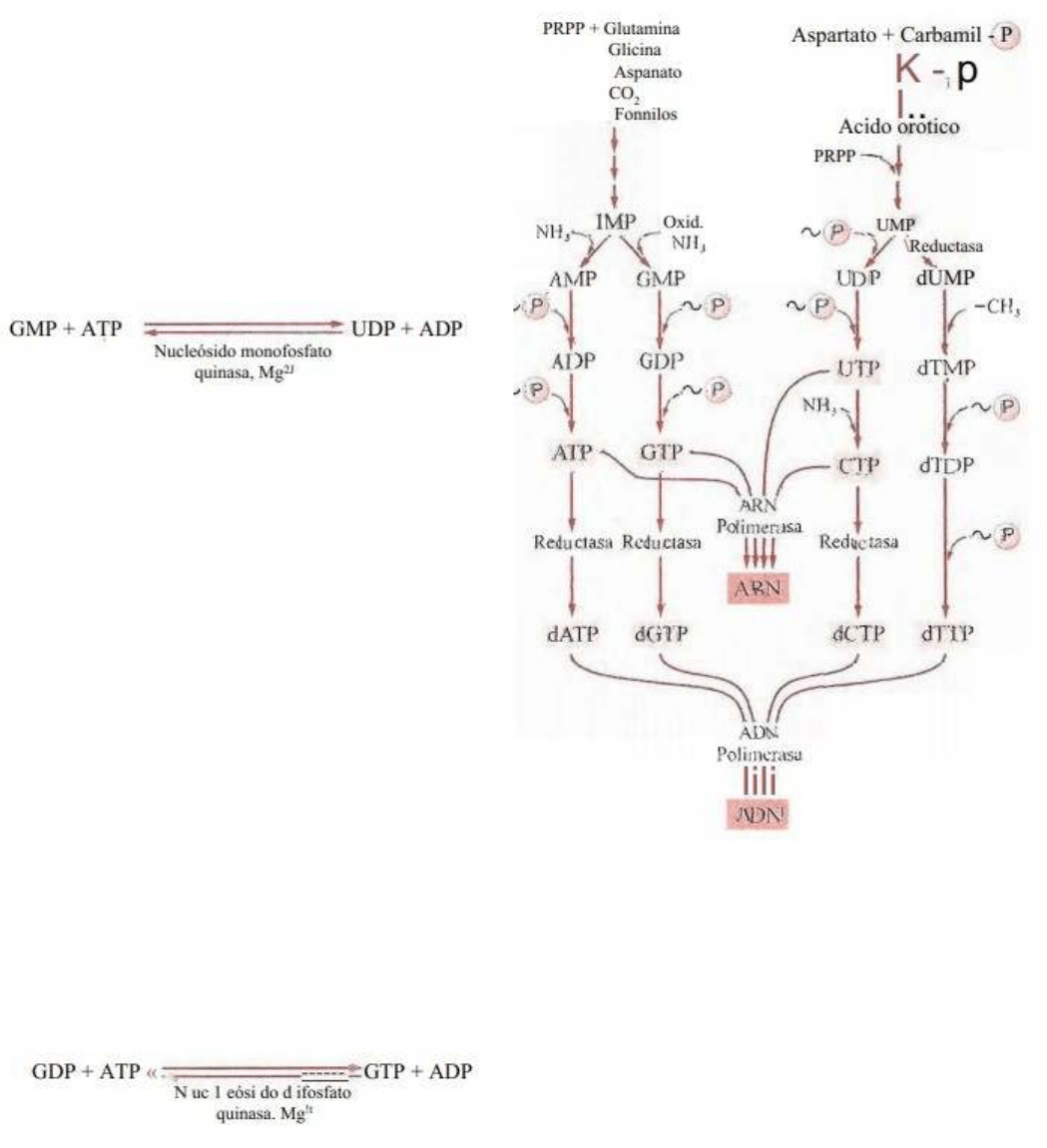
BIOSINTESIS DE NUCLOSIDOS DI Y
TRIFOSFORADOS
A la izquierda están los nucleótidos púricos y a la
derecha los pirimidicos.
Una vez sintetizado un nucleósido monofosfato se
le agregan grupos fosforilo por transferencia
desde un nucleósido trifosfato. Estas reacciones,
reversibles, son catalizadas por nucleósido
monofosfato y nucleósido difosfato quinasas.
En la síntesis ocurre primero la síntesis de nucleótidos mono fosforados, los cuales luego por
fosforilación sucesivas se convierten en tri fosforados.
El nucleósido difosfato reacciona con otra molécula de ATP para formar nucleósido trifosfato.
Los nucleósidos trifosfato participan en la síntesis de ácidos nucleicos. Si bien estas reacciones
pueden generar ATP a partir de ADP, la
fosforilación oxidativa es la vía preeminente
de producción de ATP.
El ATP, GTP, UTP y CTP si actúa una
ARN polimerasa se forma ARN, mientras que si sobre el ATP y GTP actúa una reductasa que
reduce el azúcar se convierten en desoxirribosa formando nucleótidos que luego la ADN
polimerasa la cual forma ADN, de la misma manera que lo hace el CTP.
Daiana Soto
Es por esto que se los necesita tri fosforados para que sean sustrato de la ARN y ADN
polimerasas. En el ácido nucleico quedan como monos fosforados.
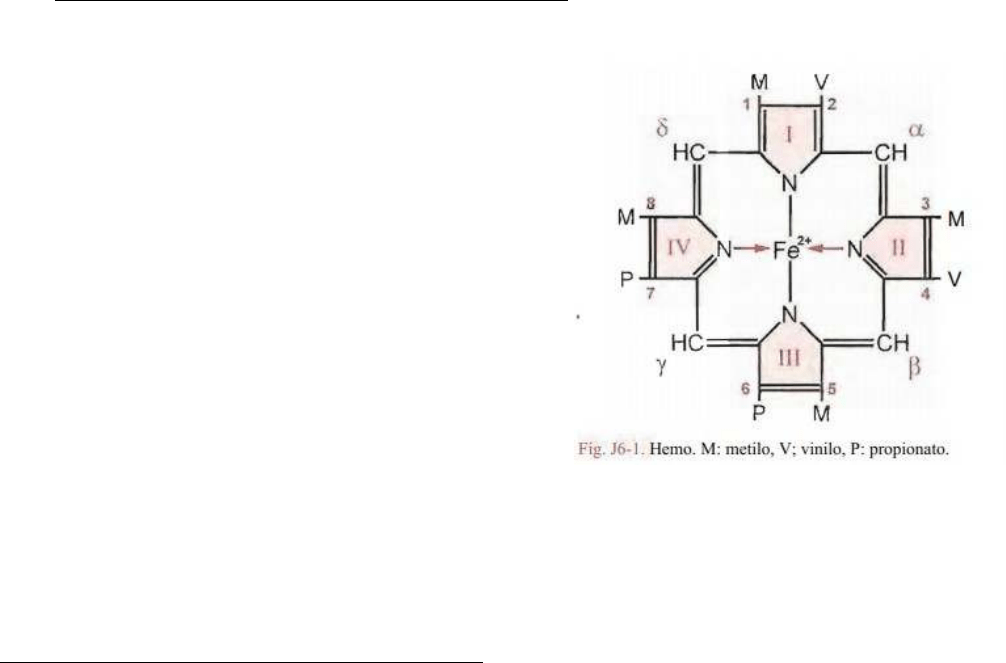
BIOSINTESIS DEL HEMO: SINTESIS DE PORFIRINA
El hemo:
Es el grupo prostético de las hemoproteínas,
hemoglobina, mioglobina, citocromos y enzimas.
Su estructura se forma por un ciclo tetrapirrolico
derivado de la protoporfirina III.
Diariamente se producen 300mg.
El 85% de su síntesis ocurre en células precursoras de los
eritrocitos en la medula ósea.
15% de su síntesis ocurre en hígado y otros tejidos.
SINTESIS DEL HEMO
El precursor protoporfirina III se sintetiza a partir de
glicina y succinil-CoA.
3 etapas: síntesis de ALA, formación de porfobilinogeno y síntesis de protoporfirina.
Cuando se añade el Fe a la protoporfirina se obtiene el hemo.
El proceso se realiza tanto en mitocondria como en citosol.
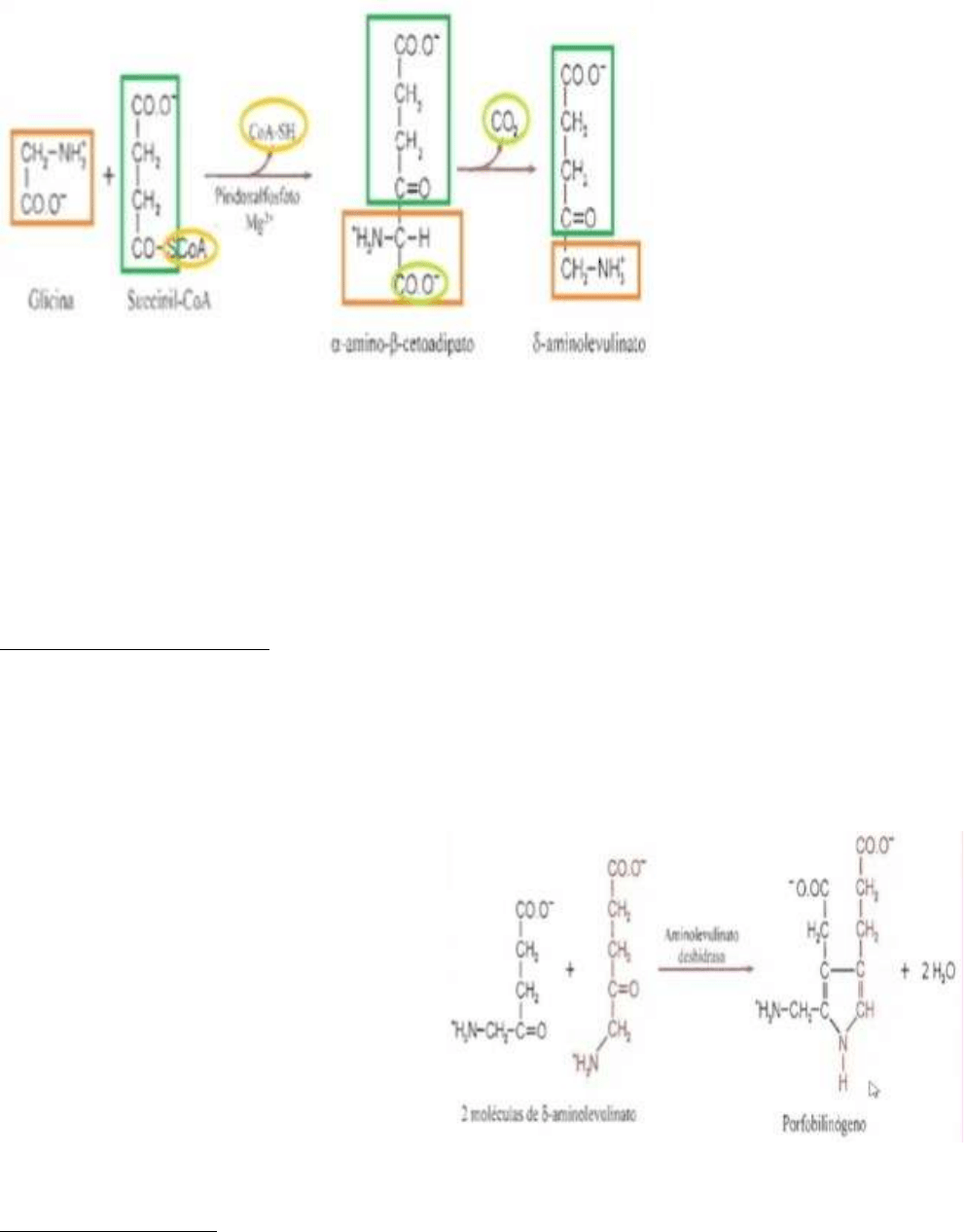
1) Formación de ALA (acido delta aminolevulinico):
Ocurre a nivel mitocondrial.
La enzima que participa es la delta aminolevulinato sintasa.
Coenzima: piridoxal fosfato.
Cofactor: catión Mg.
Principal sitio de control: hemo es inhibidor alostérico.
Síntesis enzimática inducida por: hipoxia, eritropoyetina, algunas hormonas esteroideas,
barituricos y alcohol
Daiana Soto
La glicina se condensa o se une al succinil-CoA que viene del ciclo de krebs. Previamente el
succinil-CoA pierde su coenzima A de tal manera de que la cadena de 4C de este se une a la
cadena de “C de la glicina, generando un primer compuesto denominado alfa-amino-beta-
cetoadipato el cual cuando se descarboxila se convierte en el ácido delta aminolevulinato
(están disociados los grupos aminos y carboxilos). El ALA está formado por los 4C que
viene del succinil-CoA y solo 1C y el grupo amino de la glicina, ya que el grupo carboxilo de
esta se perdió en la descarboxilación.
2) Síntesis del porfobilinogeno:
Una vez que se formó el ALA, el mismo migra de mitocondria a citosol donde continua la
síntesis de porfobilinogeno.
El proceso ocurre en el citosol.
Catalizado por la enzima delta aminolevulinato deshidrasa o porfobilinogeno sintasa.
Contiene catión Zn y grupos SH indispensables para su función.
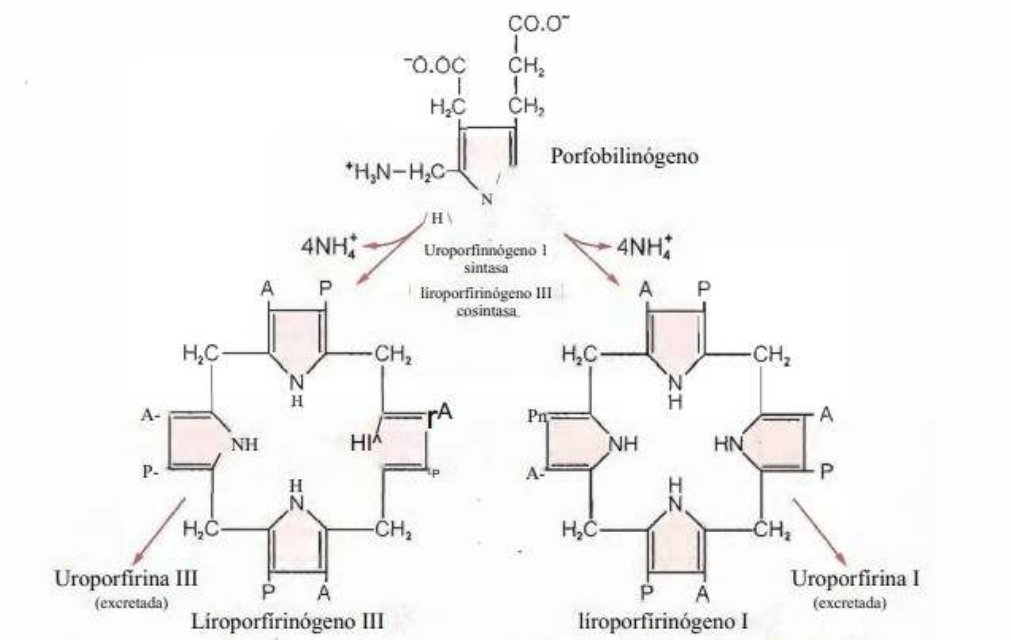
El producto obtenido, porfobilinogeno,
contiene el núcleo pirrol. El pirrol es el que
luego se junta con otros 3 pirroles para
formar el tetrapirrolico que es la
protoporfirina.
En este proceso se van a juntar 2 moléculas
de ALA y por acción de la enzima se produce
una deshidratación se formal el
porfobilinogeno que tiene estructura cíclica
que es el núcleo pirrol. Ese anillo tiene un
grupo amino, y unas cadenas carbonadas
laterales de 2 y 3 carbonos las cuales son el acetato (2C) y el propionato (3C).
3) Síntesis de la porfirina:
Daiana Soto
Ocurre en el citosol.
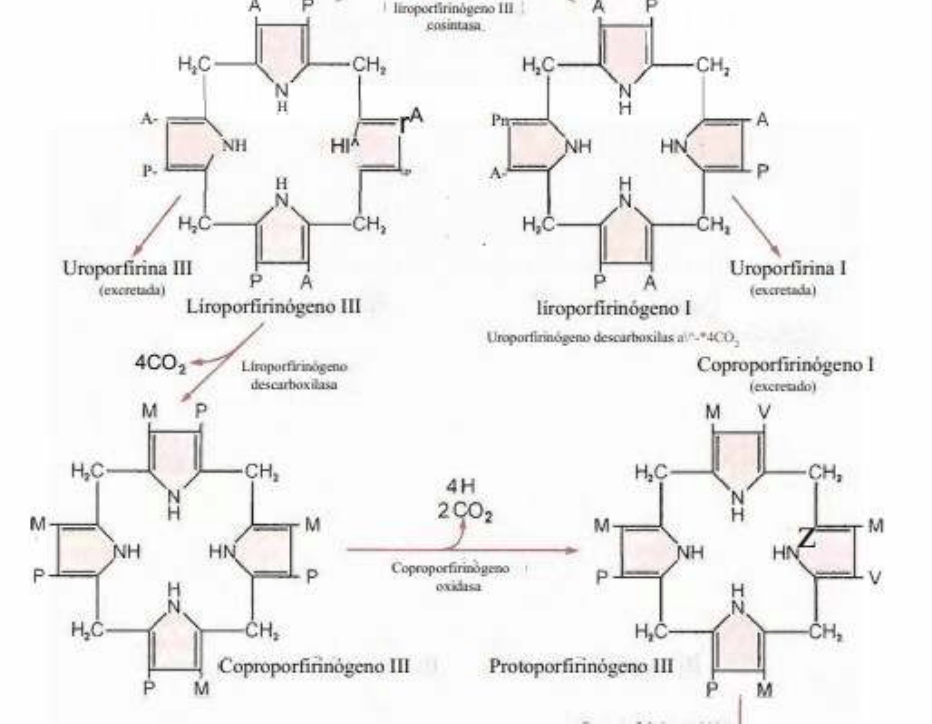
4 moléculas de porfobilinogeno forman un tetrapirrolico lineal que luego se cicla y
origina el uroporfirinogeno.
Se eliminan los grupos NH2 terminales de las cadenas de metilamina y los núcleos
pirroles se unen por puentes metilenos.
Se obtienen dos uroporfirinogenos I (disposición simétrica de A y P) y III (disposición
asimétrica de A y P) que son isómeros. El más abundante es el III, ya que se continua
para la síntesis del hemo.
El uroporfirinogenos I y sus derivados, uroporfirina y coproporfirinogeno I, no tiene
función definida y son eliminados por orina y heces, respectivamente.
Un porcentaje del uroporfirinogeno III que se forma, se elimina por orina y el resto va hacia la
síntesis del hemo.
Para que se originen estos dos isómeros participan 2 enzimas, la uroporfirinogeno I sintasa y la
uroporfirinogeno III cosintasa. Cada una se encarga de uno de los dos isómeros tetrapirrolicos
cíclicos.
Todo este proceso continúa siendo a nivel citosólico.
Daiana Soto
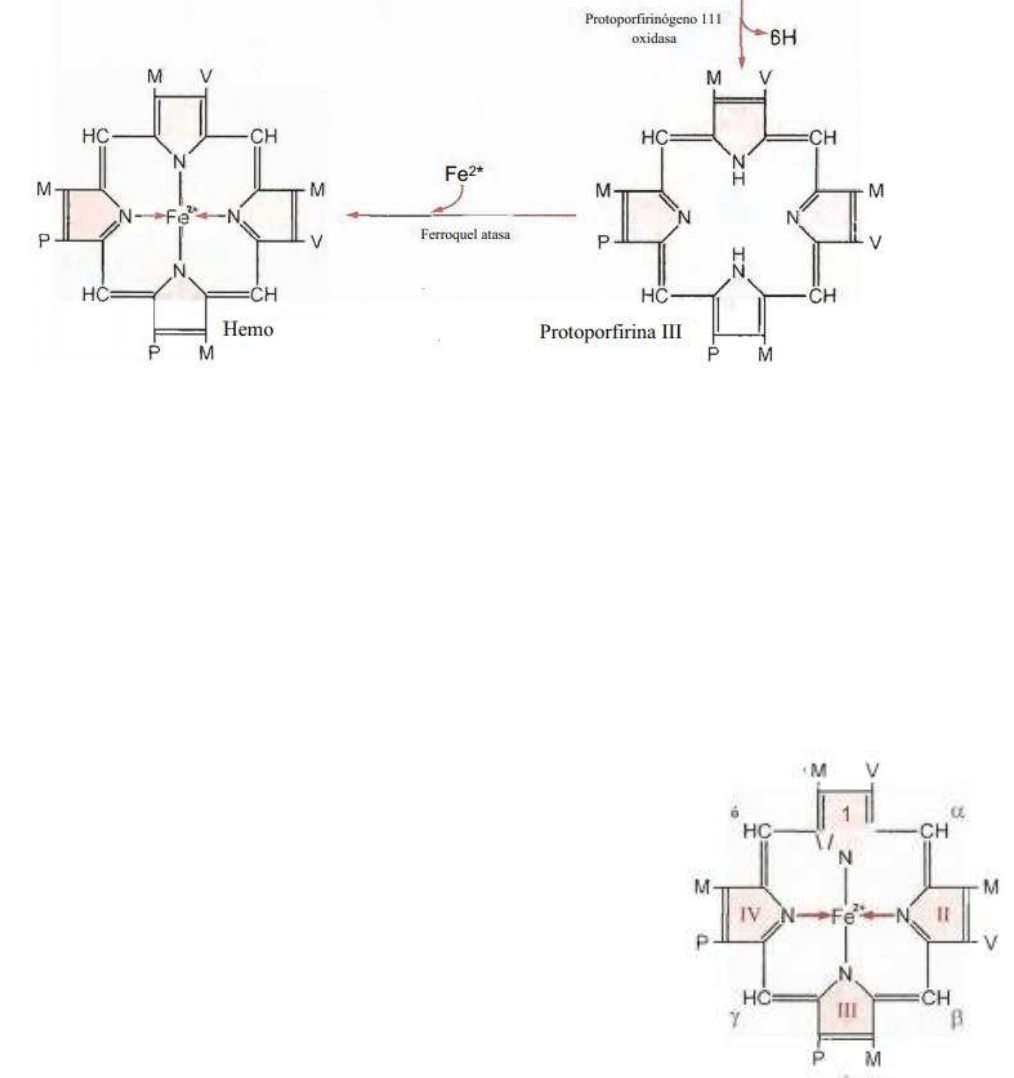
Una vez que se haya producida la síntesis de porfirina se continua con la síntesis de
protoporfirina III que es la precursora del hemo. Para eso, el uroporfirinogeno II que se acaba de
formar se va a descarboxilar, por la uroporfirinogeno descarboxilasa, convirtiéndose en
coproporfirinogeno III. Se descarboxilan los acetatos convirtiéndose en metilos. Una vez que se
forma el coproporfirinogeno III el mismo sufre una oxidación donde pierde 4H y una nueva
descarboxilación, la cual hace que algunos grupos propinilos se conviertan en vinilos (cadenas de
2C con dobles enlaces), esto sucede por la enzima coproporfirinogeno oxidasa.
El coproporfirinogeno III generado en citosol a partir del uroporfirinogeno III, ingresa a la
mitocondria en donde continua el proceso hasta la formación del hemo
ADICCIÓN DEL HEMO
Daiana Soto
A nivel mitocondrial, el protoporfirinogeno III se oxida nuevamente, pierde H a partir de los
puentes metilos, por lo que se produce la protoporfirina III por acción de la enzima
protoporfirina III oxidasa. A esta molécula, al ser la precursora del hemo, se le agrega Fe por
la enzima ferroquelatasa, el mismo se une al centro estableciendo 4 uniones coordinadas con
los nitrógenos de los pirroles originando el hemo.
PORFIRIAS
Existe un grupo de enfermedades caracterizadas por aumento de la excreción de porfirinas o sus
precursores. Estas enfermedades, denominadas porfirias, son causadas por bloqueos en la vía de
síntesis de hemo y pueden ser hereditarias o adquiridas. En general se caracterizan por
acumulación de intermediarios de las etapas anteriores a la catalizada por la enzima afectada y
disminución de los metabolitos de los pasos siguientes. En todas, la producción de hemo está
deprimida; esto estimula la síntesis de 8- aminolevulinato sintasa y exacerba la acumulación de
intermediarios.
Las porfirias hereditarias se distinguen en eritropoyéticas o hepáticas, según el órgano en el cual
se manifieste predominantemente el defecto. Mencionaremos sólo algunas de las enfermedades
de este grupo.
CATABOLISMO DEL HEMO
Cada 120 días los glóbulos rojos se destruyen en el sistema
retículo endotelial. Esto hace que se libere el hemo y las
globinas.
Las globinas son degradadas a aminoácidos, los cuales pasan a
formar parte del pool metabólico para ser reutilizados.
El hemo sufre una serie de transformaciones que ocurren en SRE
(sistema retículo endotelial), hígado e intestino. Se divide en esa
tres etapas.
Daiana Soto
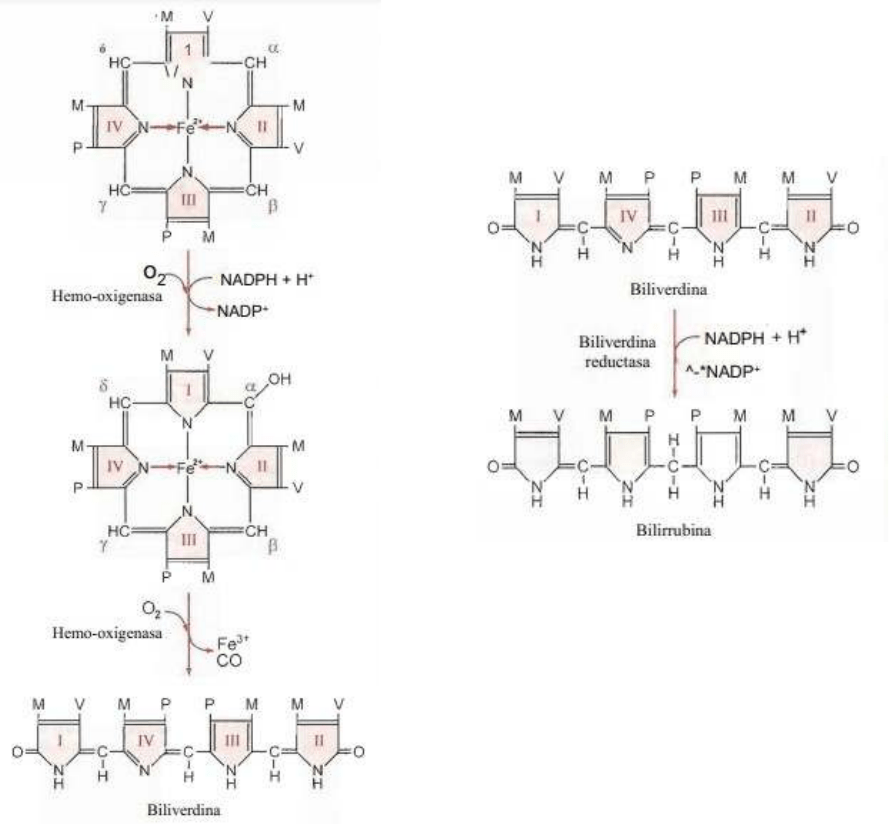
ETAPA SRE:
En el SER de baso, hígado y medula sea se lleva a cabo la etapa inicial.
El sistema multienzimatico de la hemo oxigenasa cataliza esta etapa, donde el hierro
pasa de estado ferroso a estado férrico y donde el puente metino alfa es convertido en
CO.
El hierro es rápidamente separado y almacenado para ser reutilizado.
El producto final es la biliverdina, un tetrapirrol lineal.
Una vez formada la biliverdina, esta es reducida en el puente metino que uno los pirroles
IV y III por la biliverdina reductasa y se transforma en la bilirrubina, un pigmento
amarillo-naranja insoluble en agua y soluble en lípidos. Se requiere de NADP+H para
que provea los H para hacer la reducción de los puentes metinos.
La bilirrubina puede atravesar la membrana celular. Es una sustancia toxica.
Por cada gramo de hemoglobina degradada, 35mg de bilirrubina se generan.
Este documento contiene más páginas...
Descargar Completo
2 DIGESTIÓN Y ABSORCION DE PROTEINAS Y METABOLISMO DE AA.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.