
FÍSICA BIOLÓGICA
DISPERSIONES. SOLUCIONES. CONCENTRACIÓN
JTP. Carlos J. Dabin - Prof. Adj. Graciela Bazzoni. Cátedra de Biofísica.
Facultad de Ciencias Médicas, UNR.
Contenidos
Introducción.
Dispersiones. Denición y clasicación. Solubilidad
Concentración de una solución y sus distintas formas de expresión.
Empírica.
Molaridad. Número de Avogadro. Mol. Molécula-gramo.
Normalidad. Ley de electroneutralidad. Equivalente químico-gramo.
Osmolaridad.
Diferencia entre concentración y cantidad de soluto.
Relación PM, mol, equivalente, osmol.
Dilución
INTRODUCCIÓN
En nuestra vida cotidiana, podemos entender a la materia como “todo aquello que está”, “que ocupa un espa-
cio”, “que llena un recipiente” o “que impresiona nuestros sentidos”. Con más rigor cientíco, la materia es todo
aquello que tiene masa y ocupa un lugar en el espacio y las sustancias químicas son tipos o clases de materia.
Cada sustancia química tiene propiedades que la identican y que permiten reconocerla. Podemos mencionar
la existencia de sustancias puras, ejemplo: los elementos químicos como sodio (Na), hierro (Fe), calcio (Ca),
cloro (Cl) y mezclas de sustancias que pueden dar lugar a sistemas homogéneos o sistemas heterogéneos.
En cuanto a los sistemas homogéneos, todas las porciones que los constituyen son exactamente iguales, no
observándose límites físicos o paredes físicas entre ellas (por ejemplo: mezcla de agua y vinagre). Por el con-
trario, en los sistemas heterogéneos no todas las porciones que los constituyen son uniformes en composición,
estructura y propiedades, pudiéndose percibir límites de separación entre ellas (por ejemplo: mezcla de agua y
aceite). Cada una de estas distintas porciones del sistema se llama fase y se hallan separadas por supercies
bien delimitadas, que se conocen como interfases. Por lo tanto sistemas homogéneos son aquellos constitui-
dos por una sola fase, sistemas heterogéneos son aquellos constituidos por más de una fase.
DISPERSIONES: Definición y Clasificación
Nuestro medio interno está formado por diferentes sustancias disueltas constituyendo las denominadas solu-
ciones. Pero las soluciones son una de las formas en que se clasican las dispersiones.
Una dispersión es la mezcla de dos o más sustancias, denominándose soluto o fase dispersa a la/s
sustancia/s que se encuentran en menor cantidad en el seno de otra mucha más abundante llamada solvente
o fase dispersante. Los componentes de esa mezcla pueden verse como una sola fase o distintas fases,
como por ejemplo: azúcar en agua, aceite en agua.
Existen diferentes tipos de dispersiones que resultan de las combinaciones posibles entre los tres estados
de la materia (sólido, líquido y gaseoso) Ej.: sólido en sólido (piedras), sólido en gas (humo), gas en sólido
(esponja), líquido en líquido (aceite en agua), etc.
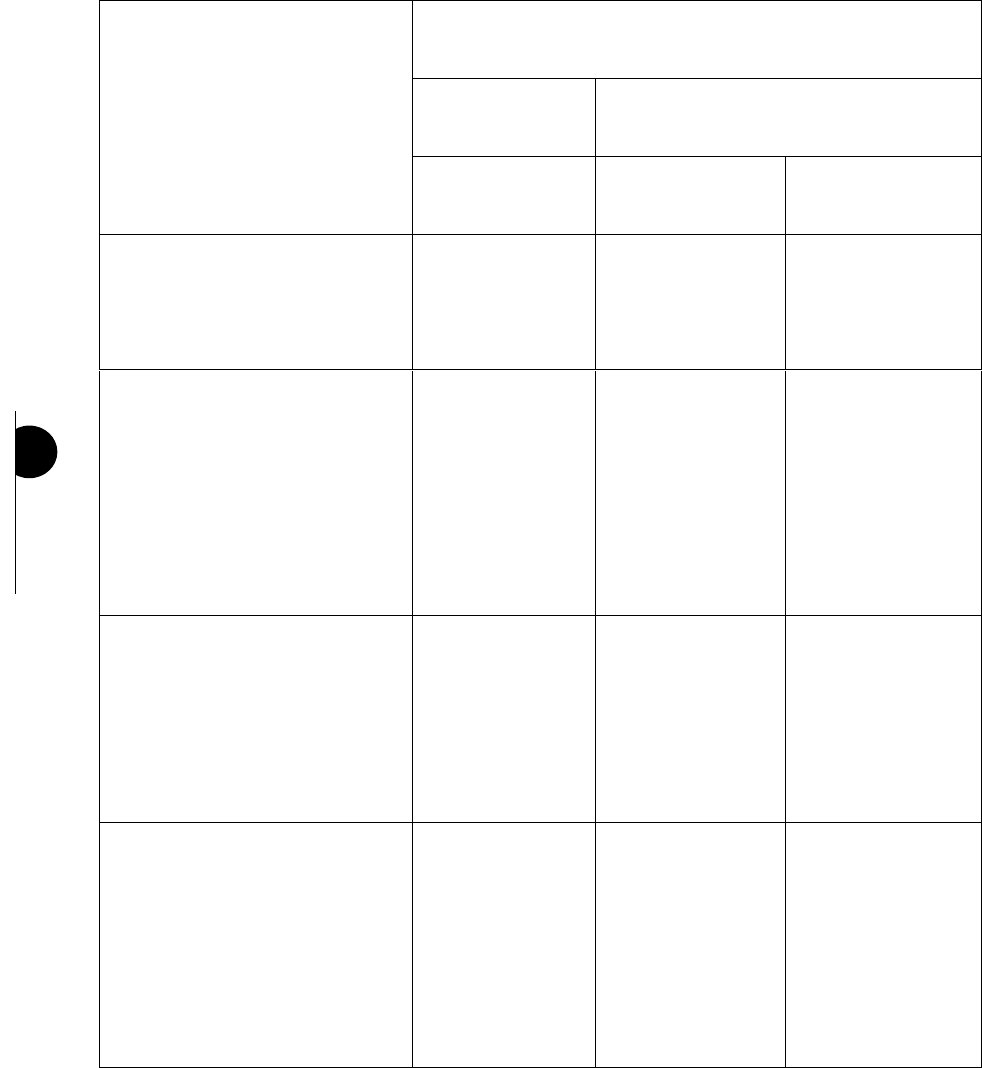
El tamaño de las partículas dispersas condiciona muchas de las propiedades de las dispersiones, por lo que
se lo utiliza como criterio de clasicación. El tamaño del soluto afecta la visibilidad (a simple vista o con el uso
91
Guía de Aprendizaje - Crecimiento y Desarrollo - 1-9
de dispositivos ópticos especiales), la estabilidad en solución y la posibilidad de que el soluto difunda a través
de membranas que presentan poros de diferente tamaño (difusibilidad). Se denen así tres tipos de dispersio-
nes cuyas características se muestran en la tabla siguiente.
CARACTERÍSTICAS
TIPO DE DISPERSIÓN
HETEROGÉNEAS HOMOGÓNEAS
GROSERAS COLOIDALES VERDADERAS
Tamaño de las partículas
en nm (1nm=10-9m)
Mayor a 100 De 1 a 100 Menor de 1
Ejemplos
arena en agua
humo
aceite en agua
plasma
el líquido intersticial
cremas cosméticas
ultraltrado plasmático
en túbulo renal
lágrimas
sudor
azúcar en agua
sal en agua
Estabilidad
• gravedad
• centrifugación
• ultracentrifugación
No
No
No
Si
Si
No
Si
Si
Si
Difusibilidad a través de las mem
branas
• permeable
• dialíticas
• semipermeables
No
No
No
Si
No
No
Si
Si
No
Nota: Las dispersiones coloidales y verdaderas también son denominadas soluciones coloidales y
verdaderas, respectivamente
92
SOLUBILIDAD
Este concepto debe ser introducido para comprender ciertos aspectos de la teoría de soluciones que desa-
rrollaremos.
Se dene a la solubilidad como la máxima cantidad de soluto que se disolverá en un volumen dado de sol-
vente, a una temperatura dada, para producir una solución estable. Una solución es no saturada cuando la
cantidad de soluto es menor a la máxima, y sobresaturada cuando la cantidad de soluto es mayor. Una solución
está saturada cuando no se le puede incorporar más soluto, entonces precipita sin disolverse, en consecuencia
coexisten o pueden existir en equilibrio dos fases, una sólida y otra líquida. Si se enfría lentamente una solución
saturada, se puede llegar a obtener una solución de mayor concentración a esa temperatura, entonces se dice
que está sobresaturada
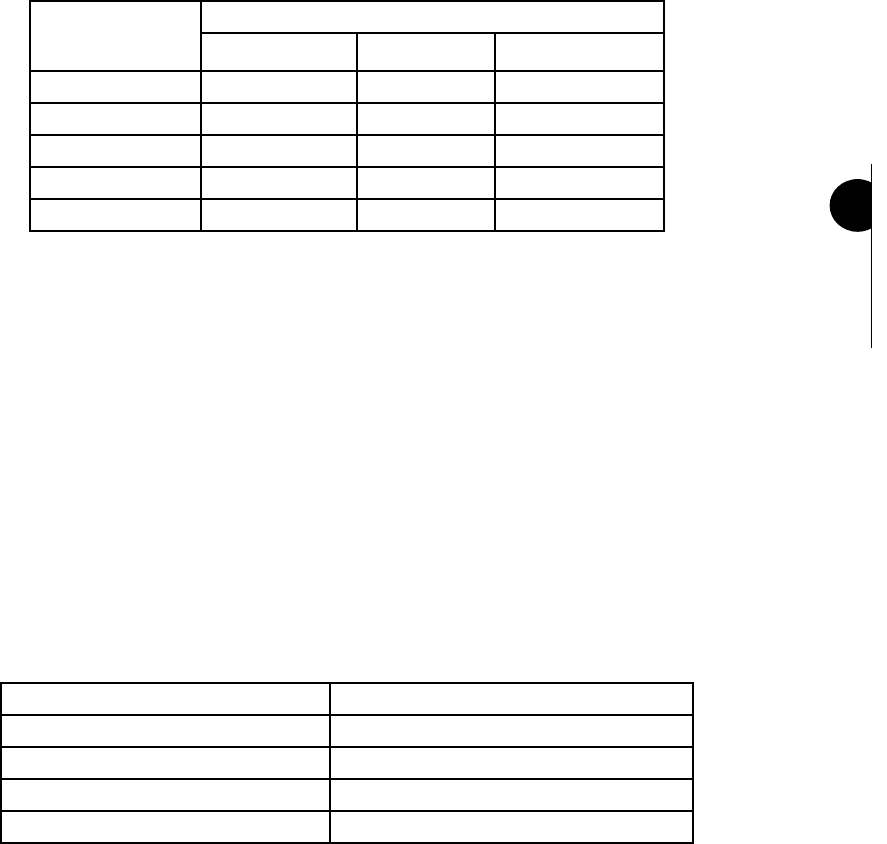
La temperatura es un factor importante que afecta la solubilidad de un soluto. En la tabla siguiente puede
verse algunos ejemplos de esta inuencia
SAL
Solubilidad g/100
20ºC 40ºC 80ºC
KCl 33 39 50
KNO
3
33 65 168
KClO
3
8 15 40
NaCl 37 37 38
NaNO
3
88 106 147
Concentración de una Solución
La concentración de una solución es la cantidad de soluto que se encuentra disuelto por unidad de cantidad
de solvente o de solución y se expresa como el cociente entre estas dos magnitudes:
C = Q/V
Siendo
C: concentración
Q: cantidad de soluto
V: volumen de solución
Formas de expresar la concentración de una solución
La concentración de una solución se puede expresar de distintas formas, dependiendo de la manera en
que se exprese la cantidad de soluto y la unidad de volumen que se tome como referencia: 1litro de solución
(1000ml) y en algunos casos 100ml.
Cantidad de soluto expresada en La concentración se denomina
gramos EMPÍRICA
moles MOLARIDAD
equivalentes NORMALIDAD
osmoles OSMOLARIDAD
a) EMPÍRICA
Es la forma cotidiana y más simple de expresar la concentración.
Es el número de gramos (u otra unidad en que se exprese la masa) de soluto presentes en 100 ó 1000
cm
3
(cc o mililitro) de solución.
Cuando el volumen de referencia es de 100 ml, la forma empírica se expresará como g%, mg%, etc.; mientras
que, si el volumen es de 1000ml resultan las expresiones g‰, mg‰, etc.
Es una de las aplicaciones más frecuentes en Medicina para expresar la concentración en plasma de sustan-
93

Guía de Aprendizaje - Crecimiento y Desarrollo - 1-9
cias tales como glucosa, urea, triglicéridos o colesterol. Por Ej: el rango normal de la concentración de glucosa
en sangre (glicemia) es: 70 - 110mg% (ó 0,7 - 1,10g‰).
Aplicación:
¿Cuál será la concentración (C) empírica de una solución donde se disolvieron 3g de glucosa, alcanzándose
un volumen total de 20ml?
Datos del problema:
V: 20 ml solución Q: 3 g C empírica: incógnita
Solución del problema:
I) 3g 20 ml solución O II) 3g 20 ml solución
x g 100 ml solución x g 1000 ml solución
x = 15g x = 150g
Respuesta: g % = 15
g ‰ = 150
b) MOLARIDAD
Previo a la denición de esta forma de concentración debemos introducir algunos conceptos como:
NÚMERO DE AVOGADRO: Esta constante universal tiene un valor de 6,023x10
23
entes. El número de Avoga-
dro expresa una cantidad ja similar a cuando expresamos la cantidad en docenas. Es decir, sabemos que una
docena expresa una cantidad ja que es 12.
MOL: Es la cantidad de materia que contiene 6,023 × 10
23
(número de Avogrado) entes de la misma especie
(moléculas o átomos). Por ejemplo: en 1 mol de urea hay 6,023 × 10
23
moléculas de urea; en 1 mol de ATP hay
6,023 × 10
23
moléculas de ATP; en 1 mol de zinc hay 6,023 × 10
23
átomos de Zn.
Se establece que la masa de esa cantidad de materia donde se encuentran 6,023 × 10
23
moléculas de esa
sustancia se denomina molécula gramo o mol gramo y coincide con el valor del peso molecular ó atómico ex-
presado en gramos. Retomando el concepto de docena: en una docena de manzanas sabemos que hay doce
manzanas y en una docena de sandias también hay doce sandias pero el peso dependerá de cada tipo de
fruta. Ejemplo: glucosa (PM 180) y albúmina (PM 67.000), teniendo en cuenta lo dicho anteriormente el número
de Avogadro de moléculas de glucosa (6,023 .10
23
) le corresponde una masa de 180g; mientras que el mismo
número de moléculas de albúmina pesará 67.000g (67kg)
Una vez comprendido el concepto de mol, podemos denir Molaridad (M) de una solución como: “la cantidad
de moles de soluto contenidos en un litro de solución”. (M = moles/l ó moles/1000ml,)
Como en cualquier sistema de medidas, el prejo mili (m) equivale a 10
3
(1000) veces más chico, por lo tanto
1mol=1000mmoles; 1 milimol= 0,001 mol, es decir 10
-3
mol. Por lo tanto, 1mM=1milimolar= 0,001M: 1 mmoles/l
ó 1 mmoles/1000ml.
Esta forma de expresar la concentración no se utiliza en la vida cotidiana, pero es importante en Medicina
porque reeja la composición molecular de las soluciones.
Aplicación:
Calcular la M (molaridad) de un litro de solución compuesta por 117g de NaCl (PM: 58,5) y de un litro de solu-
ción que contiene 360 g de glucosa (PM: 180).
Datos del problema:
Solución 1: V: 1 litro Q
NaCl
: 117 g PM
NaCl
: 58,5 M: incógnita
94

Solución 2: V: 1 litro Q
Glucosa
: 360 g PM
glucosa
: 180 M: incógnita
Solución del problema:
Solución1:
1 mol de NaCl 58,5 g
x mol NaCl 117g en 1000ml de solución
x = 2 moles de NaCl en 1000 ml de solución
Solución 2:
1 mol de glucosa 180 g
x mol glucosa 360 g en 1000 ml de solución
x = 2 moles de glucosa en 1000 ml de solución
Respuesta: solución 1: 2 M ó 2 moles de NaCl en 1 litro de solución (1000 ml)
solución 2: 2 M ó 2 moles de glucosa en un litro de solución (1000ml)
Algunas consideraciones sobre la molaridad:
A) Dos soluciones pueden estar compuestas por distintos solutos que tienen la misma molaridad, en el ejem-
plo anterior: 2M, el mismo número de moléculas (2 x 6,023
23
moléculas) PERO, nótese, que la MASA que las
contiene es DIFERENTE
B) Si en un canasto colocamos 5 manzanas y 5 sandías, podemos decir que hay 10 frutas. Pero son frutas dife-
rentes, si lo relacionamos con el concepto de mol, deberemos citar la cantidad de cada fruta por separado. En
nuestro caso, si 2 solutos diferentes forman parte de una misma solución (por ejemplo: en un litro de solución
tenemos 2 moles de glucosa y 2 moles de urea) no se puede calcular la molaridad total de la solución (el re-
sultado 4M sería erróneo). Este resultado equivoco surge de no haber contemplado la denición de mol: can-
tidad de entes de la misma especie. Entonces, deberemos informar por separado la molaridad de cada soluto
que constituye la solución. (M de la glucosa= 2 y M de la urea= 2, ambas forman parte de una misma solución).
c) NORMALIDAD
Antes de denirla, debemos conocer y entender la ley de electroneutralidad, y el concepto de equivalente
químico gramo
LEY DE ELECTRONEUTRALIDAD: Es una propiedad fundamental de toda solución electrolítica cuyo enun-
ciado establece: “En solución, la carga positiva total de los cationes es igual en valor absoluto a la carga
negativa total de los aniones”.
Discutamos brevemente este enunciado. Si bien toda molécula es eléctricamente neutra, existen moléculas de
determinadas sustancias que puestas en agua se disocian generando partículas cargadas (positivas y negati-
vas). A esas sustancias se las denomina electrolitos (porque conducen la corriente eléctrica) y a las partículas
cargadas iones. Los iones pueden tener carga positiva (cationes) o carga negativa (aniones). Por lo tanto
cuando una solución contiene por ej. NaCl, KCL y CaCl
2
la cantidad total de cargas negativas (CL
-
) es igual a
la de las cargas positivas (Na
+
, K
+
y Ca
++
).
De esta forma se enuncia: los iones se neutralizan equivalente a equivalente de forma tal de cumplir con la ley
de electroneutralidad.
EQUIVALENTE QUÍMICO GRAMO: En Fisiología, se aplica el equivalente químico a los electrolitos. El equi-
valente químico (eq.qco. o Eq) es la cantidad de materia que contiene el número de Avogadro de valencias.
95

Guía de Aprendizaje - Crecimiento y Desarrollo - 1-9
Una sustancia puede tener distintos valores de equivalente químico según la reacción en que forma parte, por lo
cual se lo dene para cada tipo de reacción. Por ejemplo en la neutralización, en oxido-reducción, en formación
de complejos, etc.
Ahora bien, para determinar la masa que corresponde a un equivalente de cualquier sustancia, se debe conocer
el peso molecular de ese soluto y la disociación. Entonces: la masa de un equivalente se obtiene dividiendo
el peso molecular expresado en gramos por el número de cargas o valencias que dan lugar a una molécula
neutra. (Masa de 1 eq = PM gr / nº de cargas o valencias puestas en juego)
Entonces, la normalidad (N) de una solución es “la cantidad de equivalentes químicos de un electrolito
contenidos en un litro de la misma”. (N: eq/l o eq/1000ml; milinormal (mN): milieq/l o meq/l) 1Eq = 1000mEq
y 1mEq= 0,001 Eq.
Aplicación:
Cuando la sal sólida de NaCl (cloruro de sodio) o la de AlCl
3
(cloruro de aluminio) se disuelven en agua, se
disocian en:
I) NaCl → Na+ + Cl- (PM=58,5)
Cada molécula al disociarse da como resultado una carga positiva y otra negativa (intercambian una sola va-
lencia). Entonces en 58,5g de NaCl se tiene un mol (6,023 × 10
23
moléculas) pero también 1eq.qco (6,023 ×
1023 valencias).
II) AlCl3 → Al
+++
+ 3 Cl
-
(PM: 132)
Cada molécula al disociarse da como resultado 3 cargas positivas y 3 negativas. Por lo que 132g representa la
masa de un mol (6,023 × 10
23
moléculas) y de 3 eq.qco. (3 x 6,023 × 10
23
valencias)
Como puede observarse, para obtener la relación entre moles y equivalentes se hace uso de la ecuación de
disociación electrolítica
Aplicación:
Se tiene una masa de 5 g de NaCl (PM:58,5) en 250 ml de solución. ¿Cuela será la N?
Datos del problema:
V: 250 ml
Q: 5 g de NaCl PM
NaCl
: 58,5
N: incógnita.
Solución del problema:
1 eq.qco. NaCl -------- 58,5 g
x eq.qco. NaCl ------- 5 g
x = 0,086 eq.qco. de NaCl
dado que 0,086 eq.qco. equivalen al peso de 5g disueltos en 250 ml; entonces:
0,086 eq.qco.NaCl ------------------ 250 ml
x eq.qco. NaCl ------------------ 1000 ml
x= 0,344 eq.qco. NaCl en 1000 ml de solución.
Respuesta: 0,344 N (normal) ó 0,344 eq.qco. de NaCl en un 1 litro de solución.
El plasma sanguíneo contiene Na
+
, K
+
, Ca
++
, Cl
-
, CO
3
H
-
, etc., provenientes de sales que al disociarse genera-
96

ron esos iones. Pero una vez liberados, ya no se sabe que sales los generaron, por esto la composición está
dada en iones. Sin embargo, dado que provienen de la disociación de sales neutras, se cumple que el número
de equivalentes de cationes es exactamente igual al número de equivalentes de aniones.
De acuerdo a los libros de Fisiología, la composición electrolítica de los líquidos corporales es la siguiente:
Plasma Líquido intersticial Líquido intracelular
Cationes (mEq/l)
Na
+
142 145 10
K
+
4 4,1
159
Ca
++
2,5 2,4
<1
Mg
++
1 1
40
Total
149,5 152,5 209
Aniones (mEq/l)
Cl
-
104 117
3
CO
3
H
-
24 27,1
7
Proteinatos 14 <0,1
45
Otros 7,5 8,4
154
Total
149,5 152,5
209
d) OSMOLARIDAD
Esta forma de expresar la concentración nos permite predecir el intercambio de líquido entre compartimentos
cuando la membrana sólo deja pasar al solvente (membrana semipermeable). Este fenómeno denominado
ósmosis se debe a que el agua se desplaza desde el compartimiento donde los solutos están menos concen-
trados (el que tiene mayor proporción de agua) al de mayor concentración de solutos (menor proporción de
agua), y será estudiado con mayor atención en el Área EL SER Y SU MEDIO.
Osmolaridad es el número de osmoles de soluto dispersos en un litro de solución. El osmol es la can-
tidad de materia que contiene el número de Avogadro de partículas. Esta forma de concentración se abrevia
Osm.
La cantidad de osmoles no depende del tamaño, ni la carga, ni la naturaleza química del soluto, sino del
número total de partículas presentes en la solución. Cuando la cantidad de soluto es pequeña se utiliza el
submúltiplo miliosmol (1osmol=1000miliosmoles) y la concentración se expresa como miliosmolar (mOsm).
Así, cuando se solubiliza cualquier sustancia no electrolítica (Ej.: glucosa, sacarosa o urea) sus moléculas se
hallan separadas entre sí por moléculas de solvente pero no se disocian y un mol produce 6,023.10
23
partículas
97

Guía de Aprendizaje - Crecimiento y Desarrollo - 1-9
es decir, un osmol. En cambio, si se considera un electrolito -como NaCl- cada molécula al disolverse se separa
(NaCl →Na
++
Cl
-
) dando lugar: a 1 catión y a 1 anión y cada uno de ellos corresponden a 1 partícula. Esto quiere
decir que en 58,5 gramos de NaCl (1mol: 6,023 × 10
23
moléculas) existe 2 veces el número de Avogadro (6,023
× 10
23
) de partículas.
Del ejemplo anterior se puede deducir que la masa de un osmol de cualquier sustancia se calcula dividiendo
el peso molecular (PM) expresado en gramos por el número de partículas que aporta cada molécula.
DIFERENCIA ENTRE CONCENTRACIÓN Y CANTIDAD DE SOLUTO
Resulta importante distinguir la diferencia entre estos dos conceptos. Para ello, centraremos la atención en la
noción de propiedades de la materia.
Las propiedades intensivas son aquellas que no dependen de la cantidad de sustancia o del tamaño de un
cuerpo, por lo que el valor permanece constante al subdividir el sistema inicial en varios subsistemas, por este
motivo no son propiedades aditivas (por ejemplo: temperatura, color, sabor, densidad).
Por el contrario, las propiedades extensivas son aquellas que sí dependen de la cantidad de sustancia o del
tamaño de un cuerpo, y por lo tanto se modican cuando se fracciona el sistema original. Estas magnitudes
pueden ser expresadas como la suma de las magnitudes del conjunto de subsistemas que forman el sistema
original (por ejemplo: masa, longitud, volumen). Esto se conoce como aditividad.
Aplicación:
Si preparamos un litro de una solución 0,1M de glucosa (0,1 mol de glucosa en 1000 ml de solución), la con-
centración será 0,1M en cualquier parte del sistema.
A) Si dividimos este litro de solución en dos recipientes - uno de 400 ml y otro de 600 ml - la concentración en
cada uno de ellos seguirá siendo la misma: 0,1M.
Por lo denido anteriormente, la concentración es una propiedad intensiva.
B) La cantidad de glucosa y la cantidad de agua en cada uno de los recipientes será diferente a la del recipiente
original
1000ml _______0,1mol
400ml ______ x = 0,04mol
Y haciendo el mismo razonamiento, en 600ml hay 0,06mol
Sumando independientemente volumen de solución y cantidad de sustancia, dan como resultado:
1000ml _______0,1mol
Por lo tanto, (por presentar aditividad) volumen y cantidad de sustancia son propiedades extensivas.
RELACIÓN PM, Mol, Equivalente, Osmol
La cantidad de soluto presente en una solución y la concentración de la solución, como vimos hasta ahora,
podemos expresarla de distintas maneras. Estas formas se pueden ínter convertir. Para ello debemos conocer
el peso molecular (PM) y si se trata de un soluto que se disocia (electrolito) o un no electrolito (molécula que no
se disocia). En el caso de un electrolito necesitamos conocer su ecuación de disociación.
Aplicación:
Ejemplo 1: soluto que se disocia
NaCl → Na
+
+ Cl
-
(PM=58,5)
I) cada molécula nos da 2 partículas (1mol = 2osmoles)
II) hay 1 valencia en juego (1mol = 1Eq)
III) recordando el concepto de molécula-gramo (1mol = 58,5gr)
98

Ahora podemos reunir todo lo razonado y tendremos:
NaCl: 1mol = 2osmoles = 1Eq = 58,5gr
Ejemplo 2: soluto que no se disocia
Urea. (PM: 60)
I) cada molécula es una partícula (1mol = 1osmol)
II) al no disociarse, no expresa qué cantidad de valencias hay en juego.
III) 1mol de urea tiene una masa de 60gr.
Por lo tanto:
urea: 1mol = 1osmol = 60gr
Procediendo de igual manera con cada soluto, obtendremos las equivalencias:
Ca Cl
2
: CaCl
2
→ Ca
++
+ 2 Cl
-
(PM: 111) 1mol = 3osmoles = 2Eq =111gr
NaCO
3
H: NaCO
3
H→ Na
+
+ CO3H
-
(PM: 84) 1mol = 2osmoles =1Eq =84gr
Fructosa: (PM: 180) 1mol = 1osmol = 180gr
Aplicación:
Calcular la Osm, N y M de 5g de NaCl disueltos en 250 ml de solución.
Datos del problema:
V: 250ml QNaCl: 5g PMNaCl: 58,5 Osm: incógnita
Solución del problema:
58,5g ______ 2 osmoles de NaCl
5g _______ x osmoles de NaCl
x = 0,172osmoles NaCl
Como los 5g que equivalen al peso de 0,172osmoles están en 250ml, entonces:
0,172osmoles NaCl ______ 250ml
x osmoles NaCl _________ 1000ml
x = 0,688osmoles de NaCl en 1000ml de solución
Conociendo la relación entre las distintas formas de expresar la cantidad de soluto, nos queda por hallar la N
y M de la solución:
58,5gr = 1mol NaCl = 1eq = 2osmoles por lo tanto en nuestro caso
20g = 0,344moles = 0,344eq = 0,688osmoles en 1000ml
Respuesta: Osm: 0,688 ó 0,688 osmoles de NaCl en 1 litro de solución.
N: 0,344 ó 0,344eq de NaCl en 1 litro de solución
M: 0,344 ó 0,344moles de NaCl en 1 litro de solución.
4- DILUCIÓN
El proceso de dilución consiste en el agregado de solvente a una solución, es decir en el incremento del vo-
lumen de la solución, para disminuir la concentración de dicha solución. Por ejemplo: diluimos el jugo concen-
trado porque nos resulta muy dulce, agregamos más agua para que una pintura sea más fácil de aplicar sobre
una supercie. Por lo tanto el volumen y la concentración cambian mientras la cantidad de soluto permanece
constante.
99

Guía de Aprendizaje - Crecimiento y Desarrollo - 1-9
Aplicación:
Ejemplo 1: En un vaso de precipitado se tienen 200 ml de una solución 0,1M y se le agregan 800ml de H
2
O.
¿Cuál será la concentración nal?
Datos del problema:
V
inicial
: 200ml C
inicial
: 0,1M
V
nal
: 200ml de solución inicial + 800ml H2O
C
nal
: incógnita
Solución del problema:
0,1mol ______ 1000ml
x mol ______ 200ml
x = 0,02moles ______ 200ml solución
+ 800ml H2O
_____________________________________________________
0,02 moles 1000ml solución nal
Respuesta: 0,02 M
Conclusión: el agregado de 800ml de H2O a los 200ml de solución 0,1M produjo un aumento del volumen
(1000ml), una disminución de la concentración (0,02) manteniendo la cantidad de soluto (Q = 0,02 moles)
Ejemplo 2: A partir de 1000ml de solución 2M, preparar 200ml de una solución 0,5M
Datos del problema:
V
inicial
: 1000ml C
inicial
: 2M V
nal
: 200ml C
nal
: 0,5M
Solución:
I) encontrar la cantidad de soluto necesaria para preparar 200ml (V
nal
) con una concentración de 0,5M (C
nal
)
0,5moles ________ 1000ml
x moles ________ 200ml
0,1 moles
II) determinar que volumen de la solución original 2M (C
inicial
) contiene los 0,1 moles
2moles ________ 1000ml
0,1moles _______ x ml
50ml de la solución original
Respuesta: para preparar el volumen de solución pedido se procederá:
50ml de la solución original + 150ml de agua
Conclusión: De la solución más concentrada (2M) se toman 50ml que contienen 0,1mol, cantidad de soluto
necesaria para preparar 200ml con una concentración nal de 0,5M. Luego se le agregan 150ml de agua para
llegar a tener 200ml con la concentración requerida (0,5M).
100

Referencias bibliográficas
GRIGERA R.J.: “Elementos de Biofísica”. Ed. Hemisferio Sur S.A., 1980.
FRUMENTO A.: “Biofísica”. Ed. Interamericana.
JIMÉNEZ-VARGAS: “Fisicoquímica – Fisiológica”.
RODRIGUEZ GUARNIZO J. – RODRIGUEZ BARRANTES D. Reexiones didácticas sobre los estados de
agregación de la materia
Guía de autoaprendizaje:
1.- La fase dispersa de una solución no sedimenta espontáneamente y es solo separada por una membrana
dialítica o por ultracentrifugación. Se trata de una dispersión:
a) coloidal
b) verdadera
c) grosera
2.- Cuántas fases distintas pueden reconocerse en cada caso:
a) un balde de agua con arena y trozos de madera
b) un vaso de agua con 5 cubos de hielo
c) una taza con café y 10 cucharadas de azúcar
d) una olla con agua y 5 verduras distintas
3.- El plasma y el suero de acuerdo a sus características, se clasican como:
a) verdaderas
b) coloidales
c) groseras
4.- Son formas diferentes de expresar la cantidad de soluto:
a) milímetro
b) g, mg
c) mol, equivalente químico
d) osmol, g
e) ml
5.- La masa de sustancia que contiene el número de Avogadro de moléculas es:
a) el peso atómico expresada en g
b) el peso molecular expresado en g
c) la valencia
d) el número de partículas
101

Guía de Aprendizaje - Crecimiento y Desarrollo - 1-9
Respuestas:
1.- a
2.- a) 3
b) 2
c) 2
d) 6
3.- b
4.- b, c, d
5.- b
102

FÍSICA BIOLÓGICA
SEMINARIO DISCIPLINAR:
SOLUCIONES. FORMAS DE EXPRESAR SU CON-
CENTRACIÓN
Docente Responsable: Carlos J Dabin. JTP. Cát. De Física Biológica
INTRODUCCIÓN
Nuestro cuerpo, cuyo principal componente es el agua, está organizado en compartimentos que tienen distin-
ta composición y se hallan separados por membranas. El intercambio de agua y solutos entre los compartimen-
tos mantiene la composición de las soluciones acuosas intra y extracelulares de acuerdo a sus requerimientos
siológicos. Para comprender la composición y la homeostasis del medio interno, debemos comenzar con
el estudio de “qué es una dispersión” y las distintas formas de expresar la concentración de los solutos que
componen al medio interno.
Por otra parte, la preparación y el uso de soluciones son temas cotidianos dentro de la Práctica Médica: en
promoción, terapéutica, diagnóstico, prescripción, etc.
OBJETIVOS
• Conceptuar las distintas formas de expresar la concentración de una solución y la cantidad de soluto
disuelto.
• Saber interconvertir entre sí las distintas formas de expresar la concentración y la cantidad de soluto de
las soluciones.
• Comprender el concepto de dilución y su aplicación en la práctica médica
• Interpretar a qué tipo de dispersión corresponde cada uno de los líquidos biológicos.
CONTENIDOS
Dispersiones: concepto y clasicación.
Formas de expresar la cantidad de soluto y la concentración de una solución.
Proceso de dilución
DURACIÓN: 2 horas.
Los alumnos DEBEN concurrir al seminario propuesto con la lectura previa del Material Académico aportado
por la Cátedra de Física Biológica.
DESARROLLO
1- Indique qué tipo de dispersión constituyen los siguientes ejemplos. Justique.
• Líquido cefalorraquídeo (agua, glucosa, aminoácidos, hormonas, vitaminas, electrolitos, células)
• Secreción pancreática (agua, bicarbonato, enzimas proteolíticas y lipolíticas, amilasa)
• Bilis (sales biliares, proteínas, colesterol, hormonas y agua)
• Líquido intersticial (agua, aminoácidos, azúcares, ácidos grasos, coenzimas, hormonas, neurotransmiso-
res, sales minerales y productos de desecho de las células).
103

Guía de Aprendizaje - Crecimiento y Desarrollo - 1-9
2- La concentración de una sustancia puede expresarse de distintas maneras. Indique para las siguientes, cuál
considera es la forma más adecuada de expresar su concentración:
a- Na+
b- K+
c- Glucosa
d- Proteínas
e- Todas las sustancias del plasma tomadas en conjunto
3- Un recipiente contiene 100ml de una solución de ClNa (cloruro de sodio) 9gr‰ (llamada solución o suero
siológico - SF) (NaCl → Na+ + Cl-. PM: 58,5). Si se divide el contenido en dos recipientes: uno que contiene
70ml y otro que contiene los 30ml restantes:
a- Indique que propiedades intensivas y extensivas se han modicado en cada vaso.
b- ¿Cuántos grs de ClNa habrá en cada uno de los recipientes?
c- ¿Cuál será la concentración de la solución que contiene cada uno expresada en moles/l, en meq/l y en
osm/l?
4- ¿Cuántos gramos de soluto se requieren para preparar 1.000 cm3 de las siguientes soluciones?:
a- KCl 2M (KCl → K+ + Cl-, cloruro de potasio, PM: 74,5)
b.- CaCl2 0, 03M (CaCl2 → Ca++ + 2 Cl-, cloruro de calcio, PM: 111)
5- Una solución de MgCl2 (MgCl2 → Mg++ + 2 Cl-, cloruro de magnesio, PM: 95) es 15M. ¿Cómo debe pro-
cederse para preparar 100ml de solución 3M?
6- Para poder ser consumida por lactantes, la leche de vaca debe ser diluida. Teniendo en cuenta los datos de
la siguiente tabla, calcule:
a- ¿qué volumen de la leche de vaca se debe tomar?
b- ¿cuánta agua debe agregarse para preparar un litro de leche apta para la alimentación de un lactante?
Sodio (mg/100 ml) Potasio (mg/100 ml)
Leche materna 15 53
Leche de vaca 45 159
104

TRANSPORTE A TRAVES DE LA MEMBRANA CE-
LULAR
Autores: Dra Leda Urli, Dra María Isabel Spengler. Cátedra de Física Biológica.
Los tejidos animales están constituidos por células rodeadas por una solución que las baña: el uido inters-
ticial.
Las células vivientes, tienen la habilidad de mantener muchas sustancias en concentraciones interiores dife-
rentes de las concentraciones exteriores.
El movimiento de moléculas a través de las membranas biológicas es vital para la mayoría de los procesos
celulares. Algunas moléculas se mueven a través de las membranas biológicas simplemente mediante difusión
entre las moléculas que constituyen la membrana, mientras que el paso de otras moléculas implica la inter-
vención de proteínas transportadoras especícas en la membrana. El oxígeno, por ejemplo, es una pequeña
molécula bastante soluble en disolventes no polares. Atraviesa las membranas biológicas mediante difusión a
través de la membrana.
Flujo
Denimos Flujo (J) como la cantidad de sustancia que atraviesa la membrana, por unidad de supercie per-
pendicular al ujo y por unidad de tiempo. Unidades:
J = moles
cm
2
seg
En la célula existen ujos unidireccionales de la sustancia que atraviesa la membrana: del interior al exterior
y del exterior al interior. El desplazamiento neto de esa sustancia o ujo neto de la misma es la diferencia
entre ellos e indica el sentido neto de movimiento de la sustancia en cuestión.
Difusión. Ley de Fick
La difusión es el proceso por el cual los átomos o las moléculas se entremezclan debido a un movimiento
térmico aleatorio llamado movimiento browniano. Si las propiedades de la disolución son iguales en todo su
volumen, la translación de cada partícula en cada dirección del espacio será igualmente probable. En con-
secuencia, el “desplazamiento neto” de las moléculas será nulo. Si hay diferencias de concentración, las
partículas tendrán una tendencia a desplazarse desde la zona de mayor concentración hacia las de menor
concentración. Por otro lado, si hay diferencia de potencial eléctrico las partículas cargadas tendrán una ten-
dencia determinada por la carga de la partícula y el sentido del campo eléctrico. Lo mismo podríamos decir si
existe una diferencia de presión hidrostática .El desplazamiento neto de las partículas dependerá del balance
entre las tres tendencias.
Consideremos ahora dos disoluciones de concentración y/o potencial eléctrico y/o presión hidrostática di-
ferentes separadas por una membrana. Cada solución es homogénea, pero la membrana interpuesta estará
atravesada por una diferencia de concentración y/o potencial eléctrico y/o presión hidrostática. Las partículas
de soluto que penetren en la membrana, en su movimiento al azar, resultarán dirigidas por ese gradiente y atra-
vesarán la membrana en el sentido de anular las diferencias. Este fenómeno, en virtud del cual las partículas
disueltas atraviesan la membrana, se denomina difusión simple.
La ley de Fick aplicada a la difusión de una sustancia en solución a través de la membrana dice que: “la can-
tidad de sustancia que atraviesa un cm2 de área seccional por segundo (el ujo), es directamente proporcional
a la diferencia de concentración de la sustancia”.
La ley de Fick se enuncia como:
J=P.ΔC
105
Este documento contiene más páginas...
Descargar Completo
3- Biofisica 2017-1.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.