REGULACIÓN DE LA EXPRESIÓN GÉNICA
EN PROCARIONTES
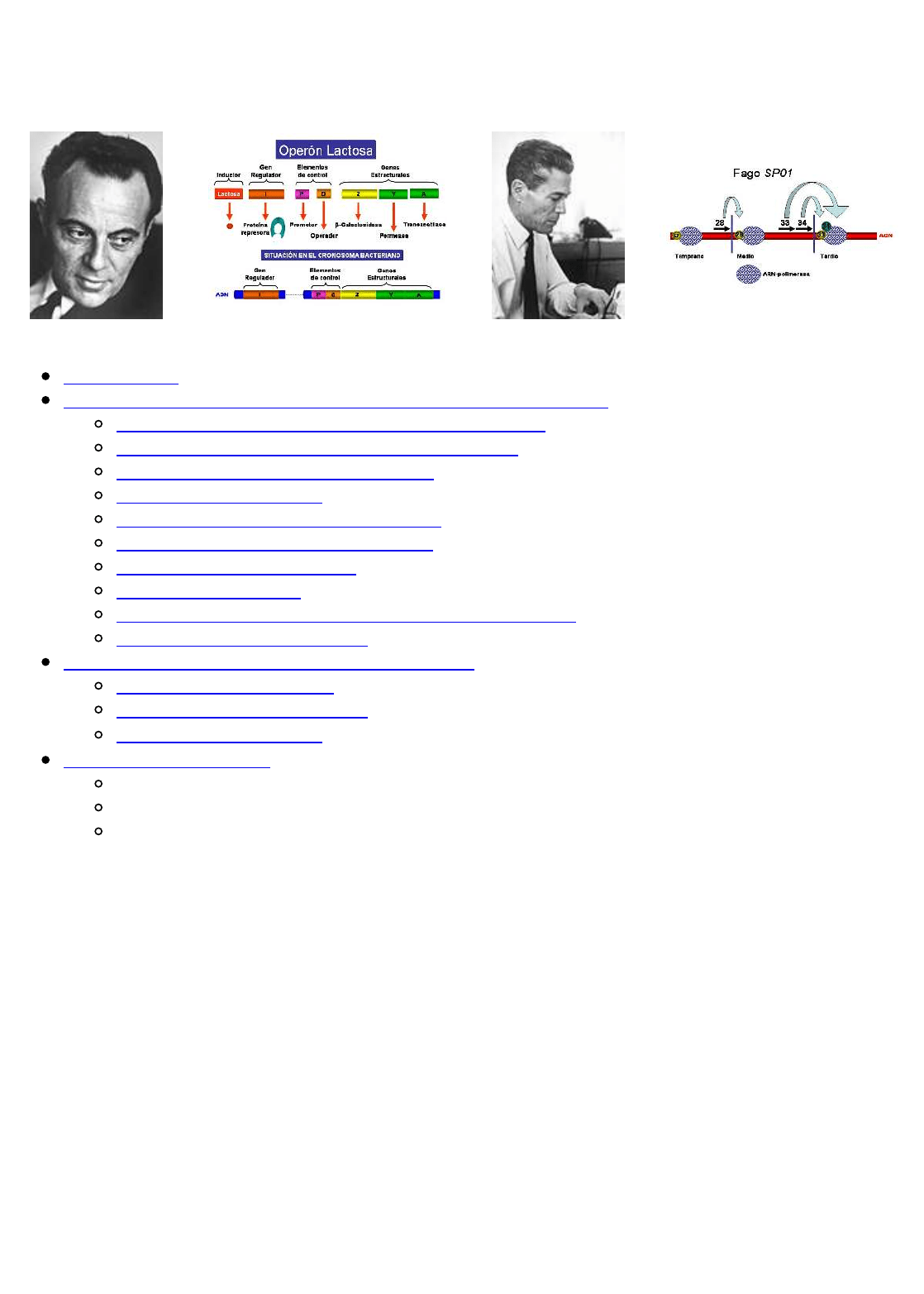
Francois Jacob Elementos Operón Lactosa Jacques Monod Regulación fago SP01
Introducción
Regulación de la expresión génica en bacterias: el operón
Sistemas constitutivos y sistemas adaptativos
Sistemas inducibles y sistemas represibles
Control positivo y control negativo
Elementos del operón
El operón lactosa: control negativo
El operón lactosa: control positivo
Represión por catabolitos
El operón triptófano
El operón triptófano: regulación por el atenuador.
Interacción entre operones
Regulación de la expresión génica en fagos
Regulación del fago T7
Regulación del Fago SP01
Regulación del Fago l
Morfogénesis en virus
Fago T4
Fago Ø29
Virus del mosaico del tabaco TMV
INTRODUCCIÓN
En nuestro recorrido por la Genética hemos averiguado que son los genes, cómo se replican y
cómo se transmiten. También hemos visto que la información contenida en los genes se
transcribe a ARN y que el ARN mensajero se traduce a proteínas. De manera que la
información contenida en los genes se convierte en proteínas. Sin embargo, aún no hemos
visto de qué manera la célula regula su funcionamiento, es decir, ¿Cómo decide la célula que
proteínas necesita producir en cada momento y qué cantidad de proteína es necesario
sintetizar?.
En los organismos pluricelulares con diferentes órganos y tejidos está claro que existe un
reparto de las funciones, de manera que las células de diferentes tejidos llevan a cabo distintas
misiones y para ello necesitan sintetizar diferentes tipos de proteínas. De forma que un
hepatocito (célula del hígado) produce una colección de proteínas diferentes a las de un
reticulocito. Por consiguiente, en los diferentes tejidos de un individuo pluricelular adulto, se
están expresando distintas baterías de genes.

REGULACIÓN DE LA EXPRESIÓN GÉNICA EN BACTERIAS
En las bacterias, a pesar de ser organismos unicelulares, también es necesario regular la
expresión de los genes adaptándola a las necesidades ambientales. Es un principio de
economía celular el que la expresión de los genes este regulada según las circunstancias
celulares. Un buen ejemplo de esta situación en bacterias es la regulación de las enzimas
implicadas en el metabolismo de los azúcares. Las bacterias pueden emplear para obtener
energía distintas fuentes de carbono, como la glucosa, lactosa, galactosa, maltosa, ramnosa y
xilosa. Existen enzimas capaces de introducir cada uno de estos azúcares en la bacteria y
enzimas capaces de romperlos para obtener energía. Lógicamente, sería un despilfarro
energético producir simultáneamente todos los enzimas necesarios para metabolizar los
diferentes azúcares mencionados. Por consiguiente, sería mucho más económico para la célula
producir solamente las enzimas necesarias en cada momento, es decir, si en el medio en el que
vive la bacteria la principal fuente de carbono es la lactosa, solamente se expresarían los genes
necesarios para metabolizar la lactosa, mientras que los otros genes no se expresarían. Por
tanto, es esencial que exista un mecanismo de regulación de la expresión génica, de manera
que los genes se expresen cuando sea necesario.
La regulación de la producción de proteínas (síntesis de proteínas) considerando el proceso en
su conjunto, puede llevarse a cabo en tres niveles:
Replicación
Transcripción
Traducción.
De los tres niveles de regulación, uno de los mejor conocidos actualmente es la regulación
durante la transcripción. Aunque la regulación de la transcripción en eucariontes es más
compleja que en bacterias, muchos de sus aspectos son similares. Por tanto, comenzaremos
por el estudio de la regulación de la transcripción en bacterias.
SISTEMAS CONSTITUTIVOS Y SISTEMAS ADAPTATIVOS
Es evidente que existen algunos procesos metabólicos que son necesarios para el
funcionamiento normal de casi todas las células, de manera que existen una serie de
necesidades básicas para el mantenimiento normal de una célula. Por consiguiente, los genes
que codifican para las enzimas necesarias para el metabolismo básico celular se están
expresando continuamente, es decir, se expresan de forma constitutiva o continua. Por tal
motivo, a este tipo de genes se les denomina, "genes que guardan la casa" o genes
constitutivos. Estos genes que se están expresando continuamente no significa que su
actividad no esté regulada, simplemente están sometidos a un tipo de regulación diferente que
hace que se estén expresando siempre. Los genes constitutivos codifican para sistemas
enzimáticos constitutivos, que se necesitan siempre para la actividad normal de la célula.
Frente a los genes constitutivos, nos encontramos con los genes que se expresan solamente
en determinadas situaciones y que, por consiguiente, codifican para enzimas que solamente se
necesitan en momentos concretos. A este tipo de genes se les llama genes adaptativos y a las
enzimas codificadas por ellos, sistemas enzimáticos adaptativos. Se denominan así

pensando en que se expresan cuando la célula se adapta a una determinada situación
ambiental. En algunos libros de texto se denomina a este tipo de genes, genes regulados, sin
embargo, esta nomenclatura no es demasiado buena, ya que parece que los únicos genes cuya
expresión está regulada serían estos.
SISTEMAS INDUCIBLES Y SISTEMAS REPRESIBLES
Sistemas inducibles: cuando el sustrato sobre el que va actuar la enzima provoca la síntesis
del enzima. Al efecto del sustrato se le denomina inducción positiva. Por ejemplo, en E. coli
en ausencia de galactósido (sustrato) hay de una diez unidades de galactosidasa (enzima) por
miligramo de materia seca, mientras que en presencia de galactósido se detectan hasta 10.000
unidades de galactosidasa por miligramo de materia seca. Al compuesto que desencadena la
síntesis del enzima se le denomina Inductor.
Sistemas represibles: cuando el producto final de la reacción que cataliza el enzima impide la
síntesis de la misma. Este fenómeno recibe el nombre de inducción negativa. Al compuesto
que impide la síntesis del enzima se le denomina correpresor.
Los sistemas inducibles se corresponden a procesos catabólicos de degradación, por ejemplo,
el operón lactosa, el operón arabinosa, el operón maltosa. Se trata de sistemas enzimáticos
encargados de degradar la lactosa, arabinosa, maltosa, etc.
Los sistemas represibles se corresponden con procesos síntesis o Anabolismo, por ejemplo el
operón triptófano y el operón histina. Se trata de las rutas metabólicas que conducen a la
síntesis de triptófano y síntesis de histidina.
CONTROL POSITIVO Y CONTROL NEGATIVO
Control positivo: Se dice que un sistema está bajo control positivo cuando el producto del gen
regulador activa la expresión de los genes, actúa como un activador.
Control negativo: se dice que un sistema está bajo control negativo cuando el producto del
gen regulador reprime o impide la expresión de los genes, actúa como un represor.
ELEMENTOS DEL OPERÓN
Jacob, Monod y colaboradores analizaron el sistema de la lactosa en E. coli, de manera que los
resultados de sus estudios permitieron establecer el modelo genético del Operón que permite
comprender como tiene lugar la regulación de la expresión génica en bacterias. Jacob y Monod
recibieron en 1965 el Premio Nobel pos estas investigaciones.

Francois Jacob Jacques Monod
Un Operón es grupo de genes estructurales cuya expresión está regulada por los mismos
elementos de control (promotor y operador) y genes reguladores.
Los principales elementos que constituyen un operón son los siguientes:
Los genes estructurales: llevan información para polipéptidos. Se trata de los genes
cuya expresión está regulada. Los operones bacterianos suelen contener varios genes
estructurales, son poligénicos o policistrónicos. Hay algunos operones bacterianos que
tienen un solo gene estructural. Los operones eucarióticos suelen contener un sólo gen
estructural siendo monocistrónicos.
El promotor (P): se trata de un elemento de control que es una región del ADN con una
secuencia que es reconocida por la ARN polimerasa para comenzar la transcripción. Se
encuentra inmediatamente antes de los genes estructurales. Abreviadamente se le
designa por la letra P.
El operador (O): se trata de otro elemento de control que es una región del ADN con una
secuencia que es reconocida por la proteína reguladora. El operador se sitúa entre la
región promotora y los genes estructurales. Abreviadamente se le designa por la letra O.
El gen regulador (i): secuencia de ADN que codifica para la proteína reguladora que
reconoce la secuencia de la región del operador. El gen regulador está cerca de los genes
estructurales del operón pero no está inmediatamente al lado. Abreviadamente se le
denomina gen i.
Proteína reguladora: proteína codificada por el gen regulador. Está proteína se une a la
región del operador.
Inductor: sustrato o compuesto cuya presencia induce la expresión de los genes.
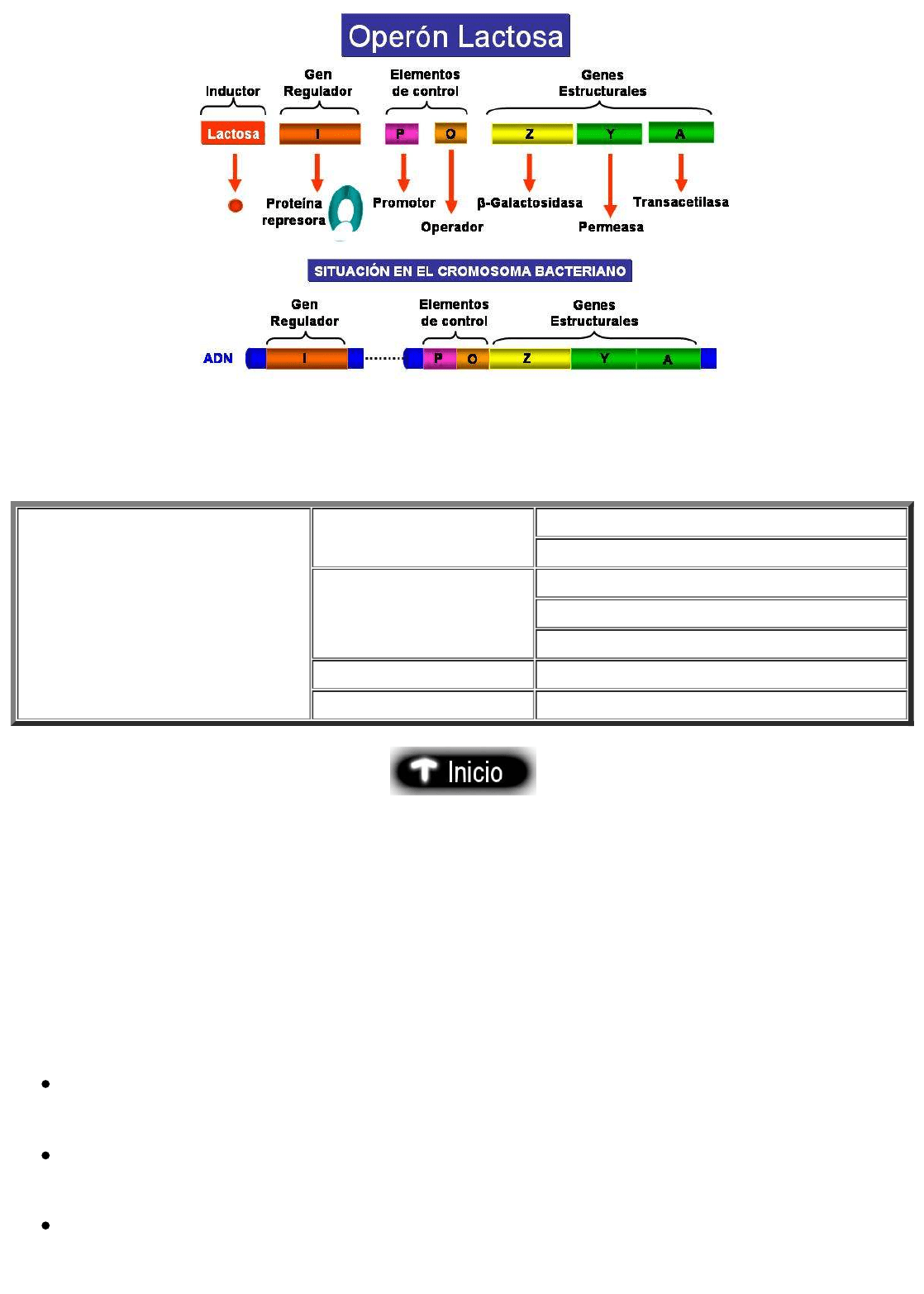
Elementos del operón lactosa
Elementos que intervienen
en la regulación de la
expresión génica en
bacterias. Elementos del
Operón.
Elementos de control
Promotor
Operador
Moléculas difusibles
Proteínas reguladoras
Efectores
Inductores
Genes Estructurales Codifican para polipéptidos
Gen regulador Codifica para proteína reguladora
EL OPERÓN LACTOSA: CONTROL NEGATIVO
El Operón lactosa, que abreviadamente se denomina Operón lac, es un sistema inducible que
está bajo control negativo, de manera que la proteína reguladora, producto del gen regulador i,
es un represor que impide la expresión de los genes estructurales en ausencia del inductor. El
inductor del sistema es la lactosa. Como veremos más adelante, el operón lac también está
bajo control positivo, ya que existe otra proteína que estimula la transcripción de los genes
estructurales.
Los genes estructurales del operón lactosa son los siguientes:
El gen z+: codifica para la
b
-galactosidasa que cataliza la hidrolisis de la lactosa en
glucosa más galactosa.
El gen y+: codifica para la galactósido permeasa que transporta b-galactósidos al
interior de la célula bacteriana.
El gen a+: codifica para la tiogalactósido transacetilasa que cataliza la transferencia del
grupo acetil del acetil Coenzima A al 6-OH de un aceptor tiogalatósido. Este gen no está
relacionado con el metabolismo de la lactosa.
El verdadero inductor del sistema es la Alolactosa y no la lactosa de manera que la β-
galactosidasa transforma la lactosa en Alolactosa. En los estudios del operón lactosa se
utiliza como inductor un análogo sintético de la lactosa que es el Isopropil tiogalactósido
(IPTG). El IPTG no necesita ser transportado por la galactósido permeasa para entrar en la
bacteria.
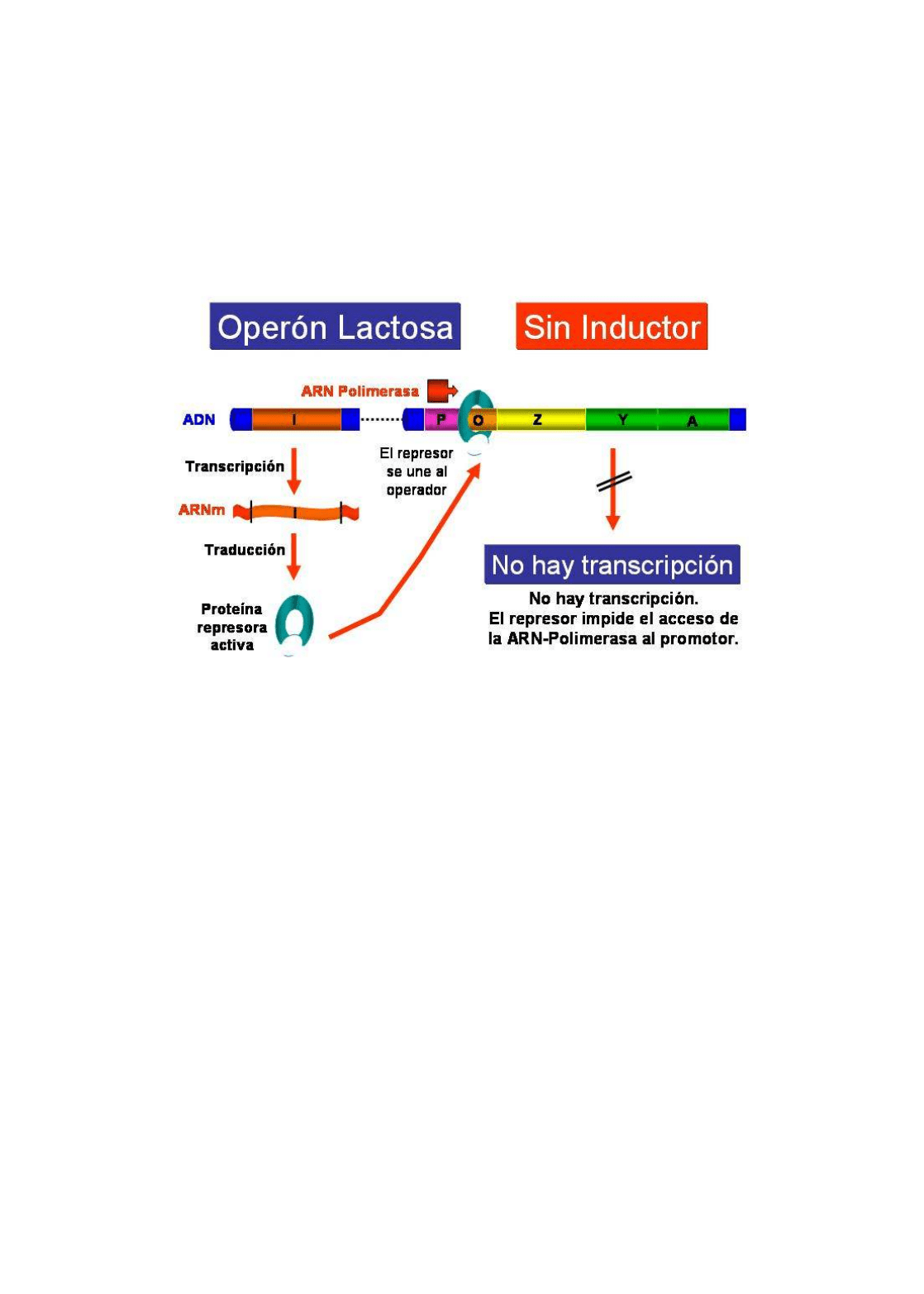
Las cepas normales de E. coli son inducibles, de manera que en ausencia del inductor (la
lactosa), la proteína represora producto del gen i se encuentra unida a la región operadora e
impide la unión de la ARN-polimerasa a la región promotora y, como consecuencia, no se
transcriben los genes estructurales.
Operón lactosa en ausencia de lactosa
Sin embargo, en presencia del inductor (la lactosa), este se une a la proteína reguladora que
cambia su conformación y se suelta de la región operadora dejando acceso libre a la ARN-
polimerasa para que se una a la región promotora y se transcriban los genes estructurales. Por
consiguiente, la presencia del inductor hace que se expresen los genes estructurales del
operón, necesarios para metabolizar la lactosa.
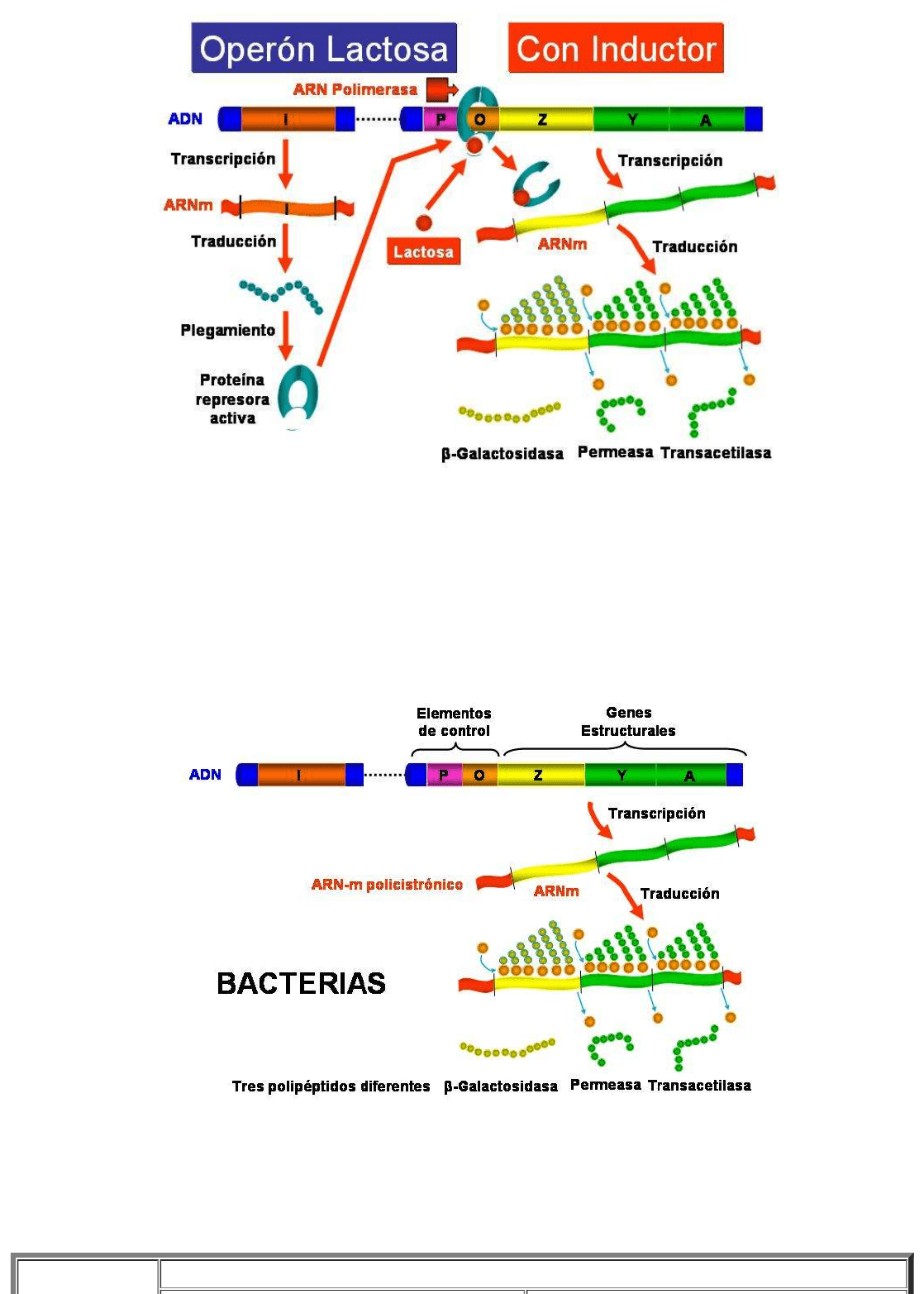
Operón lactosa en presencia de lactosa
También es conveniente recordar que los tres genes estructurales del operón lactosa se
transcriben juntos en un mismo ARNm, es decir que los ARN mensajeros de bacterias suelen
ser policistrónicos, poligénicos o multigénicos. Sin embargo, en eucariontes los mensajreos
suelen sen monocistrónicos o monogénicos, es decir, corresponden a la transcripción de un
solo gen estructural.
Operón lactosa: ARNm multigénico o policistrónico
En la siguiente tabla se muestra la expresión de los genes del operón lactosa en ausencia y en
presencia del inductor (lactosa) en una bacteria normal i
+
p o z
+
y
+
a
+
. SI = significa que se
expresan, NO = significa que no se expresan.
Bacteria Expresión de los genes estructurales del Operón lactosa
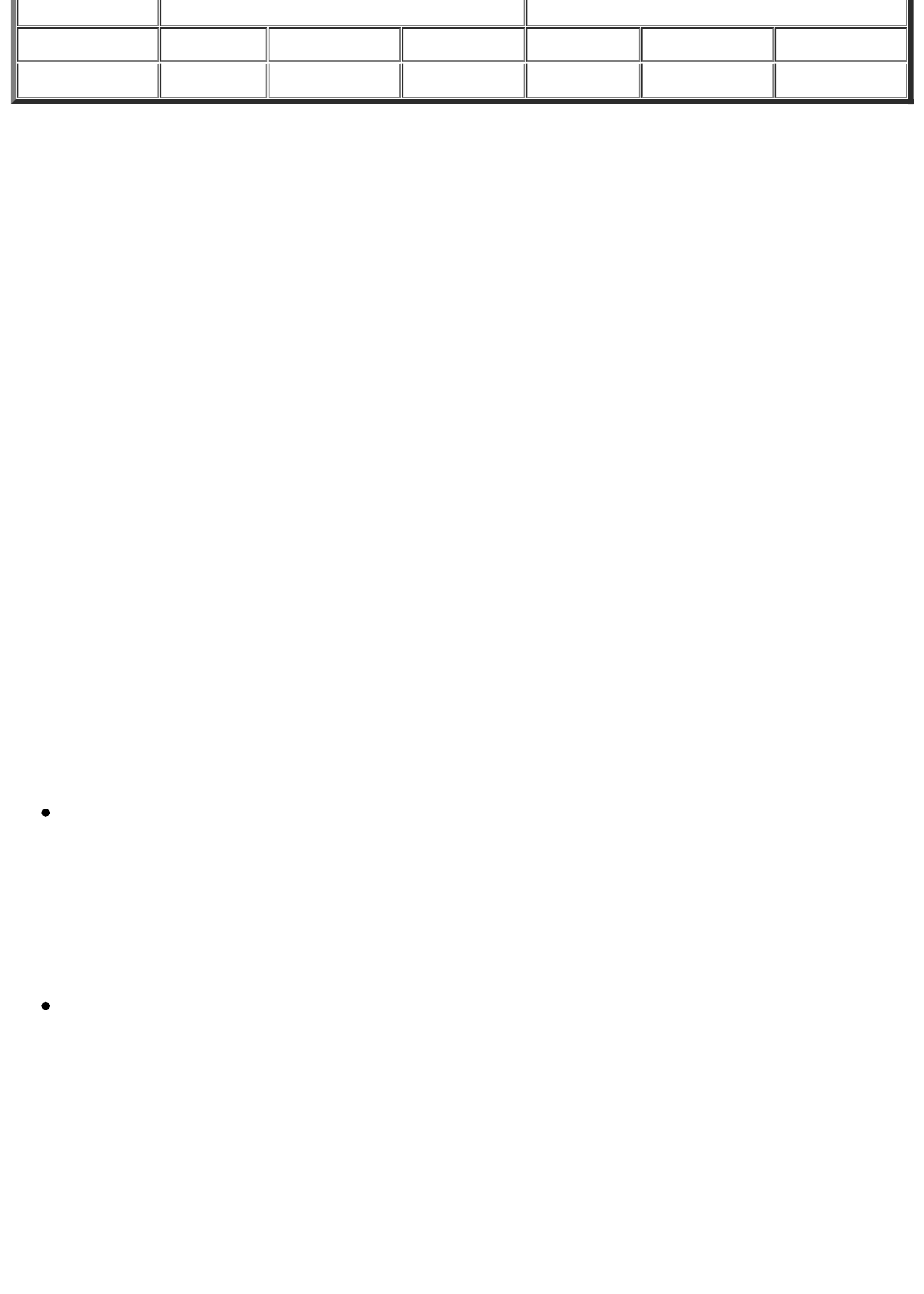
normal Ausencia de inductor (Sin lactosa) Presencia de inductor (Con lactosa)
Genotipo
z
+
y
+
a
+
z
+
y
+
a
+
i
+
p o z
+
y
+
a
+
NO NO NO SI SI SI
El conocimiento profundo del funcionamiento del operón lactosa se obtuvo gracias a la
obtención de mutantes que afectaban a los genes estructurales, a los elementos de control
(promotor y operador) y al gen regulador. Además, también fue muy importante el estudio del
operón lactosa en bacterias diploides parciales o merocigotos.
Bacteria diploide parcial o merocigoto: bacteria que tiene parte de sus genes en dos dosis.
Lo habitual en las bacterias es que los genes estén en una sola dosis, ya que se trata de
individuos haploides. Sin embargo, a veces es posible mediante conjugación entre una bacteria
donadora F
+
y una receptora F
-
, obtener bacterias descendientes diploides parciales o
merocigotos. Sin embargo, estos diploides parciales son inestables. Por tal motivo, fue muy
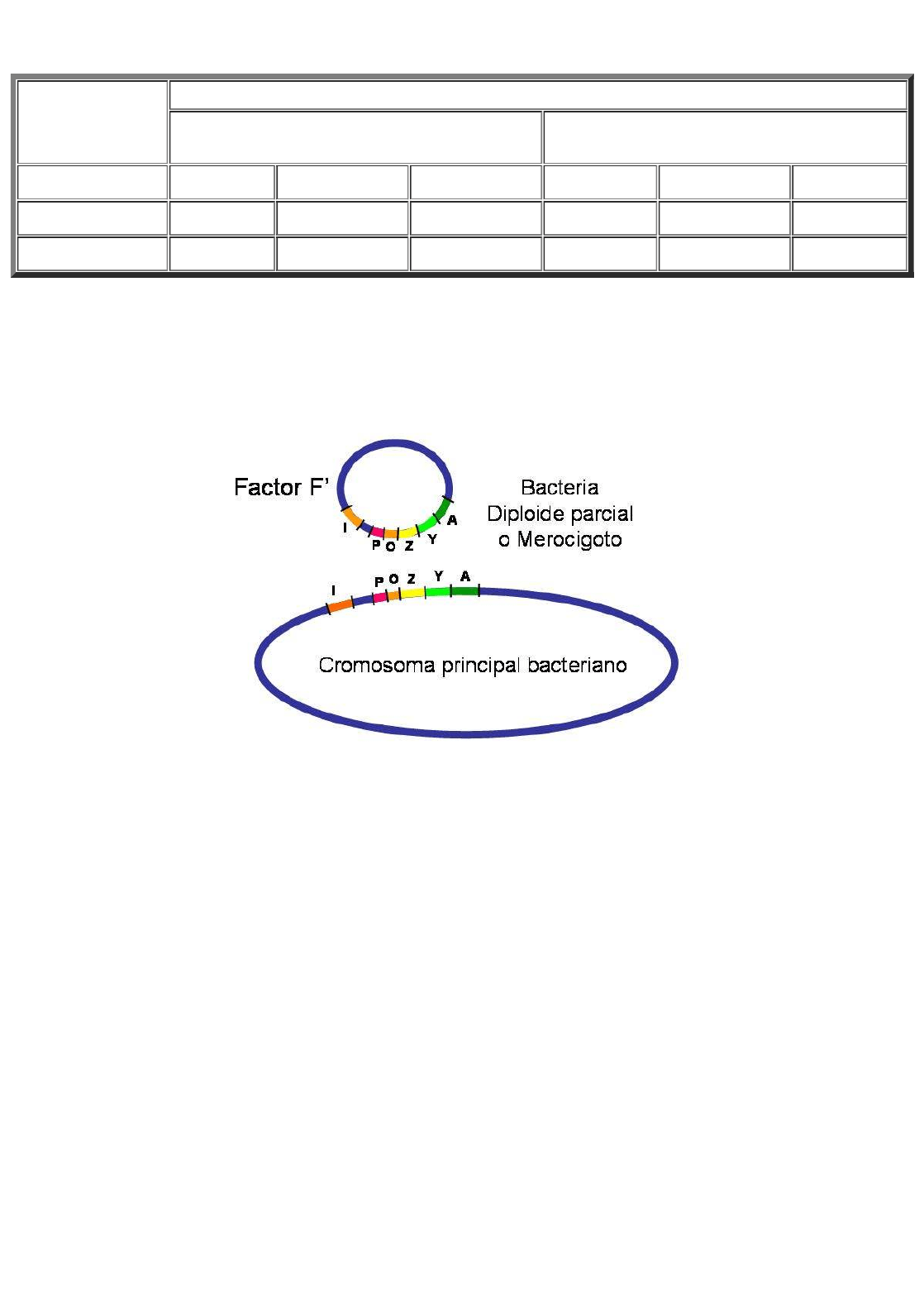
importante el descubrimiento de bacterias F' que tienen en el factor sexual (plasmidio) parte del
cromosoma principal bacteriano. En el caso del estudio del operón lactosa, se consiguieron
factores F' que tenían incorporado exclusivamente los genes del operón lactosa. De esta forma,
una bactería con un factor F' de estas características tiene dos veces los genes del operón
lactosa, una en el cromosoma principal y otra en el factor F'.
Los primeros mutantes fueron aislados por Lederberg y colaboradores y afectaban a los genes
estructurales (z, y, a). Se dedujo que los estos genes estaban juntos y en el orden z-y-a. Los
mutantes en estos genes se denominan z
-
, y
-
e a
-
y ,dan lugar a alteraciones en la estructura de
las enzimas codificadas por estos genes.
Jacob y Monod aislaron bacterias mutantes i
-
y O
C
que afectan al gen regulador (i) que lleva
información para la proteína reguladora y a la región operadora (O), respectivamente. Ambos
son mutantes de tipo constitutivo.
Mutantes constitutivos: son aquellos en los que siempre se expresan o transcriben los genes
del operón lactosa, independientemente de si está o no está presente el inductor.
La mutación constitutiva i
-
altera la estructura de la proteína reguladora o proteína
represora de manera que ya no es capaz de unirse a la región operadora. Por tanto, esta
alteración afecta a la región de la proteína represora encargada de unirse al operador. Al
no poder unirse la proteína represora al operador, la región promotora queda asequible
para la ARN polimerasa y se produce la transcripción de los genes estructurales en
ausencia de inductor (lactosa). La proteína represora es un tetrámero (cuatro cadenas
polipeptídicas idénticas).
La mutación constitutiva en el operador (O
C
), consiste en una alteración en la
secuencia de bases nitrogenadas de la región del Operador que tienen como
consecuencia que la proteína reguladora producto del gen i ya no sea capaz de unirse al
operador. Al no poder unirse la proteína represora al operador, la región promotora queda
asequible para la ARN polimerasa y se produce la transcripción de los genes estructurales
en ausencia de inductor (lactosa). El estudio de diferentes mutantes del operador ha
permitido determinar que el operador es una región de 17 a 25 nucleótidos situada justo
antes del gen z y después del promotor. Esta región muestra una enorme especificidad
por la proteína represora.
Es importante destacar que tanto la mutación i- como la O
C
actúan simultáneamente sobre los
tres genes estructurales del operón lactosa. En la siguiente tabla se indica la expresión de los
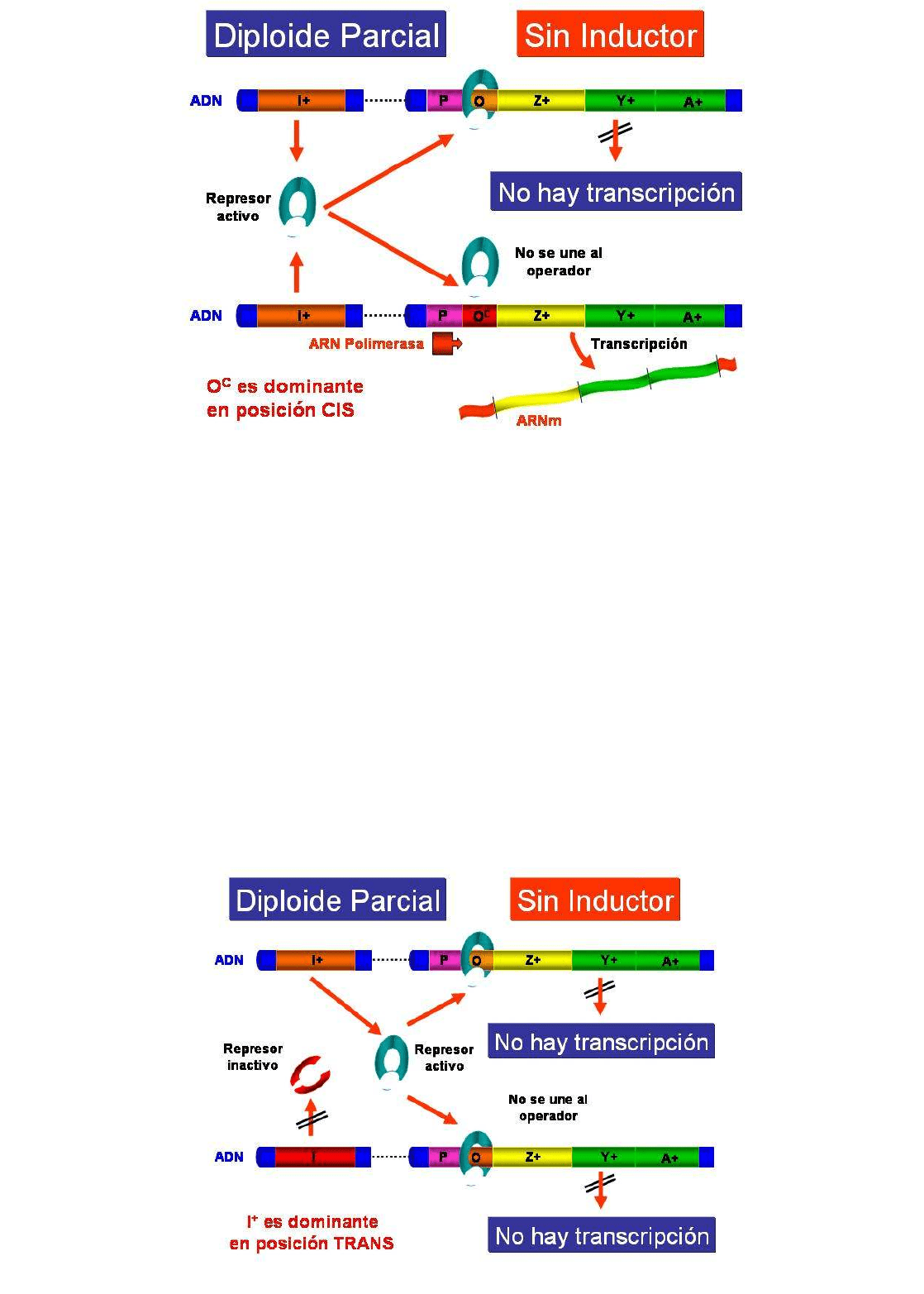
genes del operón lactosa en los dos mutantes constitutivos estudiados, en el regulador
constitutivo (i- ) y en el operador constitutivo (O
C
).
Mutantes
constitutivos
Expresión de los genes estructurales del Operón lactosa
Ausencia de inductor (Sin lactosa)
Presencia de inductor (Con
lactosa)
Genotipo
z
+
y
+
a
+
z
+
y
+
a
+
i
-
P O
C
z
+
y
+
a
+
SI SI SI SI SI SI
i
+
P O
z
+
y
+
a
+
SI SI SI SI SI SI
También es importante conocer lo que sucede en los diploides parciales o merocigotos que
contienen una región operadora normal y una región operadora mutante constitutiva, es decir,
bacterias diploides parciales O/O
C
.
Diploide parcial: operón lactosa
En estos diploides parciales, se ha comprobado que el operador constitutivo es dominante en
posición CIS, es decir, ejerce su efecto solamente sobre los genes estructurales que están en
su misma molécula de ADN que la mutación del operador, pero no actúa sobre los genes
estructurales de otra molécula de ADN. Esto significa que el operador es una secuencia de
bases en el ADN que no codifica para ninguna molécula difusible. En el siguiente diploide
parcial i
+
P O z
+
y
+
a
+
/ i
+
P O
C
z
+
y
+
a
+
tanto en ausencia como en presencia de lactosa se
produce la expresión de los tres genes estructurales del operón. Esto se debe a que los genes
estructurales que están en la misma molécula de ADN que la mutación constitutiva O
C
se van a
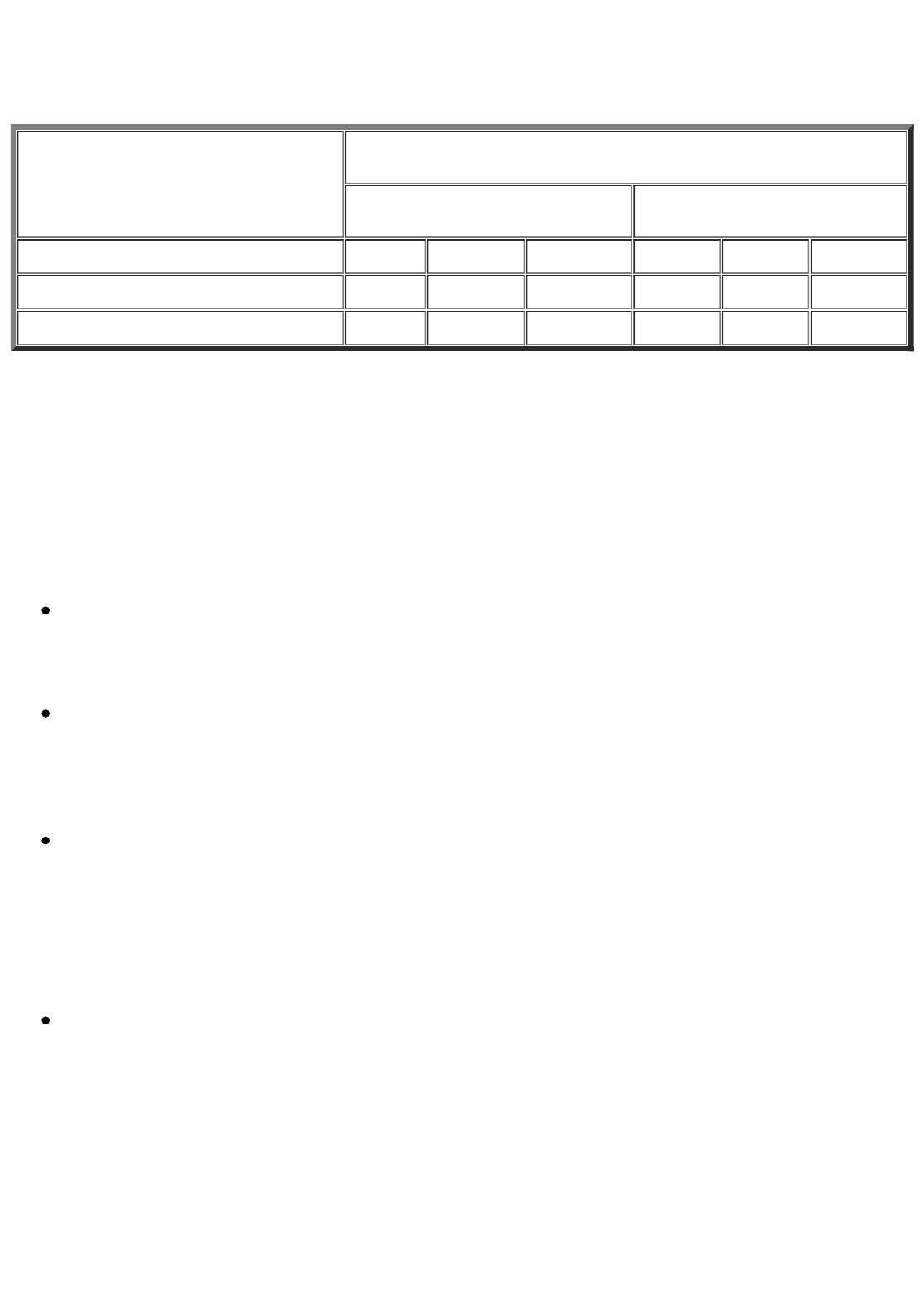
expresar siempre. En el siguiente esquema se indica lo que sucede en un diploide parcial O/O
C
en ausencia de inductor.
Diploide parcial O/O
C
: Sin Inductor (lactosa)
En el siguiente esquema se indica lo que sucede en un diploide parcial O/O
C
en presencia de
inductor.
Sin embargo, en los diploides parciales con un gen regulador normal y un gen regulador
mutante constitutivo, es decir, en baterias diploides parciales i
+
/i
-
, el gen regulador normal i
+
es
dominante en posición TRANS, es decir, ejerce su efecto sobre los genes estructurales de la
misma molécula de ADN en que está la mutación del gen regulador y también sobre los genes
estructurales de otra molécula de ADN diferente. Por tanto, el gen regulador codifica para una
proteína o producto difusible que puede ejercer su efecto en diferentes moléculas de ADN. En
el siguiente diploide parcial i
+
P O z
+
y
+
a
+
/ i
-
P O z
+
y
+
a
+
en ausencia de lactosa no hay
expresión de los genes estructurales mientras que en presencia de lactosa si se expresan. Esto
se debe a que la proteína represora normal producida por el gen i
+
al ser difusible se puede
unir a ambas regiones operadoras. En el siguiente esquema se indica lo que sucede en un
diploide parcial i
+
/i
-
en ausencia de inductor de inductor.
Diploide parcial i
+
/i
-
: Sin Inductor (lactosa)
En la siguiente tabla se indica la expresión de los genes del operón lactosa en los dos diplides
parciales, uno con en el regulador constitutivo (i- ) y el otro con en el operador constitutivo (O
C
).
Diploides parciales
Expresión de los genes estructurales del Operón
lactosa
Ausencia de inductor (Sin
lactosa)
Presencia de inductor
(Con lactosa)
Genotipo
z
+
y
+
a
+
z
+
y
+
a
+
i
+
P O z
+
y
+
a
+
/ i
+
P O
C
z
+
y
+
a
+
SI SI SI SI SI SI
i
+
P O z
+
y
+
a
+
/ i
-
P O z
+
y
+
a
+
NO NO NO SI SI SI
Mutantes del Promotor (O
O
): estos mutantes presetan una alteración en la secuencia de
bases nitrogenadas de la región promotora, como consecuencia la ARN-polimerasa no
reconoce la secuencia promotora y, por consiguiente, no se produce la transcripción de los
genes estructurales. A estos mutantes se les ha denominado "Operador cero" (O
O
), pero es
necesario recordar que afectan a la región promotora.
Además de los mutantes anteriormente indicados también se han obtenido otros tipos de
mutantes que afectan al gen regulador. Entre estos mutantes se encuentran los siguientes:
Mutante i
-
: la primera mutación que hemos visto es el mutante i
-
que ya hemos dicho que
es recesivo con respecto al i
+
en los diploides parciales(i
+
/i
-
). Da lugar a un represor que
es inactivo.
Mutante i
Q
: mutación en el promotor del gen regulador que codifica para la proteína
reresora (i
Q
): la consecuencia es que no aparece proteína represora y, por tanto, siempre
se están expresando los genes del operón lactosa tanto en ausencia como en presencia
del inductor. Se trata, por consiguiente, de un mutante de tipo constitutivo.
Mutante i
-d
: afecta al gen estructural de la proteína represora en la región que codifica
para el extremo amino terminal (NH2). Esta región es la encargada de reconocer la región
operadora. La proteína represora mutante se une al inductor (al IPTG) pero no es capaz
de unirse al operador. Esta mutación es dominante sobre la i
+
en los diploides parciales
(i
+
/i
-d
). En los diploides parciales la proteína represora mutante no se une a las regiones
operadoras y se produce siempre la trasncripción de los genes estructurales.
Mutante i
S
: afecta al gen estructural de la proteína represora modificando la parte central
de la proteína encargada de unirse al inductor (al IPTG). La proteína represora mutante se
une al operador pero no es capaz de reconocer al inductor (IPTG). Se trata de un mutante
que está siempre reprimido en el que no se expresan los genes del operón lactosa ya que
la proteína represora está permanentemente unida a la región operadora y no se suelta a
pesar de añadir el inductor. Este mutante es dominante sobre i
+
en los diploides parciales
(i
+
/i
S
). En los diploides parciales el represor mutante se une a ambas regiones operadoras
bloqueando la transcripción de los genes estructurales.
El comportamiento de las mutaciones i
-d
e i
S
en los diploides parciales se explica mejor
sabiendo que la proteína represora del operón lactosa es un tetrámero (proteína constituida por

cuatro cadenas polipéptídicas idénticas con un peso molecular cada una de 38.000). En el
diploide parcial (i
+
/i
S
) ,los tetrámeros con polipéptidos mutantes estarían unidos a las regiones
operadora acaparándolas de forma permanente e impidiendo la transcripción. En el diploide
parcial (i
+
/i
-d
) los polipéptidos normal y mutante se unen al azar para formar tetrámeros, de
manera que la mayoría de los tetrámeros tienen al menos un polipéptido mutante (15/16) y
solamente una pequeña fracción de los tetrámeros tiene todos los polipéptidos normales (1/16),
por tanto, la inmensa mayoría de los tetrámeros no son capaces de unirse a las regiones
operadoras y se transcribirían los genes estructurales.
OPERÓN LACTOSA: CONTROL POSITIVO
Como ya he mencionado anteriormente, el operón lactosa también está sujeto a un control de
tipo positivo, de manera que existe una proteína que estimula la transcripción de los genes
estructurales. En los sistemas de control negativo existe una proteína que que impide la
transcripción de los genes estructurales, en los sistemas de control positivo existe una prteína
activadora que estimula la transcripción de los genes. En principio existen cuatro tipos de
sistemas posibles de regulación de la expresión génica:
Tipo 1: Inducible, control negativo (operón lactosa y operón galactosa)
Tipo 2: Inducible, control positivo (operón arabinosa y operón maltosa)
Tipo 3: Represible, control negativo (operón triptófano y operón histidina)
Tipo 4: Represible, control positivo (no se han descrito)
Por supuesto, un operón pude estar sujeto a más de un tipo de control, como sucede en el caso
del operón lactosa que esta bajo control negativo ejercido por la proteína represora y bajo
control positivo ejecutado por una proteína activadora por catabolitos (CAP) también llamada
proteína activadora del AMP cíclico (CRP). El control positivo del operón lactosaa como
veremos está estrechamente relacionado con la Represión catabólica.
REPRESIÓN POR CATABOLITOS
Cuando la bacteria E. coli crece en un medio que contiene glucosa, prefiere este azúcar como
fuente de energía y como consecuencia los operones que ponen producen las enzimas
necesarias para obtener energía de otros azúcares están bloqueados. Uno de los catabolitos
del metabolismo de la glucosa actúa sobre el AMP cíclico (AMPc). El AMP cíclico (AMPc) es
necesario para la transcripción de todos los operones que son inhibidos por el catabolismo de la
glucosa. Es decir, para que se transcriban los genes del operón lactosa se necesitan niveles
elevados de AMPc. Esto mismo sucede con los operones de arabinosa, maltosa, galactosa,
etc.. Se trata. por tanto de un sistema general de control positivo que se denomina represión
catabólica. Cuando E. coli crece en un medio con glucosa, los niveles de AMPc son muy bajos
y como consecuencia no se transcriben los operones de otros azúcares. Aún no se conoce el
motivo por el que los niveles de AMPc son bajos cuando E. coli crece en un medio con glucosa
como fuente de energía.
Cuando E. coli crece en un medio sin glucosa pero con lactosa los niveles de AMPc son altos,
el AMPc se une a la proteína receptora receptora de AMPc (CRP) activándola y la proteína

activada CRP-AMPc a su vez estimula la transcripción de los genes estructurales del operón
lactosa y de otros operones de azúcares. La proteína activadora por catabolitos (CAP) es un
dímero que al unirse al AMPc se activa y estimula la transcripción de los genes del operón
lactosa, de manera que la proteína activadora CAP-AMPc es necesaria para la unión de la
ARN-polimerasa al promotor de los genes del operón lactosa. La proteína activadora CAP-
AMPc parece ser que se une a la región promotora cerca del nucleótido que ocupa la posición
-60 (60 nucleótidos antes del comienzo del gen z).
Los mutantes que afectan a la adenilato ciclasa, enzima que transforma el ATP en AMPc,
muestran niveles muy bajos de expresión de los genes del operón lactosa, debido a que los
niveles de AMPc son muy bajos en ausencia de glucosa.
Los mutantes que afectan a la proteína CRP o CAP también presentan niveles muy bajos de
expresión de los genes del operón lactosa en ausencia de glucosa.
EL OPERÓN TRIPTÓFANO
El operón triptófano (operón trp) es un sistema de tipo represible, ya que el aminoácido
triptófano (Correpresor) impide la expresión de los genes necesarios para su propia síntesis
cuando hay niveles elevados de triptófano. Sin embargo, en ausencia de triptófano o a niveles
muy bajos se transcriben los genes del operón trp. Los elementos del operón trp son en esencia
semejantes a los del operón lactosa:
Genes estructurales: existen cinco genes estructurales en el siguiente orden trpE-trpD-
trpC-trpB-trpA.
Elementos de control: promotor (P) y operador (O). El promotor y el operador están al
lado de los genes estructurales y en el siguiente orden: P O trpE-trpD-trpC-trpB-trpA.
Curiosamente, las enzimas codificadas por estos cinco genes estructurales actúan en la
ruta metabólica de síntesis del triptófano en el mismo orden en el que se encuentran los
genes en el cromosoma.
Gen regulador (trpR): codifica para la proteína reguladora. Este gen se encuentra en otra
región del cromosoma bacteriano aunque no muy lejos del operón.
Correpresor: triptófano.
En el siguiente esquema se indican los elementos del Operón Triptófano:
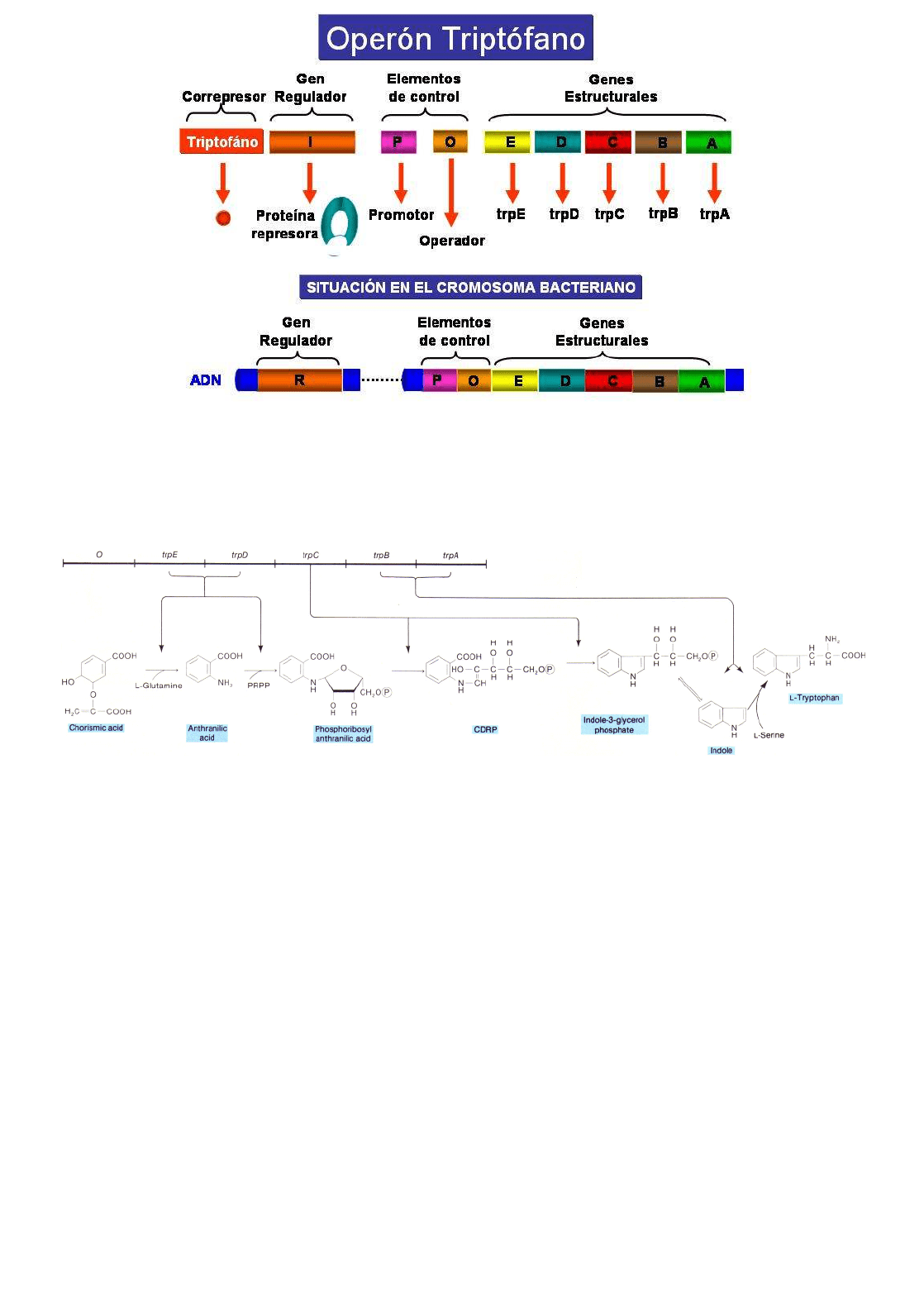
Elementos del Operón Triptófano
Los genes estructurales del operón triptófano se encuentran en el mismo orden que actúan las
productos codificados por ellos en la ruta biosintética del triptófano (ver el siguiente esquema).
Orden de los genes estructurales del operón triptófano y ruta de síntesis del triptófano
En ausencia de triptófano, o cuando hay muy poco, la proteína reguladora producto del gen
trpR no es capaz de unirse al operador de forma que la ARN-polimerasa puede unirse a la
región promtora y se transcriben los genes del operón triptófano.
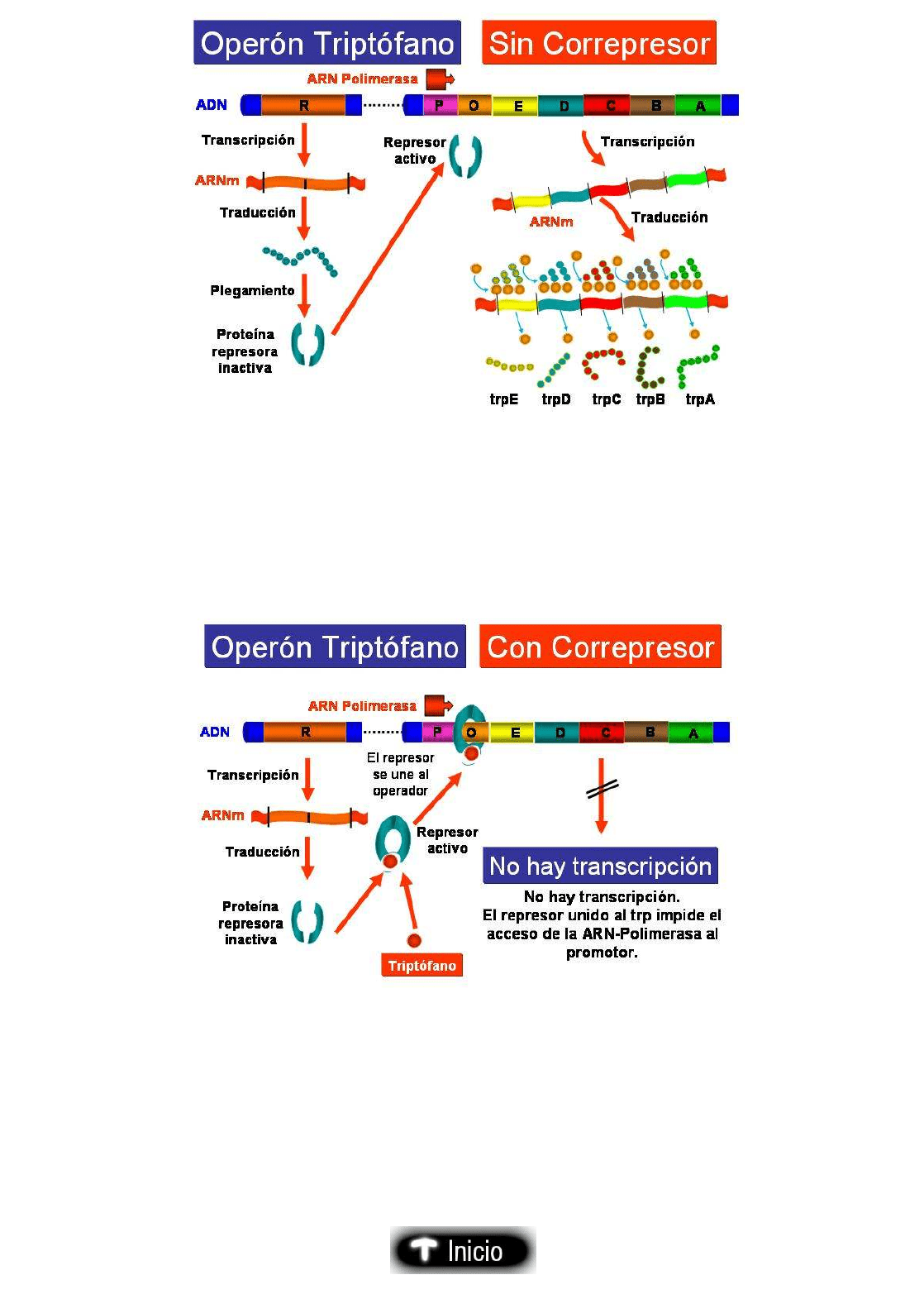
Operón triptófano: en ausencia de triptófano
En presencia de triptófano, el triptófano se une a la proteína reguladora o represora cambiando
su conformación, de manera que ahora si puede unirse a la región operadora y como
consecuencia la ARN-polimerasa no puede unirse a la región promotora y no se transcriben los
genes estructurales del operón trp.
Operón triptófano: en presencia de triptófano
Por tanto, la diferencia esencial entre el operón lac (inducible) y el operón trp (represible), es
que en este último el represor del triptófano solamente es capaz de unirse al operador cuando
previamente está unido al trp.
Al estudiar más profundamente el operón trp se encontró que además del mecanismo de
regulación represor-operador existía otro mecanismo de regulación que se denominó
regulación por atenuación.
Este documento contiene más páginas...
Descargar Completo
23-Regulación de la expresión génica en procariontes.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.