
E L A G U A
Tema: LA MOLÉCULA DEL AGUA

“Toda vida, desde un punto de vista
energético, no es otra cosa que una
función del agua, y nosotros mismos
somos poco mas que una masa de agua
marina a la que le ha crecido una piel
que le permite arrastrarse por la tierra”
A. Szent Gyorgyi

MOLECULA DE AGUA
El agua es el principal componente de nuestro cuerpo.
El ser humano no puede estar sin beberla más de cinco
o seis días sin poner en peligro su vida.
Nuestro cuerpo tiene un 80 % de agua cuando
nacemos y el peso corporal de un adulto esta
constituido por ella, todas las células y demás líquidos
biológicos se encuentran condicionados por su
presencia.
Las imágenes e ilustraciones de la web son utilizadas solo con fines educativos y sin fines de lucro

La mayor parte de este agua se encuentra
en el interior de las células y es el agua
intracelular: ejemplo el citoplasma.
El resto se denomina agua extracelular y
es la que circula en el torrente sanguíneo
y forma parte de sus componentes tal
como lo es el plasma.
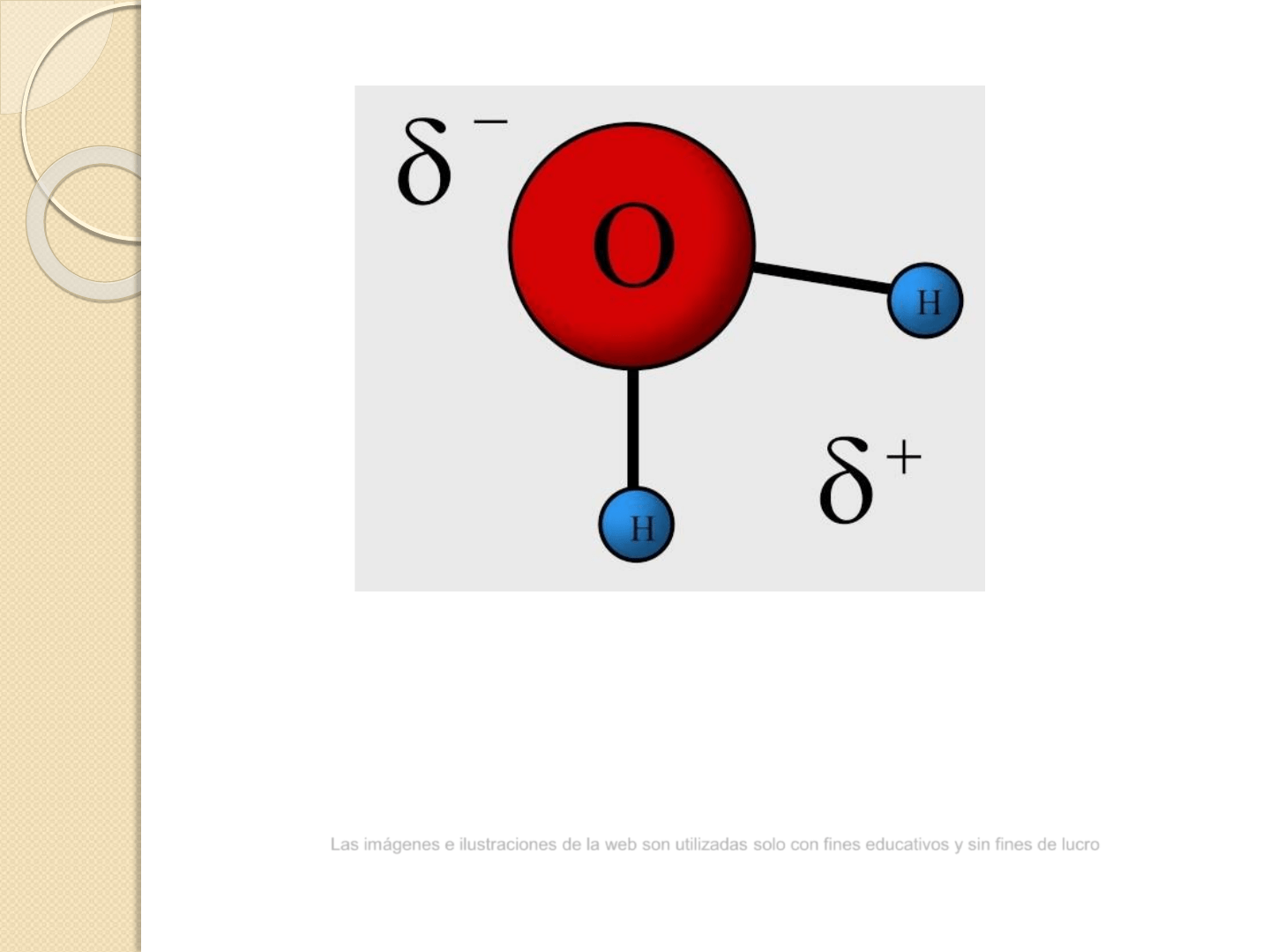
Sus átomos están unidos por enlaces covalentes
simples.
Las imágenes e ilustraciones de la web son utilizadas solo con fines educativos y sin fines de lucro
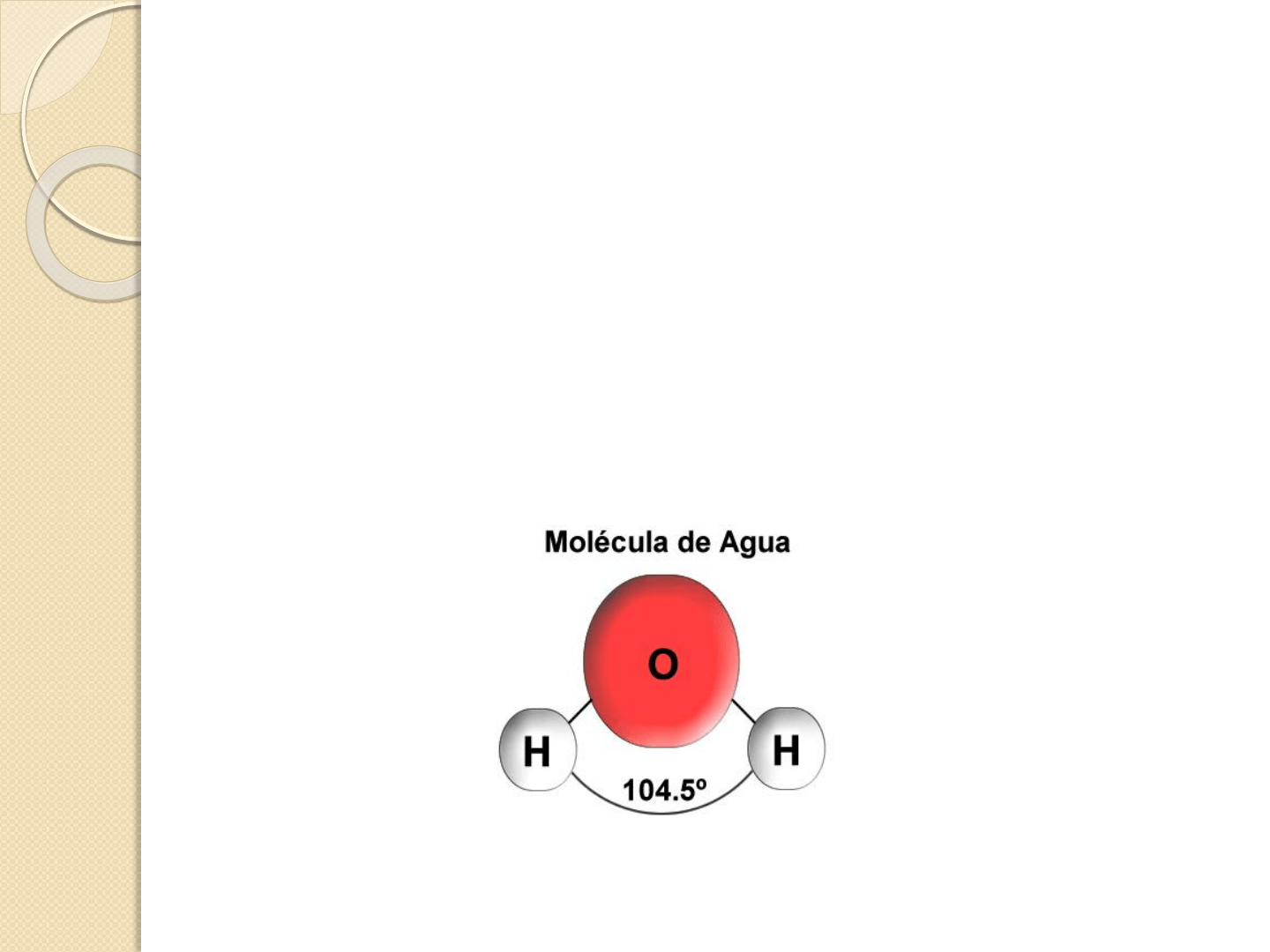
LA MOLECULA DE AGUA ES POLAR
Si los átomos estuvieran dispuestos en línea recta el centro de gravedad
de las cargas positivas estaría situado en el centro de la molécula,
coincidiendo con la carga negativa. Como por ejemplo en el CO
2.
H-O-H
Centro de gravedad apolar
Sin embargo el ángulo entre los enlaces es de 104, 5º
Las imágenes e ilustraciones de la web son utilizadas solo con fines educativos y sin fines de lucro

Se forma un dipolo.
Posee una distribución asimétrica de sus electrones, lo que la
convierte en una molécula polar.
Alrededor del oxígeno se concentra una densidad de carga
negativa, mientras que los núcleos de hidrógeno parcialmente
desprovistos de sus electrones poseen una densidad de carga
positiva.
Pero eléctricamente es neutra.
+ +
-

.
El oxígeno es más electronegativo que el hidrógeno
y atrae con más fuerza a los electrones de cada
enlace.
El resultado es una molécula de agua con carga
total neutra es decir igual número de protones que
de electrones.
Su polaridad permite que atraiga
electrostáticamente a otras moléculas de agua
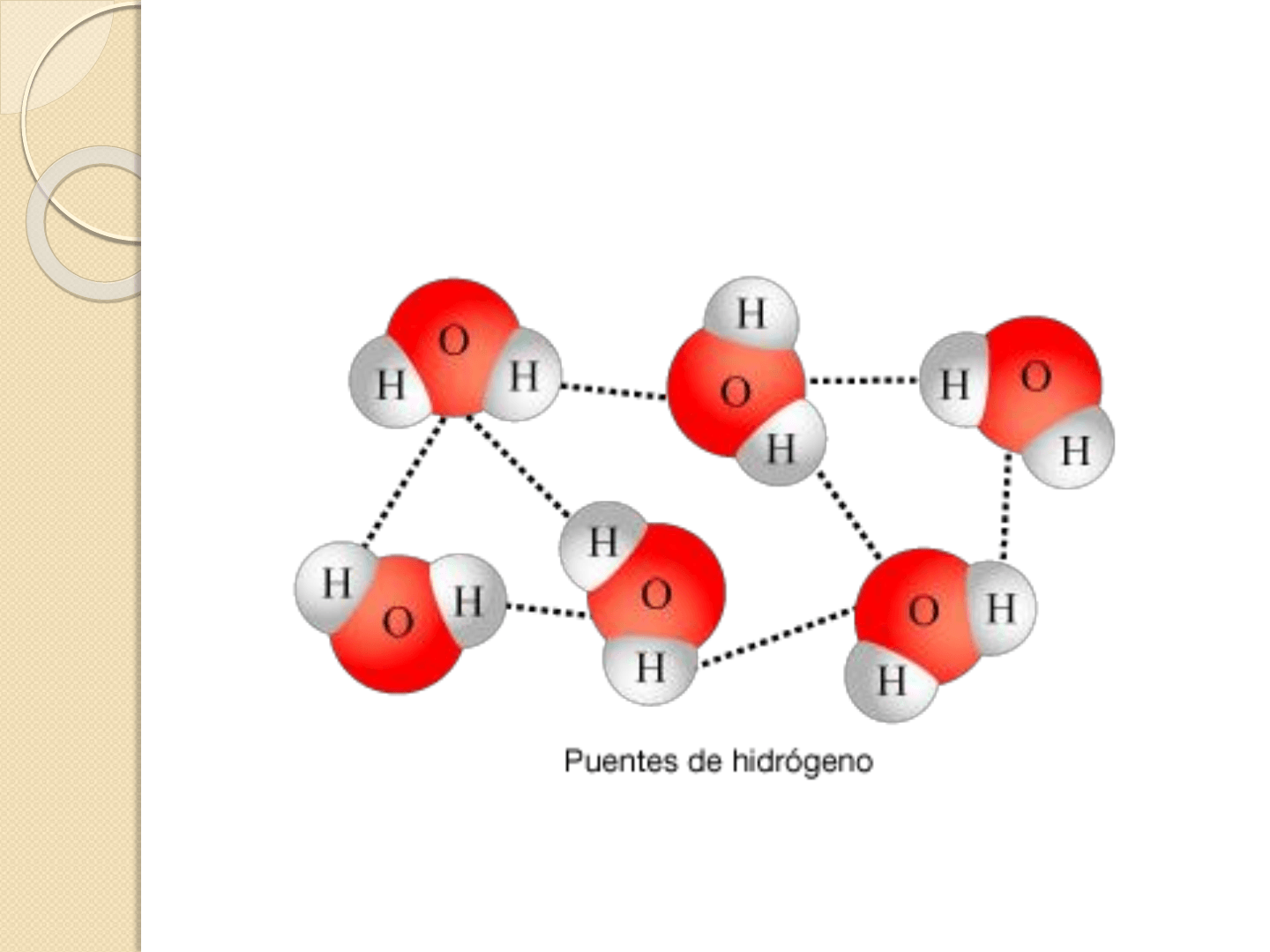
Se dan interacciones dipolo-dipolo entre las propias moléculas
de agua, formándose enlaces por puentes de hidrógeno
Las imágenes e ilustraciones de la web son utilizadas solo con fines educativos y sin fines de lucro
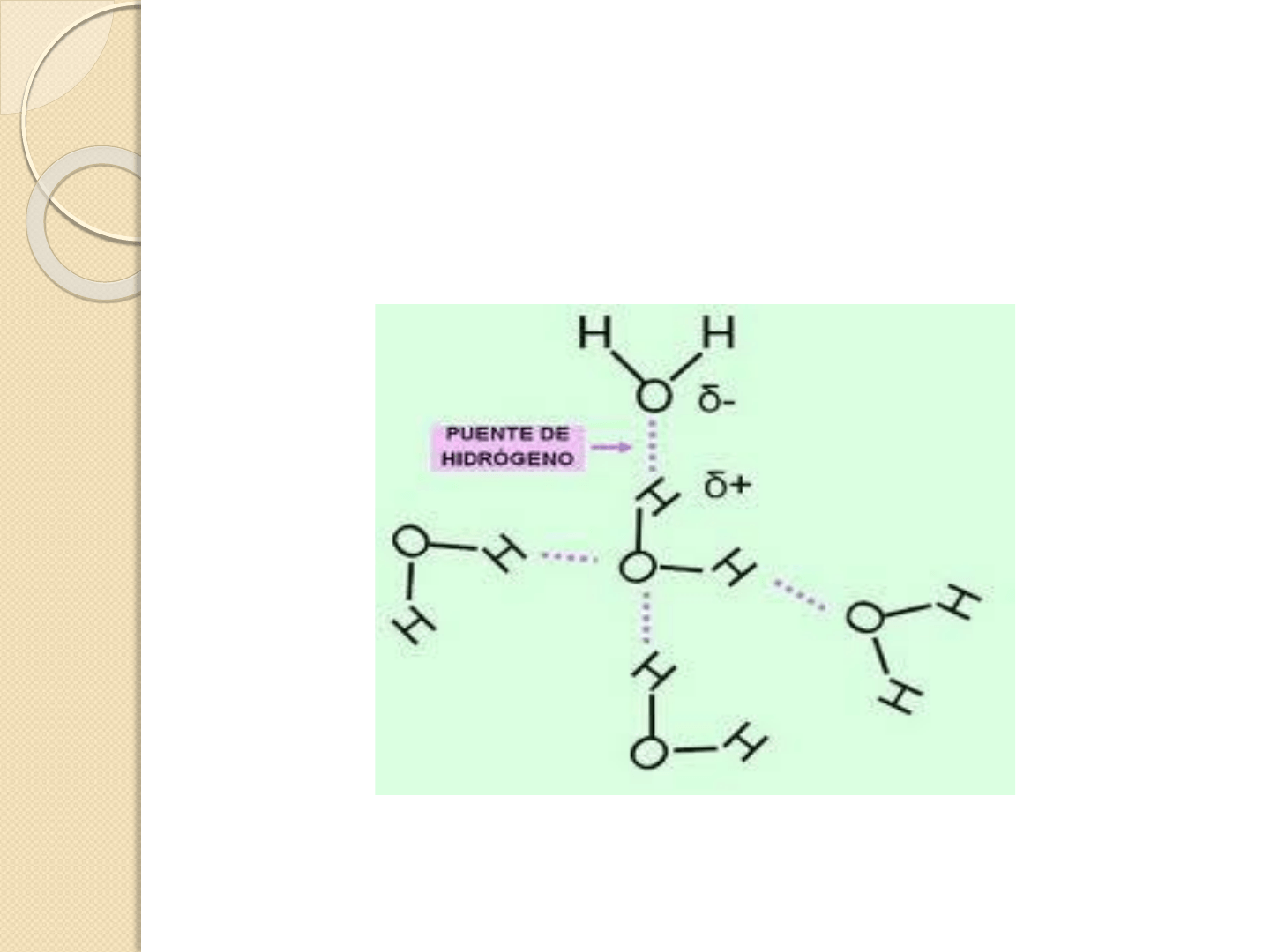
. La carga parcial negativa del oxígeno de una molécula ejerce
atracción electrostática sobre las cargas parciales positivas
de los átomos de hidrógeno de otras moléculas adyacentes.
.
Las imágenes e ilustraciones de la web son utilizadas solo con fines educativos y sin fines de lucro

Aunque son uniones débiles, el hecho
de que alrededor de cada molécula de
agua se dispongan otras cuatro
molécula unidas por puentes de
hidrógeno permite que se forme en el
agua una estructura de tipo reticular,
responsable de la peculiaridad de sus
propiedades físico-químicas
Las imágenes e ilustraciones de la web son utilizadas solo con fines educativos y sin fines de lucro

Sin embargo las uniones químicas puente de H son inestables se
forman y se rompen con gran rapidez….esa red dinámica explica los
valores elevados de calor de vaporización y el punto de ebullición.
Las uniones puente de H proporcionan una elevada tensión
superficial, mayor fluidez y menor viscosidad que la correspondiente
a moléculas poliméricas.
Las imágenes e ilustraciones de la web son utilizadas solo con fines educativos y sin fines de lucro
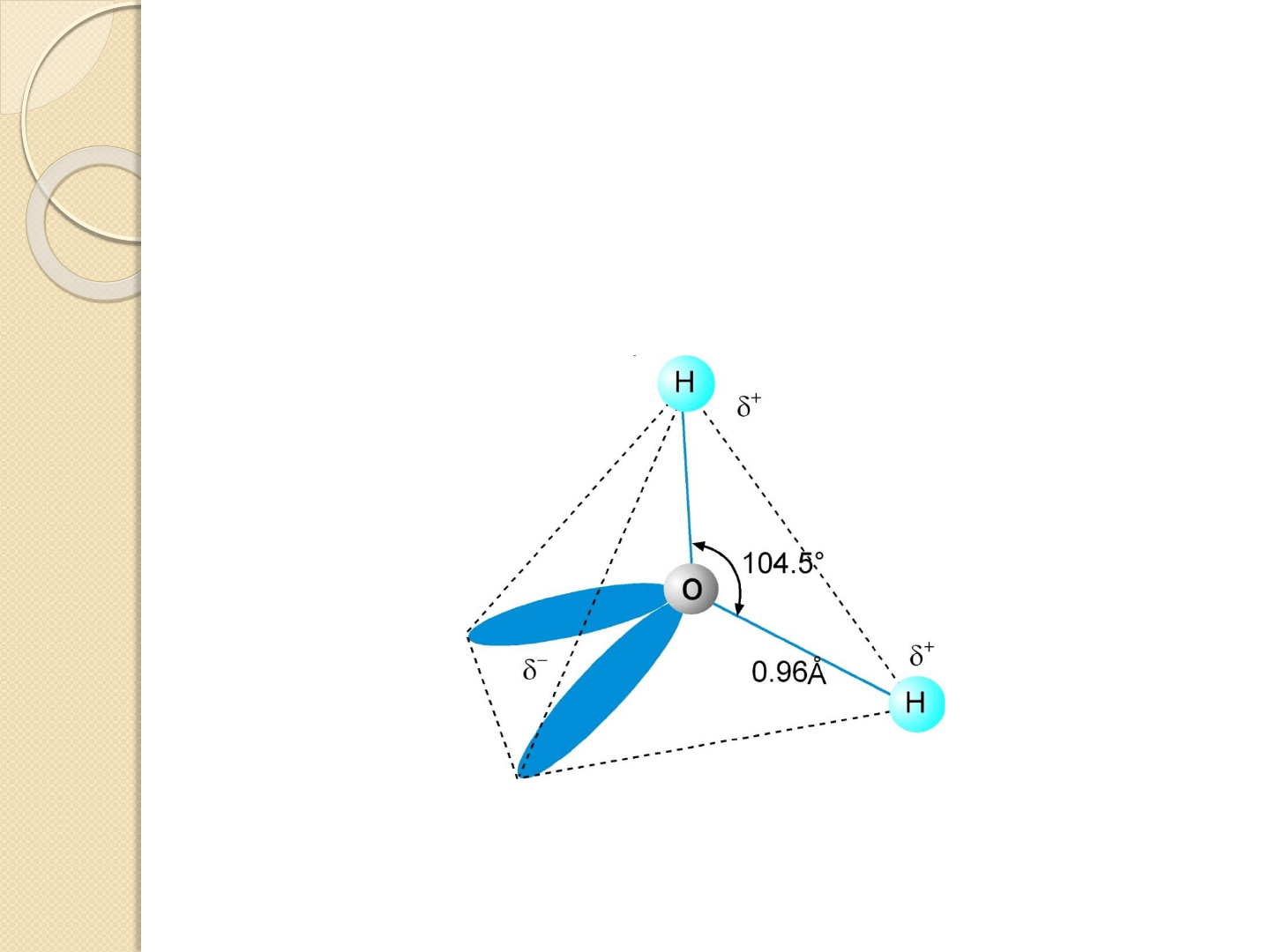
El carácter direccional del enlace puente de H determina
relaciones geométricas en las asociaciones poli-moleculares del
agua. Los enlaces O-H se dirigen hacia los vértices de un
tetraedro y los electrones no compartidos se orientan hacia los
dos vértices del tetraedro.
Las imágenes e ilustraciones de la web son utilizadas solo con fines educativos y sin fines de lucro
EL AGUA COMO SOLVENTE
Las sustancias iónicas son solubles en agua:
Na+ Cl-
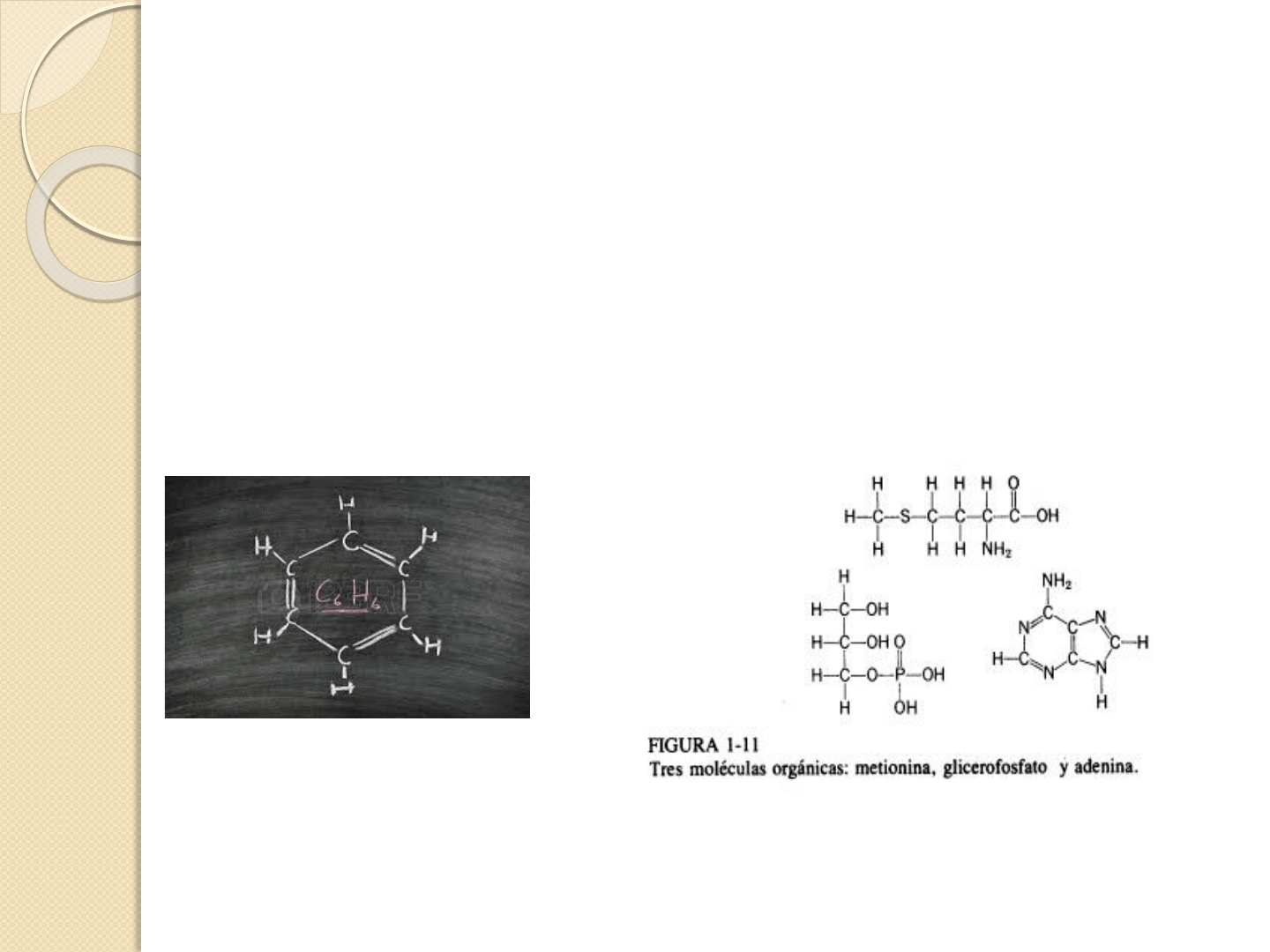
Los compuestos iónicos y polares no iónicos, son
hidrófilos: pueden interaccionar con las moléculas de
agua y formar soluciones estables. Ej. Benceno.
Benceno.
Las imágenes e ilustraciones de la web son utilizadas solo con fines educativos y sin fines de lucro
Este documento contiene más páginas...
Descargar Completo
1 Molécula de Agua.ppt
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
