4 - TABLA PERIÓDICA
Gran parte de los elementos conocidos en la actualidad se descubrieron entre 1800 y
1900. A medida que los fueron descubriendo, los químicos observaron que, a pesar de
las diferencias en el número de protones y las masas, muchos elementos tenían
comportamientos semejantes. El reconocimiento de estas regularidades en las
propiedades químicas y físicas, así como la necesidad de organizar la gran cantidad de
información disponible, condujeron al desarrollo de la tabla periódica.
Una de las primeras clasificaciones periódicas de los elementos se le atribuye al
químico ruso Dimitri Mendeleev. En 1869, basado en trabajos de investigadores
contemporáneos, propuso una clasificación de los elementos conocidos hasta el
momento, basado en propiedades medibles empíricamente en aquella época como la
masa atómica, el punto de fusión, densidad y la capacidad de formar compuestos.
Vale destacar que su trabajo fue anterior al modelo atómico tal como lo conocemos,
sin embargo, logró una clasificación y orden racional que tiempo después se comprobó
que era correcta bajo la luz de la teoría atómica. Además, predijo (con muy buena
precisión) la existencia de elementos que no habían sido descubiertos hasta ese
momento.
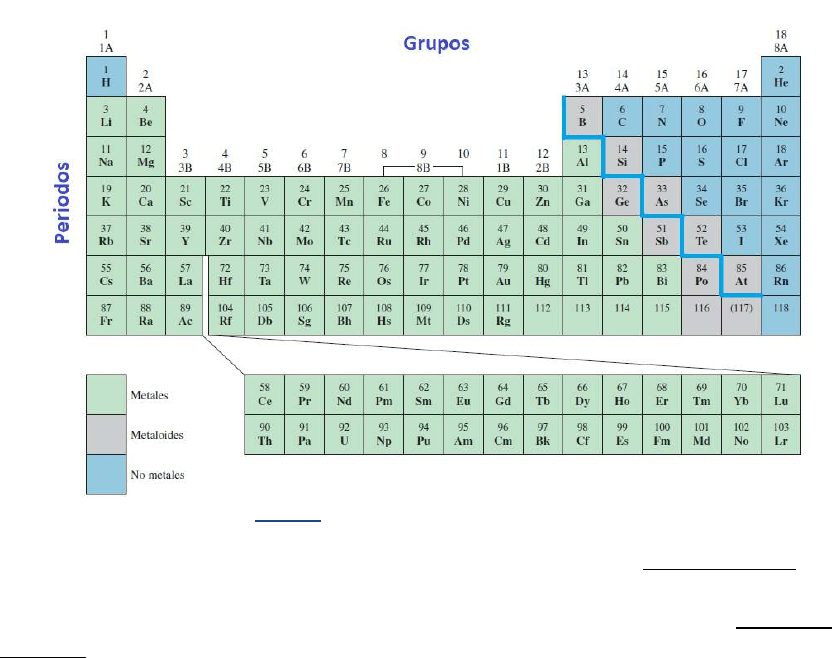
En la tabla periódica, tal la conocemos en la actualidad, los elementos están
ordenados de acuerdo a su número atómico (que aparece sobre el símbolo del
elemento) en filas o períodos y columnas o grupos. Dos elementos consecutivos en un
grupo (misma columna) tienden a tener comportamientos similares, a pesar de la
significativa diferencia de masas.
Figura 1: Tabla periódica de los elementos
En este curso vamos a trabajar con los elementos que se llaman representativos, esto
significa que son característicos del grupo que representan y, por lo tanto, tienen
cierta regularidad en sus propiedades. Estos elementos se ubican en los bloques s y
bloque p de la tabla, como se puede ver en la Figura 2.
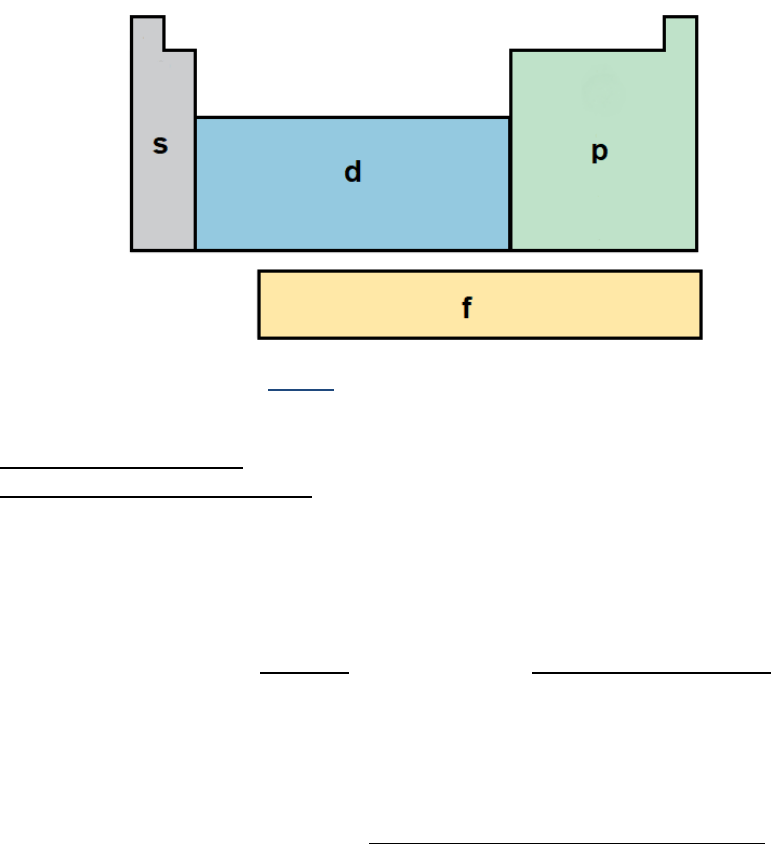
Figura 2: Bloques de la tabla periódica.
Los elementos ubicados en el bloque d (tienen orbitales d incompletos) se llaman
elementos de transición, y los del bloque f (tienen orbitales f incompletos) son los
elementos de transición interna. Estos no los vamos a ver mucho en este curso, porque
no presentan esa regularidad en sus propiedades.
La ubicación de los elementos en la tabla no sólo responde a su número atómico
creciente, sino que tiene su correlato con su configuración electrónica:
● El período nos indica en qué nivel se encuentran los electrones más externos.
Por ejemplo, todos los elementos ubicados en el período 3 tienen sus electrones de
mayor energía (más externos) en el nivel 3, y por lo tanto dicho nivel está incompleto
(excepto en el último elemento, al final del período).
● El grupo, por su parte, nos indica la cantidad de electrones en el último nivel.
Por ejemplo, todos los elementos del grupo 1 tienen 1 electrón en su último nivel y,
además, comparten la misma configuración externa ns
1
.
Cómo determinar en qué grupo y período se encuentra un elemento
Necesitamos conocer su número atómico, que nos dice cuántos protones hay en el
núcleo, pero también cuántos electrones tiene un elemento cuando es neutro.
Hacemos su configuración electrónica y determinamos la CEE
El n del ultimo nivel es = al número de período
Contamos los electrones externos y:
- si el ultimo electrón es s → N° grupo = n° electrones externos (s)
- si el ultimo electrón es p → N° grupo = n° electrones externos (s + p) + 10
- si el ultimo electrón es d → N° grupo = n° electrones externos (s + d)
Ejemplos: Ubicar en grupo y período (sin utilizar la tabla periódica):
a) Li (Litio) (Z = 3)
Su configuración electrónica es 1s
2
2s
1
; y su CEE es 2s
1
.
El litio está ubicado en el Período 2 (máximo valor de n) y en Grupo 1 pues tiene un
solo electrón en su último nivel.
b) Br (bromo) (Z = 35)
Con ayuda de la regla de las diagonales podemos decir:
La CE es 1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
3d
10
4p
5
La CEE es 4s
2
4p
5
--- tiene 2 + 5 = 7 electrones externos, en el nivel 4
Como la CEE termina en un orbital p, al número de electrones de la CEE hay que
sumarle 10: 7 + 10 = 17
El bromo se ubica en el Período 4, Grupo 17.
CEE de los elementos representativos
Como decíamos antes, todos los elementos del grupo 1 tienen 1 electrón en su último
nivel y, además, comparten la misma configuración externa ns
1
. Si hacemos el mismo
análisis con los elementos del grupo 2, veremos que todos tienen CEE ns
2
.
En el bloque s el número de grupo es exactamente igual al número de electrones
externos.
Si ahora vemos los siguientes grupos de elementos representativos, observamos que
los electrones que se van agregando se ubican en orbitales p, y que tienen las CEE: ns
2
np
1
, ns
2
np
2
, ns
2
np
3
, y así sucesivamente hasta ns
2
np
6
(nivel p completo).
En el bloque p, el número de grupo se determina considerando los electrones del
último nivel de energía (presentes en los orbitales s y los orbitales p) sumado 10.
Este número no es arbitrario, ya que sale de tener en cuenta los 10 electrones que
completarían el bloque d, que aparece intercalado (en n=4) entre los bloques s y p.
Tabla 1: CEE de los grupos representativos
Grupo
CEE
1
ns
1
2
ns
2
13
ns
2
np
1
14
ns
2
np
2
15
ns
2
np
3
16
ns
2
np
4
17
ns
2
np
5
18
ns
2
np
6

Como ejemplo, si vemos en la Tabla 1, el grupo 13 tiene una CEE = ns
2
np
1
. En el último
nivel de energía (n) todos los elementos tienen 3 electrones (2 en s y 1 en p), y como
nos encontramos en el bloque p, se suma 10, resultando 13 como el número de grupo.
Y lo mismo sucederá con los grupos 14 al 18.
La numeración de los grupos aquí explicada es la numeración moderna de los grupos
(va del 1 al 18) y es la que usaremos en el curso. Existe otra numeración más antigua,
que se puede ver en varias tablas periódicas, que emplea numeración romana y letras.
Se usa la letra A para los elementos representativos (bloques s y p) y la letra B para los
elementos de transición (bloque d). De esta manera los elementos de los grupos 1 y 2
quedarían como IA y IIA, respectivamente. El grupo 13 sería IIIA, y los subsiguientes
quedarían IVA, VA, VIA, VIIA y VIIA. Mientras que los grupos IB al VIIIB corresponden a
los elementos de transición.
Por razones históricas, algunos grupos tienen nombres propios: los nombres más
comunes están en la Tabla 2. Los elementos del grupo 18 se denominan Gases Nobles
o Inertes por ser muy poco reactivos, es decir que tienen poca tendencia a participar
de reacciones químicas y formar compuestos.
Tabla 1: Nombres tradicionales de los grupos de elementos representativos
Grupo
Nombre del grupo
Elementos
1 (IA)
metales alcalinos
Li, Na, K, Rb, Cs y Fr
2 (IIA)
metales alcalino-térreos
Be, Mg, Ca, Sr, Ba, Ra
17 (VIIA)
halógenos
F, Cl, Br, Y y At
18 (VIIIA)
gases nobles o inertes
He, Ne, Ar, Kr, Xe, Rn
Los elementos de este grupo tienen CEE de la forma ns
2
np
6
, a excepción del He (helio),
cuya configuración electrónica es 1s
2
, pero que tiene también propiedades similares a
los demás gases nobles.
Ejemplo de aplicación:
Escribir la configuración electrónica de distintos elementos de los grupos 1 (IA), 2 (IIA),
14 (VIA) y 16 (VIA). Ver la tendencia. ¿En qué se parecen?
Al analizar la CE de los elementos de un grupo en particular, se observa con claridad
que siguen un patrón: todos los elementos del mismo grupo tienen configuraciones
electrónicas externas semejantes.
Por ejemplo, si observamos la CEE de los elementos del grupo 1 (IA) es, de manera
general, ns
1
. Donde n es el nivel (o período) para un determinado elemento, y el
superíndice 1 es la cantidad de electrones externos. Este número coincide con el
número de grupo.
Por lo tanto, la CEE nos dice cómo ubicar al elemento en la Tabla Periódica (es decir,
grupo y período en el que se encuentra).

Ejercicio:
Repetir el mismo procedimiento para el resto de los grupos elegidos. Observar la CEE y
escribirla en forma general: ns
a
np
b
(a, b = número de electrones correspondiente a
cada subnivel)
Iones
Cuando un átomo toma o cede electrones adquiere una carga neta, negativa o
positiva; estas partículas cargadas se llaman iones. El número de protones, ubicados
en el núcleo, permanece igual durante las reacciones químicas, pero se pueden
intercambiar electrones.
La cesión de uno o más electrones en un átomo neutro forma un catión, un ion con
carga neta positiva. Por ejemplo, un átomo de sodio (Na) fácilmente puede ceder un
electrón para formar el catión sodio, que se representa como Na
+
.
Átomo Na
Catión Na
+
11 protones
11 protones
11 electrones
10 electrones
Por otra parte, un anión es un ion cuya carga neta es negativa debido a que toma uno
o más electrones. Por ejemplo, un átomo de cloro (Cl) puede tomar un electrón para
formar el anión cloruro, Cl
−
.
Átomo Cl
Anión Cl
-
17 protones
17 protones
17 electrones
18 electrones
Ion más probable
Para determinar si un átomo tiene tendencia a formar un catión o un anión,
tomaremos como criterio: el ion formado tendrá la configuración electrónica del gas
noble más cercano en la Tabla Periódica. Como se dijo más arriba, los gases nobles son
particularmente estables (poco reactivos), entonces los iones formados buscarán tener
la configuración de estos elementos, para alcanzar la mínima energía y por lo tanto a la
estabilidad.
Si analizamos los ejemplos anteriores bajo este criterio, podemos ver que cuando el
átomo Na cede un electrón la configuración resultante es idéntica a la del neón, el
elemento inmediatamente anterior al sodio. Se dice que el ion Na
+
es isoelectrónico
con el Ne.
Átomo Na
Catión Na
+
11 electrones
10 electrones
CE
1s
2
2s
2
2p
6
3s
1
1s
2
2s
2
2p
6
= CE (Ne)

Por su parte, si analizamos el ion más probable del elemento cloro, vemos que cuando
el átomo toma un electrón se llega a la configuración electrónica de un gas noble, ya
que la CEE es 3s
2
3p
6
, o sea es isoelectrónico con argón.
Átomo Cl
Anión Cl
-
17 electrones
18 electrones
CE
1s
2
2s
2
2p
6
3s
2
3p
5
1s
2
2s
2
2p
6
3s
2
3p
6
= CE (Ar)
Ejercicio de aplicación:
Determinar el ion más probable de cada uno de los siguientes elementos:
a) S (Z=16)
b) Mg (Z=12)

06-el enlace quimico.pdf
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Descargar
 Estamos procesando este archivo...
Estamos procesando este archivo...
 Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.
Lamentablemente la previsualización de este archivo no está disponible. De todas maneras puedes descargarlo y ver si te es útil.